Сайзен® 8 Мг Клик.изи
Регистрационный номер: UA/1567/01/02
Импортёр: Арес Трейдинг С.А.
Страна: ШвейцарияАдреса импортёра: Зон Индустриель де Л'Урьетаз, 1170 Обонн, Швейцария
Форма
порошок для приготовления раствора для инъекций по 8 мг, 1 или 5 флаконы с порошком, 1 или 5 картриджи из 1,37 мл растворителя(0,3 % (г./о.) раствор м-крезола в воде для инъекций) предварительно собранных в 1 или 5 пристроил для растворения(клик.изи), что состоят из 1 или 5 корпуса устройства и 1 или 5 стерильных переходных канюль в картонной коробке
Состав
1 флакон с порошком содержит 8 мг соматропину(рекомбинантного человеческого гормона роста)
Виробники препарату «Сайзен® 8 Мг Клик.изи»
Страна производителя: Италия
Адрес производителя: Виа делле Магнолиє 15(р-н Промышленная Зона), 70026 Модуньо(Баре), Италия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
САЙЗЕНâ 8 мг клик изи
(SAIZENâ 8 mg click easy®)
Состав
действующее вещество: соматропин;
1 флакон с порошком содержит 8 мг соматропину(рекомбинантного человеческого гормона роста);
вспомогательные вещества: сахароза, кислота фосфорная и натрию гидроксид(для доведения рН);
растворитель: 1 картридж с бактериостатическим растворителем содержит 1,37 мл 0,3 % (г./о.) раствора м-крезола в воде для инъекций.
Врачебная форма. Порошок для приготовления раствора для инъекций.
Основные физико-химические свойства: препарат - белое или почти белое лиофилизированное вещество, растворитель - прозрачный бесцветный раствор.
Фармакотерапевтична группа. Гормоны передней судьбы гипофиза и их аналоги. Соматропін.
Код АТХ Н01А С01.
Фармакологические свойства.
Фармакодинамика.
Препарат Сайзенâ 8 мг клик.изи содержит рекомбинантный гормон роста человека(соматропин), выработанный с помощью генно-инженерных методов из клеток млекопитающих. Соматропін - это пептид, который состоит из 191 аминокислоты и является идентичным человеческому гипофизарному гормону роста за аминокислотной последовательностью и составом, а также за картой пептидов, изоэлектрической точкой, молекулярным весом, изомерной структурой и биологической активностью.
Соматропіну присущие анаболические и антикатаболические свойства, то есть он влияет не только на рост, но и на телосложение и метаболизм. Соматропін взаимодействует со специфическими рецепторами на клетках разного типа, включая миоциты, гепатоциты, адипоцити, лимфоциты и гематопоэтические клетки. Некоторые из таких эффектов опосредствуют другим классом гормонов, известным как соматомедин(IGF - 1 и IGF - 2).
В зависимости от величины дозы, введения препарата приводит к повышению уровней IGF - 1(инсулиноподобный фактор роста 1), IGFBP - 3(белок 3, что связывает инсулиноподобный фактор роста), неетирификованих жирных кислот и глицерина и снижения уровней мочевины в крови, а также к уменьшению мочевого выведения азоту, натрию и калию. Длительность повышения уровней гормона роста может играть важную роль в определении степени его эффективности. Для высоких доз соматропину вероятное существование явления относительного насыщения эффекта, но это не касается гликемии и мочевого выведения С-пептиду, которые существенно растут лишь после введения высоких доз препарата(20 мг).
Фармакокинетика.
Фармакокинетика препарата имеет линейный характер по меньшей мере при применении доз до 8 МО(2,67 мг). При применении высших доз(60 МО/20 мг) нельзя исключать некоторую нелинейность ответа, которая, однако, не имеет клинического значения.
После внутривенного введения препарата здоровым добровольцам объем распределения в равновесном состоянии представляет приблизительно 7 л, общий метаболический клиренс − приблизительно 15 л/час, тогда как почечный клиренс является незначительным. Период полувыведения препарата представляет 20 − 35 минуты.
После разового подкожного или внутримышечного введения препарата мнимый конечный период полувыведения более длителен и представляет приблизительно от 2 до 4 часов, что предопределенно процессом абсорбции, который ограничивает скорость выведения.
Максимальная сывороточная концентрация соматропину достигается приблизительно через 4 часы после введения, после чего сывороточный уровень гормона роста возвращается к базовому в течение 24 часов, что свидетельствует об отсутствии кумуляции соматропину при повторных введениях.
Абсолютная биодоступность соматропину при внутримышечном и подкожном введении представляет 70 − 90 %.
Поражение почек
Известно, что клиренс соматропину у пациентов с поражением почек уменьшается. Однако по клиническим данным, это не нуждается регулирования дозы препарата.
Поражение печенки
Известно, что клиренс соматропину у пациентов с поражением печенки уменьшается. Однако клиническое значение этого факта неизвестно, поскольку влияние препарата на пациентов с поражением печенки не изучалось.
Клинические характеристики
Показание
Деть
- Задержка роста у детей, вызванная уменьшением или отсутствием секреции эндогенного гормона роста.
- Задержка роста у девочек из дисгенезиею гонад(синдром Тернера), подтвержденной хромосомным анализом.
- Задержка роста у детей препубертатного возраста, вызванная хронической почечной недостаточностью.
- Нарушение роста у низкорослых детей в возрасте от 4 лет(индекс стандартного отклонения(SDS) существующего роста < - 2,5 и с учетом роста родителей SDS < - 1), которые родились с ростом, который не отвечает гестационному возраста, а масса тела та/або длина которых при рождении была меньше - 2 SD(стандартное отклонение) и которые не догнали необходимый рост(SDS скорости роста < 0 в течение последнего года).
Взрослые
- Заместительная терапия у взрослых с выраженным дефицитом гормона роста, диагностированным за одним динамическим тестом на дефицит гормона роста.
Взрослые пациенты также должны отвечать нижеозначенным критериям.
Дефицит гормона роста, диагностированный в детстве
Пациенты, в которых недостаточность гормона роста была диагностирована в детстве, перед началом гормонозамисной терапии с применением препарата Сайзенâ 8 мг клик.изи должны пройти повторное обследование для подтверждения дефицита гормона роста.
Дефицит гормона роста, диагностированный во взрослом возрасте
Пациентам должен быть поставленный диагноз недостаточности гормона роста в результате заболеваний гипоталамуса или гипофиза и дефицита по меньшей мере еще одного гормона(за исключением пролактину). Кроме того, перед началом применения соматропину следует начать соответствующую гормонозамисну терапию другими гормонами.
Противопоказание
- Гиперчувствительность к действующему веществу или к любым вспомогательным веществам порошка или растворителя;
- закрытие эпифизарных зон роста у детей;
- наличие активных новообразований; к началу лечения следует удостовериться, что любые существующие новообразования находятся в неактивной форме и любая противоопухолевая терапия завершена; лечение следует прекратить в случае наличия доказательств роста опухоли;
- подтвержденный прогресс или рецидив основного внутричерепного объемного процесса;
- острые критические состояния, которые развились в результате осложнений после открытой операции на сердце, брюшной полости, в результате множественных травм, острой дыхательной недостаточности или подобных патологий;
- трансплантация почки у детей с хронической почечной недостаточностью; применение соматропину необходимо прекратить на время трансплантации почки;
- пролиферативная или предпролиферативная диабетическая ретинопатия.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Одновременное применение кортикостероидов ингибуе ускорение роста, вызванное препаратами, которые содержат соматропин. Для предотвращения любому ингибуючему влиянию кортикостероидов на действие гормона роста следует провести тщательную корректировку заместительной терапии пациентов с дефицитом адренокортикотропного гормона.
Кроме того, у некоторых пациентов начало гормонозамисной терапии соматропином может привести к проявке замаскированной вторичной недостаточности надпочечников за счет снижения активности 11β-гідроксистероїд-дегідрогенази типа 1(11β- HSD1) - ферменту, который превращает неактивный кортизон в кортизол. Начало применения соматропину у пациентов, которые проходят курс заместительной терапии кортикостероидами, может привести к появлению проявлений дефицита кортизола. В таких случаях может быть нужным корректировка дозы кортикостероидов.
Поскольку пероральные препараты естрогенив могут ослаблять ответ на лечение соматропином, что выражается в снижении сывороточных уровней IGF - 1, пациентам, которые проходят курс заместительной терапии пероральными препаратами естрогенив, может быть нужным увеличение дозы соматропину.
Даны, полученные в исследовании врачебных взаимодействий при лечении взрослых пациентов с дефицитом гормона роста, дают возможность допустить, что введение соматропину может увеличивать клиренс соединений, которые метаболизуються изоферментами системы цитохрома Р450. Клиренс соединений, что метаболизуються при участии системы цитохрома Р450 3А4(например, половые гормоны, кортикостероиды, противосудорожные препараты и циклоспорин), может существенно расти, что будет приводить к снижению уровня этих соединений в плазме крови. Клиническое значение этого явления неизвестно.
Особенности применения
Лечение препаратом следует проводить под постоянным надзором врача, который имеет опыт диагностирования и лечения пациентов с дефицитом гормона роста.
Новообразование
Пациентов из внутришне- и зовнишнечерепними новообразованиями в стадии ремиссии, которые лечатся гормоном роста, следует регулярно тщательным образом обследовать. При лечении пациентов с дефицитом гормона роста в результате внутричерепных опухолей следует проводить частые медицинские обследования для выявления возможного прогресса или рецидивов основного заболевания.
Существуют лишь ограниченные данные относительно риска развития опухолей во время лечения гормоном роста. Поэтому во время лечения препаратами соматропину пациенты должны находиться под тщательным надзором.
Сообщалось о росте риска развития вторичных новообразований у детей, которые болели раком, а после вылечивания первичного рака лечились соматропином. Среди таких вторичных новообразований самыми распространенными были внутричерепные опухоли, в частности менингиомы, которые наблюдались у пациентов после лучевой терапии первичного новообразования председателя. Однако при лечении соматропином детей с вылеченным раком не сообщалось об увеличении риска рецидива. Учитывая ограниченность данных, во время лечения препаратом пациенты должны находиться под тщательным надзором для выявления прогресса или рецидива опухолей.
Синдром Прадера − Вилли
Препарат Сайзенâ 8 мг клик.изи не показан для длительного лечения детей, в которых задержка роста предопределена генетически подтвержденным синдромом Прадера − Вилли, если у них также не диагностирован дефицит гормона роста. Существуют сообщения о синдроме ночного апноэ и внезапную смерть после начала лечения гормоном роста детей с синдромом Прадера − Вилли, которые имели один или несколько из таких факторов риска : тяжелая форма ожирения, обструкция верхних дыхательных путей или синдром ночного апноэ в анамнезе и неопределенная инфекция дыхательных путей.
Лейкемия
У небольшого количества пациентов с дефицитом гормона роста, часть из которых лечилась соматропином, была диагностированная лейкемия. Однако нет никаких доказательств того, что лечение соматропином приводит к росту частоты заболевания на лейкемию у пациентов, которые не имеют предиктивних факторов.
Резистентность к инсулину
Поскольку соматропин может снижать чувствительность к инсулину, во время лечения следует обследовать пациентов относительно выявления признаков непереносимости глюкозы. После начала терапии препаратами соматропину пациентам с сахарным диабетом может быть нужная корректировка дозы инсулина. Пациентам с сахарным диабетом или со случаями сахарного диабета в семье, а также пациентам с непереносимостью глюкозы препарат следует назначать с осторожностью.
Ретинопатия
Развитие стабильной фоновой ретинопатии не является основанием для прекращения заместительной терапии с применением соматропину.
Функция щитовидной железы
Во время лечения гормоном роста повышается уровень превращения Т4 в Т3, что может привести к манифестации скрытой субклинической формы гипотиреоза. Таким образом, у всех пациентов следует проводить мониторинг функции щитовидной железы к началу лечения и периодически в дальнейшем. Гипотиреоз, который развился при применении препарата Сайзен® 8 мг клик.изи, нуждается соответствующего лечения. При назначении соматропину пациентам с гипопитуитаризмом(гипоталамо-гипофизарной недостаточностью) проведения стандартной заместительной терапии нужно тщательным образом контролировать.
Доброкачественная внутричерепная гипертензия
Для исключения диагноза отека диска зрительного нерва следует провести офтальмоскопию перед началом лечения препаратом и повторно в случае развития клинических симптомов, таких как тяжелая или периодическая головная боль, нарушение зрения, тошнота та/або блюют, за которыми можно допустить наличие этого расстройства. При подтверждении отека диска зрительного нерва следует учесть возможность диагноза доброкачественной внутричерепной гипертензии(или псевдоопухоли мозга) и при необходимости прекратить лечение препаратом Сайзенâ 8 мг клик.изи. Лечение можно обновить с применением низших доз препарата после исчезновения симптомов доброкачественной внутричерепной гипертензии, которая быстро происходит после прекращения лечения.
Панкреатит
Следует учитывать вероятность развития панкреатита у пациентов, которые применяют соматропин, в частности у детей при появлении абдоминальной боли.
Антитела
Как и в случае применения других препаратов соматропину, у небольшого процента пациентов могут образовываться антитела к соматропину. Зв'язувальна способность этих антител низкая, и они не влияют на скорость роста. При отсутствии ответа на лечение у любого пациента следует провести тестирование на наличие антител к соматропину.
Епіфізеоліз головки бедренной кости
Епіфізеоліз головки бедренной кости часто связан с эндокринными расстройствами, такими как дефицит гормона роста и гипотиреоз, или со стремительным ростом. У детей, которые лечатся гормоном роста, епифизеолиз головки бедренной кости может быть вызван или основными эндокринными расстройствами, или ростом скорости роста благодаря лечению. Стремительный рост может увеличивать риск появления проблем с суставами, поскольку бедренный сустав находится под особенной нагрузкой во время препубертатного периода стремительного роста. Врачи и родители детей, которые лечатся препаратом Сайзенâ 8 мг клик.изи, должны внимательно следить за своевременным выявлением у детей хромоты или жалоб на боль в бедрах и коленях.
Пациенты с задержкой росту, вызванной хронической почечной недостаточностью
Пациентов с задержкой росту, вызванной хронической почечной недостаточностью, следует периодически обследовать относительно выявления признаков прогресса почечной остеодистрофии. У детей с прогрессирующей почечной остеодистрофией может наблюдаться епифизеолиз или аваскулярний некроз головки бедренной кости, хотя еще не выяснено, или связаны эти проблемы с применением гормона роста. В таких случаях к началу терапии следует провести рентгенологическое обследование бедренного сустава.
Детям с хронической почечной недостаточностью препарат назначают лишь в тех случаях, когда к началу лечения почечная функция снижена больше чем на 50 % от нормы. Для подтверждения нарушений роста к началу терапии следует наблюдать за ростом пациента на протяжении года. На протяжении 1 года до начала лечения следует подобрать консервативное лечение почечной недостаточности(контроль ацидоза, гиперпаратиреоза и ограничения в питании), которое в дальнейшем следует проводить во время лечения гормоном роста. Лечение препаратом следует прекратить на время трансплантации почки.
Низкорослые дети, которые родились с ростом, который не отвечает гестационному возраста(НГВ)
Для низкорослых детей, которые родились из НГВ, к началу лечения следует исключить другие медицинские условия и методы лечения, которые могут объяснять существующее нарушение роста.
У пациентов из НГВ рекомендуется измерять натощак уровни инсулина и глюкозы в крови к началу лечения и ежегодно в дальнейшем. У пациентов с повышенным риском развития сахарного диабета(например, заболевание на диабет в семьи, ожирения, повышенный индекс массы тела, тяжелая форма резистентности к инсулину, акантокератодермия) следует проводить тестирование пероральной переносимости глюкозы. Гормон роста не следует назначать при явном сахарном диабете.
У пациентов из НГВ рекомендуется измерять уровень IGF - 1 к началу лечения и в дальнейшем дважды на год. Если при повторных измерениях уровень IGF - 1 превышает +2 SD сравнительно со значениями, которые отвечают возраста и стадии полового дозревания, следует провести регулирование дозы препарата с учетом соотношения IGF- И/ІGFBP - 3.
Опыт лечения пациентов из НГВ, начало которого приближается к наступлению половой зрелости, ограниченный. Поэтому начинать лечение незадолго до наступления половой зрелости не рекомендуется. Опыт лечения пациентов с НГВ и синдромом Сильвера − Рассела ограничен.
Увеличение роста, полученное при лечении соматропином низкорослых детей из НГВ, может быть в некоторой степени потеряно, если лечение было прекращено к достижению пациентом конечного роста.
Задержка жидкости
У взрослых во время заместительной терапии с применением гормона роста следует ожидать развития явлений задержки жидкости.
В случае длительного отека или тяжелой парестезии следует уменьшить дозирование препарата для того, чтобы предупредить развитие синдрома запястного канала.
Пациенты, которые находятся в остром критическом состоянии
При лечении препаратом пациентов, которые находятся в остром критическом состоянии, следует оценить возможные преимущества применения соматропину над потенциальным риском.
Общие рекомендации
Для предотвращения развития липоатрофии каждый раз следует изменять место инъекции.
Дефицит гормона роста у взрослых является пожизненным состоянием, которое нуждается соответствующего лечения, однако опыт лечения пациентов возрастом свыше 60 лет и опыт длительного применения препарата ограничены.
Применение в период беременности или кормления груддю.
Беременность
Клинические данные относительно применения препарата в период беременности отсутствуют. Поэтому препараты соматропину не рекомендуется применять беременным женщинам, а также женщинам репродуктивного возраста, которые не принимают надлежащих мер из контрацепции.
Кормление груддю
Клинических исследований применения соматропину у женщин, которые кормят груддю, не проводилось. Неизвестно, или выделяется соматропин в грудное молоко человека. Поэтому женщинам, которые кормят груддю, препараты соматропину следует назначать с осторожностью.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Препараты соматропину не влияют на способность пациента руководить автомобилем или работать с другими механизмами.
Способ применения и дозы
Препарат Сайзен® 8 мг клик.изи предназначен для многократного использования.
Дозирование препарата следует подбирать индивидуально для каждого пациента, в зависимости от площади поверхности тела или массы тела.
Лечение детей
Препарат Сайзен® 8 мг клик.изи рекомендуется вводить перед сном в таких дозах:
Задержка роста, вызванная недостаточностью секреции эндогенного гормона роста
Подкожно вводят по 0,7 − 1,0 мг/м2 площади поверхности тела на сутки, или по 0,025 − 0,035 мг/кг массы тела на сутки.
Задержка роста у девочек, вызванная дисгенезиею гонад(синдром Тернера)
Подкожно вводят по 1,4 мг/м2 площади поверхности тела на сутки, или по 0,045 − 0,050 мг/кг массы тела на сутки.
Проведение одновременной терапии с применением неандрогенных анаболических стероидов у пациенток с синдромом Тернера может приводить к усилению ответа на введение гормона роста.
Задержка роста у детей препубертатного возраста, вызванная хронической почечной недостаточностью
Подкожно вводят по 1,4 мг/м2 площади поверхности тела на сутки, которые приблизительно представляют 0,045 − 0,050 мг/кг массы тела на сутки.
Нарушение роста у низкорослых детей, которые родились с ростом, который не отвечает гестационному возраста(НГВ)
Рекомендуется ежедневно вводить по 0,035 мг/кг массы тела(или по 1 мг/м2 площади поверхности тела на сутки, которые представляют 0,1 МО/кг/добу, или 3 МО/м2/сутки) подкожно.
Длительность лечения
Лечение следует прекратить при достижении пациентом роста, достаточного для взрослых, или при закрытии эпифизарных зон роста.
Лечение нарушений роста у низкорослых детей, которые родились из НГВ, обычно рекомендуется продолжать к достижению ими конечного роста. Лечение следует прекратить после 1-го года лечения, если SDS скорости роста менее +1. Лечение следует прекратить при достижении пациентом конечного роста(определяется за скоростью роста < 2 см/год). Нужное подтверждение необходимости лечения, если возраст костей отвечает возраста > 14 годы(девушки) или > 16 годы(ребята), что отвечает закрытию эпифизарных зон роста.
Дефицит гормона роста у взрослых
В начале терапии рекомендуется подкожно вводить низкие дозы препарата, которые представляют 0,15 − 0,3 мг соматропину на сутки. Дозу следует постепенно регулировать и контролировать за уровнями IGF - 1. Рекомендованная окончательная доза гормона роста редко превышает 1,0 мг/сутки. В целом следует вводить самые низкие эффективные дозы препарата. Для пациентов пожилого возраста или пациентов с избыточной массой тела может быть необходимым уменьшения доз препарату.
Способ приготовления раствора и введения инъекций
Препарат следует растворять бактериостатическим растворителем, который добавляется к упаковке, используя устройство для растворения "клик.изи".
Разведенный раствор предназначен для подкожного введения; он должен быть прозрачным и не содержать частиц. Если раствор содержит частицы, его нельзя вводить. Разведенный раствор имеет концентрацию 5,83 мг/мл и содержит 8 мг соматропину в целом.
Пациента следует детально проинструктировать относительно проведения процедуры растворения препарата.
Подготовительный этап
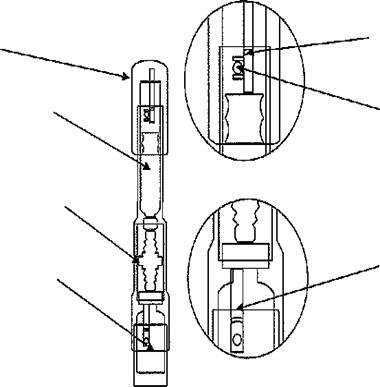
· Убедитесь, что устройство для растворения "клик.изи" имеет полную комплектацию, то есть имеются флакон с препаратом Сайзен® (а), стерильная переходная канюля(b) и картридж с растворителем(с).
· Проверьте, что защитные язычки на корпусе устройства "клик.изи"(d) и на колпачке(е) не повреждены. Если любой из язычков поврежден, препарат нельзя использовать.
· На чистую поверхность положите все предметы, необходимые для приготовления раствора.
· Вымойте руки водой с мылом.
Приготовление и дальнейшее введение раствора для инъекций следует проводить в соответствии с такими инструкциями:
1. Поместите устройство для растворения "клик.изи" вертикально на ровную поверхность таким образом, чтобы флакон находился снизу, а колпачок(g) - сверху.
2. Нажимайте на колпачок движением книзу до тех пор, пока он не прекратит двигаться дальше(примечание: сейчас защитный язычок на корпусе устройства "клик.изи" разрушен).
3. Слегка поверните колпачок по часовой стрелке таким образом, чтобы зеленая отметка(f) была расположена в вертикальном отверстии.
4. Для перенесения растворителя из картриджа в флакон продолжайте очень медленно нажимать на колпачок, пока он не прекратит двигаться дальше(примечание: сейчас защитный язычок на колпачке разрушен). Для предотвращения образования пены в флаконе важно, чтобы нажатие было медленным. Проверьте, или весь растворитель перенесен к флакону.
5. Растворите порошок в растворителе, осторожно вращая устройство "клик.изи"(примечание: избегайте энергичного стряхивания для предотвращения образования пены). Оставьте раствор на некоторое время для полного растворения порошка. Нажимайте на колпачок движением книзу до тех пор, пока он не прекратит двигаться дальше, и оставьте его в этом положении.
|
g. колпачок c. картридж из растворителем b. стерильная переходная канюля a. флакон из препаратом Сайзен® |
|
e. защитный "язычок" f. зеленая отметка d. защитный "язычок" |
6. Переверните устройство "клик.изи" флаконом кверху и медленно оттягивайте колпачок книзу, пока раствора полностью не попадет к картриджа.
7. Проверьте, что в флаконе осталось не больше одной или двух капель раствора. Если в флаконе осталось больше раствор, медленно нажимайте на колпачок, пока некоторой части раствора не попадет обратно к флакону, и осторожно постучите пальцем по устройству "клик.изи". Потом медленно втяните раствор обратно к картриджа.
8. Удалите воздух, который попал к картриджа, медленно нажимая на колпачок(примечание: следует избегать слишком быстрого оттягивания колпачка, поскольку это приведет к попаданию воздуха к картриджа).
9. Удерживая устройство "клик.изи" в этом положении(флакон сверху), отвинтите колпачок и снимите его. Удерживая устройство "клик.изи" в таком же положении(флакон сверху), удалите из устройства "клик.изи" картридж, который содержит разведенный раствор для инъекций.
10. Осторожно снимите внешнюю этикетку с помощью язычка. На прозрачной внутренней этикетке картриджа запишите дату разведения. Осторожно избавьтесь от использованного устройства "клик.изи".
Введения приготовленного раствора проводят с использованием автоматического инжектора Оne.clickтм или Easypodтм или безголкового автоматического инжектора Сool.clickтм в соответствии с инструкцией из использования избранного автоматического инжектора.
Инжектор Easypodтм предназначен для использования в первую очередь детьми, начиная из 7-летнего возраста, и взрослыми. Дети всегда должны использовать инжектор под надзором взрослых.
Деть.
Препарат Сайзен® 8 мг клик.изи применяют в педиатрической практике.
Передозировка
Превышение рекомендованных доз может повлечь развитие побочных эффектов. Передозировка может приводить к развитию гипогликемии с дальнейшей гипергликемией. Кроме того, вероятно, что передозировка соматропину может привести к развитию проявлений задержки жидкости.
Побочные реакции
До 10 % пациентов могут иметь покраснение и зуд в месте инъекции.
При проведении гормонозамисной терапии с применением гормона роста у взрослых ожидается развитие явлений задержки жидкости, которая клинически может проявляться периферическим отеком, отеком суставов, артралгией, миалгией и парестезией. Однако эти симптомы и признаки обычно имеют временный и дозозависимый характер.
При лечении взрослых пациентов с дефицитом гормона роста, в которых этот диагноз был установлен в детстве, сообщается о меньшей частоте развития побочных реакций сравнительно с теми, у кого дефицит гормона роста начался во взрослом возрасте.
У небольшого процента пациентов могут образовываться антитела к соматропину. До этого времени сообщалось о низкой звъязувальну способности таких антител, а их образование не приводило к послаблению роста, за исключением пациентов из делециями генов. В крайне одиночных случаях, когда низкорослость связана с делециею генного комплекса гормона роста, лечения соматропином может индуктировать развитие антител, которые ослабляют процесс роста.
У небольшого количества пациентов с дефицитом гормона роста, часть из которых лечилась соматропином, была диагностированная лейкемия. Однако нет никаких доказательств того, что лечение соматропином приводит к росту частоты заболевания на лейкемию у пациентов, которые не имеют предиктивних факторов.
Побочные реакции, о которых сообщалось в связи с применением препарата и которые перечислены ниже, классифицируются за частотой таким образом: очень распространенные(³ 1/10), распространенные(от ≥ 1/100 к < 1/10), нераспространенные(от ≥ 1/1000 к < 1/100), одиночные(от ≥ 1/10000 к < 1/1000), редкие(< 1/10 000), частота неизвестна(частоту нельзя установить на основании имеющихся данных).
Расстройства со стороны нервной системы
Распространены: головная боль(изолированный), синдром запястного канала(у взрослых).
Нераспространены: идиопатическая внутричерепная гипертензия(доброкачественная внутричерепная гипертензия), синдром запястного канала(у детей).Мышечно-скелетные расстройства и расстройства со стороны соединительной ткани
Редкие: епифизеолиз головки бедренной кости или аваскулярний некроз головки бедренной кости.
Расстройства со стороны иммунной системы
Частота неизвестна: локализованные или генерализуемые реакции гиперчувствительности.
Эндокринные расстройства
Редкие: гипотиреоз.
Расстройства метаболизма и питания
Распространенные(у взрослых) /нераспространены(у детей) : задержка жидкости, которая проявляется как периферический отек, скованность суставов, артралгия, миалгия, парестезия.
Частота неизвестна: резистентность к инсулину, которая может приводить к гиперинсулинемии, в одиночных случаях − к гипергликемии.
Расстройства со стороны репродуктивной системы и молочных желез
Нераспространены: гинекомастия.
Общие расстройства и реакции в месте введения
Распространены: реакции в месте введения; локализована липоатрофия, которую можно предупредить, каждый раз изменяя участок для инъекции.Желудочно-кишечные расстройства
Частота неизвестна: панкреатит.
Несовместимость
Поскольку специальных исследований совместимости не проводилось, препарат нельзя смешивать с другими лекарственными средствами.
Срок пригодности. 3 годы.
Не применять после окончания срока пригодности, отмеченного на упаковке.
Готовый раствор следует хранить при температуре 2 − 8 ºC(в холодильнике) максимально на протяжении 28 дней. Не замораживать.
Условия хранения.
Хранить при температуре не выше 25 ºС в оригинальной упаковке.
Хранить в недоступном для детей месте.
Автоматические инжекторы Оne.clickтм или Easypodтм, которые содержат картридж с разведенным раствором препарата, следует хранить при температуре 2 − 8 ºC(в холодильнике). При использовании безголкового автоматического инжектора Сool.clickтм в холодильнике при температуре 2 − 8 ºC следует хранить лишь картридж с разведенным раствором препарата.
Упаковка
- По 1 флакону с порошком для приготовления раствора для инъекций в комплекте с 1 картриджем из 1,37 мл бактериостатического растворителя для парентерального приложения(0,3 % (г./о.) раствор м-крезола в воде для инъекций), которые предварительно собраны в 1 устройство для растворения(клик.изи), которое состоит из 1 корпуса устройства и 1 стерильной переходной канюли, в картонной коробке.
- По 5 флаконы с порошком для приготовления раствора для инъекций в комплекте с 5 картриджами из 1,37 мл бактериостатического растворителя для парентерального приложения(0,3 % (г./о.) раствор м-крезола в воде для инъекций), которые предварительно собраны в 5 пристроил для растворения(клик.изи), что состоят из 5 корпусов устройства и 5 стерильных переходных канюль, в картонной коробке.
Категория отпуска. За рецептом.
Производитель.
Мерк Сероно С.п.А./Merck Serono S.p.A.
Местонахождение производителя и адрес места осуществления деятельности
Віа делле Магноліє 15(р-н Промышленная Зона), 70026 Модуньо(Баре), Италия/
Via delle Magnolie 15 (loc. frazione Zona Industriale), 70026 Modugno (Bari), Italy.
Другие медикаменты этого же производителя
Форма: порошок и растворитель для раствора для инъекций по 0,25 мг, 1 флакон с порошком в комплекте с 1 предварительно заполненным шприцем с растворителем(вода для инъекций) по 1 мл, 1 иглой для растворения, 1 иглой для инъекций и 2 тампонами, пропитанными спиртом, в контурной ячейковой упаковке; по 7 контурных ячейковых упаковок в картонной коробке
Форма: порошок и растворитель для раствора для инъекций, 1 или 3 флаконы с порошком в комплекте с 1 или 3 флаконами из 1 мл растворителя(вода для инъекций) в контурной ячейковой упаковке; по 1 контурной ячейковой упаковке в коробке; 5 флаконы с порошком в комплекте с 5 флаконами из 1 мл растворителя(вода для инъекций) в контурной ячейковой упаковке; по 2 контурные ячейковые упаковки в коробке
Форма: раствор для инъекций по 12 мг(8,0 мг/мл) по 1,50 мл в картриджах № 1
Форма: гель влагалищный 8 % по 1,45 г(что отвечает дозе для введения 1,125 г) в одиндозовом апликатори, вложенному в многослойную упаковку, по 6 или 15 одиндозовых апликаторив в картонной коробке
Форма: таблетки по 10 мг в алюминиевом блистере № 1, № 4 или № 6 запечатанному в картонную обложку