Клексан®
Регистрационный номер: UA/7181/01/01
Импортёр: ООО "Санофи-Авентис Украина"
Страна: УкраинаАдреса импортёра: Украина, 01033, г. Киев, ул. Жилянская, 48-50А
Форма
раствор для инъекций, 10 000 Анти-Ха МО/1 мл, № 2: по 0,8 мл в шприцевой дозе с защитной системой иглы, по 2 шприцевые дозы в блистере, по 1 блистеру в картонной коробке
Состав
1 мл раствора содержит 10 000 Анти-Ха МО, что эквивалентно 100 мг еноксапарину натрия; 1 шприц-доза содержит 8000 Анти-Ха МО/0,8 мл, что эквивалентно 80 мг еноксапарину натрия
Виробники препарату «Клексан®»
Страна производителя: Франция
Адрес производителя: 180 рю Жан Жорес 94700 МЕЗОН-АЛЬФОР, Франция
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
КЛЕКСАНТ
(CLEXANEТ)
Состав
действующее вещество: еноксапарин;
1 мл раствора содержит 10 000 Анти-Ха МО, что эквивалентно 100 мг еноксапарину натрия;
1 шприц-доза содержит 8000 Анти-Ха МО/0,8 мл, что эквивалентно 80 мг еноксапарину натрия;
вспомогательные вещества: вода для инъекций.
Врачебная форма. Раствор для инъекций.
Основные физико-химические свойства: бесцветный или бледно-желтого цвета, прозрачный раствор.
Фармакотерапевтична группа. Антитромботические средства. Группа гепарина.
Код АТХ В01А В05.
Фармакологические свойства.
Фармакодинамика.
Еноксапарин является низкомолекулярным гепарином, у которого антитромботическая и антикоагулянтная активность стандартного гепарина не связаны между собой. Ему свойственное высшее соотношение Анти-Ха к анти-ИИа(антитромбиновой) активности. Для еноксапарину соотношения этих двух видов активности представляет 3,6.
Как и для стандартного гепарина, Анти-Ха и анти-ИИа активность еноксапарину обусловлена его влиянием на антитромбин.
В профилактических дозах он не делает значительного действия на активированное частичное тромбопластиновий время(АЧТЧ).
На пике активности лечебных доз АЧТЧ может в 1,5 − 2,2 раза превышать контрольное время. Это удлинение указывает на остаточную антитромбинову действую.
Лечение острого инфаркта миокарда с подъемом сегмента ST, в комбинации с тромболитическим средством, у пациентов, в которых проводится дальнейшее перкутанне коронарное вмешательство, а также у пациентов, которым эта процедура не проводится. В большом многоцентровом клиническом исследовании 20479 пациенты с острым инфарктом миокарда с подъемом сегмента ST после того, как они получили фибринолитическую терапию, были рандомизированы распределенные на группы для получения или еноксапарину в виде болюсной внутривенной инъекции 3000 Анти-Ха МО, следом за которой немедленно подкожно вводили дозу 100 Анти-Ха МО/кг, потом проводили подкожные инъекции по 100 Анти-Ха МО/кг каждые 12 часы, или для введения внутривенного нефракционировав гепарина в виде болюсной инъекции 60 МО/кг(максимум 4000 МО) с дальнейшей постоянной инфузией в дозе, которая была откорректирована в зависимости от показателя АЧТЧ. Подкожные инъекции еноксапарину применяли к выписке из стационара или в течение максимум 8 сутки(в 75 % случаи не менее 6 суток). Половине пациентов, которые получали гепарин, препарат вводили не менее 48 часов(в 89,5 % случаи ≥ 36 часы). Все пациенты также получали аспирин в течение не менее 30 суток. Дозу еноксапарину для пациентов возрастом ≥ 75 годы откорректировали: 75 МО/кг в виде подкожной инъекции каждые 12 часы без начальной болюсной внутривенной инъекции.
В ходе исследования в 4716(23 %) пациентов было проведено перкутанне коронарное вмешательство на фоне антитромботической терапии с применением замаскированных исследуемых препаратов. Пациенты не получали дополнительную дозу, если с момента последней подкожной инъекции еноксапарину к раздуванию баллона прошло менее 8 часов, или же получали болюсну внутривенную инъекцию еноксапарину в дозе 30 Анти-Ха МО/кг, если с момента последней подкожной инъекции еноксапарину к раздуванию баллона прошло больше 8 часов.
Еноксапарин дал возможность значительно уменьшить частоту событий первичных конечных точек (комбинированная конечная точка, которая включает у себя рецидив инфаркта миокарда и смерть по любой причине в течение 30 суток после включения в исследование, : 9,9 % в группе еноксапарину сравнительно с 12 % в группе нефракционировав гепарина (снижения относительного риска - 17 % (р<0,001)). Частота рецидива инфаркта миокарда была значительно ниже в группе еноксапарину (3,4 % сравнительно с 5 %, р<0,001, снижение относительного риска - 31 %). Частота летальных случаев была ниже в группе еноксапарину, однако разница между группами не была статистически достоверной (6,9 % сравнительно с 7,5 %, р=3D0,11).
Позитивное влияние еноксапарину на первичную конечную точку было постоянным в подгруппах(возраст, пол, локализация инфаркта миокарда, диабет или инфаркт миокарда в анамнезе, тип назначенного фибринолитического препарата и промежуток времени между появлением первых клинических признаков и началом лечения).
Еноксапарин продемонстрировал значительное преимущество сравнительно с нефракционировав гепарином с точки зрения первичной конечной точки эффективности как у пациентов, которые перенесли коронарную ангиопластику в течение 30 суток после включения в исследование(10,8 % сравнительно с 13,9 %, снижение относительного риска на 23 %), так и у пациентов, которым коронарную ангиопластику не проводили(9,7 % сравнительно с 11,4 %, снижение относительного риска на 15 %).
Частота возникновения больших кровотечений в течение 30 суток была значительно выше в группе еноксапарину(2,1 %) сравнительно с группой гепарина(1,4 %). Частота желудочно-кишечных кровотечений была более высока в группе еноксапарину(0,5 %), чем в группе гепарина(0,1 %), тогда как частота внутричерепных кровоизлияний в обеих группах была одинаковой(0,8 % в группе еноксапарину сравнительно с 0,7% в группе гепарина).
Анализ комбинированных конечных точек, с помощью которых определяли общую клиническую пользу, показал статистически значимое преимущество(р<0,0001) еноксапарину над нефракционировав гепарином: снижение относительного риска на 14 % в пользу еноксапарину(11 % сравнительно с 12,8 %) для комбинированной конечной точки смерть, рецидив инфаркта миокарда или большое кровотечение(критерии ТИМЕ) в течение 30 суток и 17 % (10,1 % сравнительно с 12,2 %) для комбинированной конечной точки смерть, рецидив инфаркта миокарда или внутричерепное кровоизлияние в течение 30 суток.
Через 12 месяцы периода наблюдение определено снижение относительного риска комбинированной конечной точки(повторное возникновение инфаркта миокарда и смерть по любой причине) в пользу еноксапарину на 8%(95% ДІ : 2−14%).
Фармакокинетика.
Фармакокінетичні показатели еноксапарину оценивали на основании длительности Анти-Ха и анти-ИИа активности в плазме крови при рекомендованных дозах(валидовани амидолитические методы) после однократного и повторного подкожного введения и после однократной внутривенной инъекции.
Биодоступность. Еноксапарин, что вводится подкожно, быстро и почти полностью всасывается(приблизительно на 100 %). Максимальная активность в плазме крови наблюдается через 3 − 4 часы после введения. Такая максимальная активность(что выражена в Анти-Ха МО) представляет 0,18±0,04(после введения 2000 Анти-Ха МО), 0,43±0,11(после введения 4000 Анти-Ха МО) при применении профилактических доз и 1,01±0,14(после введения 10000 Анти-Ха МО) при применении лечебной дозы.
Болюсна внутривенная инъекция 3000 Анти-Ха МО с дальнейшими подкожными инъекциями еноксапарину в дозе 100 Анти-Ха МО/кг каждые 12 часы приводит к достижению первого максимального уровня концентрации антифактора Ха, что представляет 1,16 МО/мл(n=3D16), и среднего показателя площади под фармакокинетичной кривой, которая отвечает 88 % стойкой концентрации. Стойкая концентрация достигается на второе время лечения.
В пределах рекомендованных доз фармакокинетика еноксапарину является линейной. Внутрииндивидуальная и межиндивидуальная вариабельнисть низкая. После повторных подкожных введений здоровым добровольцам 4000 Анти-Ха МО 1 раз в сутки стойкая концентрация достигается на 2-й день, при этом средняя активность еноксапарину приблизительно на 15 % выше, чем после одноразовой дозы. Уровень активности еноксапарину в равновесном состоянии можно предусмотреть за фармакокинетикой однократной дозы. После многократного подкожного введения еноксапарину в дозе 100 Анти-Ха МО/кг 2 разы на сутки стойкая концентрация достигается на 3−4-у сутки, средний показатель площади под фармакокинетичной кривой приблизительно на 65 % выше, чем после однократной дозы, а максимальный и минимальный уровни Анти-Ха активности представляют 1,2 и 0,52 Анти-Ха МО/мл соответственно. Учитывая фармакокинетику еноксапарину натрия, эта разница стойкой концентрации является предсказуемой и находится в пределах терапевтического интервала.
Анти-ІІа активность в плазме крови после подкожного введения приблизительно в 10 разы более низкая за Анти-Ха активность. Средняя максимальная анти-ИИа активность наблюдается приблизительно через 3 − 4 часы после подкожной инъекции и достигает 0,13 анти-ИИа МО/мл при повторных введениях дозы 100 Анти-Ха МО/кг два раза на сутки.
Фармакокінетичної взаимодействия между еноксапарином и тромболитическим средством при одновременном приложении не наблюдалось.
Распределение. Объем распределения Анти-Ха активности еноксапарину представляет приблизительно 5 литры и является приближенным к объему крови.
Метаболизм. Еноксапарин метаболизуеться преимущественно в печенке(десульфатизация, деполимеризация).
Выведение. После подкожного введения период полувыведения Анти-Ха активности в низкомолекулярных гепаринив более высок, чем в нефракционировав гепаринив.
Еноксапарину свойственное монофазное выведение с периодом полувыведения приблизительно 4 часы после подкожного введения одноразовой дозы и приблизительно 7 часы после введения повторных доз.
У низкомолекулярного гепарина(НМГ) анти-ИИа активность в плазме крови снижается быстрее, чем Анти-Ха активность.
Еноксапарин и его метаболити выводятся почками(ненасыщаемый механизм) и через желчевыводящие пути.
Почечный клиренс фрагментов, которые имеют Анти-Ха активность, представляет приблизительно 10 % от введенной дозы, а общая почечная экскреция активных и неактивных веществ - 40 % дозы.
Особенные популяции.
Пациенты пожилого возраста. Выведение замедлено через физиологически сниженную функцию почек в этой группе. Это изменение не влияет на дозирование и режим введения при профилактической терапии, если почечная функция у таких больных остается в приемлемых пределах, то есть когда она лишь немного снижена.
Перед началом лечения НМГ у пациентов возрастом свыше 75 лет необходимо систематически оценивать функцию почек за формулой Кокрофта(см. раздел "Особенности применения").
Пациенты с легким или умеренным нарушением функции почек(клиренс креатинина >30 мл/хв).
В определенных случаях может быть полезным мониторинг активности циркулирующего Анти-Ха фактора для предотвращения передозировки, если еноксапарин применяется в лечебных целях(см. раздел "Особенности применения").
Клинические характеристики
Показание
Лечение диагностированного тромбоза глубоких вен, который сопровождается тромбоэмболией легочной артерии или без нее и не имеет тяжелых клинических симптомов, за исключением тромбоэмболии легочной артерии, которая требует лечения тромболитическим средством или хирургического вмешательства.
Лечение нестабильной стенокардии и острого инфаркта миокарда без зубца Q, в комбинации с ацетилсалициловой кислотой.
Лечение острого инфаркта миокарда с подъемом сегмента ST, в комбинации с тромболитическим средством, у пациентов, которым планируется или не планируется проведение перкутанного коронарного вмешательства.
Противопоказание
Повышенная чувствительность к еноксапарину, гепарина или его производных, в том числе других низкомолекулярных гепаринив.
Наличие в анамнезе тяжелой гепарининдукованой тромбоцитопении(ГІТ) типа ІІ, что была вызвана нефракционировав гепарином или низкомолекулярным гепарином(см. раздел "Особенности применения").
Кровотечение или склонность к кровотечению в связи с нарушением гемостазу (возможным исключением из этого противопоказания может быть дисеминоване внутрисосудистое свертывание крови, если оно не связано с лечением гепарином (см. раздел "Особенности применения").
Органическое поражение с вероятностью возникновения кровотечения.
Активное клинически значимое кровотечение.
Внутримозговое кровоизлияние.
Активная язва желудка или двенадцатиперстной кишки.
Из-за отсутствия соответствующих данных препарат не применяют пациентам с тяжелой почечной недостаточностью(клиренс креатинина, рассчитанный за формулой Кокрофта, 30 мл/хв), за исключением пациентов, которые находятся на диализе. Пациентам с тяжелой почечной недостаточностью следует назначать нефракционировав гепарин. Для проведения расчета за формулой Кокрофта необходимо иметь данные последнего измерения массы тела больного(см. раздел "Особенности применения) ".
Спинальную или эпидуральную анестезию не следует ни в коем случае применять пациентам, которые находятся на лечении низкомолекулярными гепаринами(НМГ).
Пациентам, которые получают гепарин для лечения, а не для профилактики, противопоказанная местная анестезия при плановых хирургических вмешательствах.
Не рекомендуется применять этот препарат в таких случаях.
При остром обширном ишемическом инсульте головного мозга с потерей сознания или без. Если инсульт вызван эмболией, в первые 72 часы после инсульта еноксапарин применять нельзя.
На сегодня не определенная эффективность лечебных доз НМГ, независимо от причины, обширности поражения или тяжести клинических проявлений инфаркта головного мозга.
При остром инфекционном эндокардите(кроме некоторых заболеваний сердца, вызванных эмболией).
При почечной недостаточности легкой или умеренной степени тяжести(клиренс креатинина 30-60 мл/хв).
Кроме того, этот препарат в целом не рекомендуется назначать в комбинации с такими средствами(см. раздел "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий") :
1. Ацетилсалициловая кислота в знеболювальних, жаропонижающих и противовоспалительных дозах.
2. Нестероидные противовоспалительные препараты(НПЗП) (системное приложение).
3. Декстран 40(парентеральное приложение).
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Лекарственные средства и терапевтические классы препаратов, которые могут содействовать развитию гиперкалиемии, : соли калия, калийзберигаючи диуретики, ингибиторы ангиотензинперетворюючего фермента, ингибиторы рецепторов ангиотензина ІІ, нестероидные противовоспалительные препараты, гепарини(низкомолекулярный или нефракционировав гепарин), циклоспорин, такролимус и триметоприм.
Развитие гиперкалиемии может зависеть от того, или имеет пациент соответствующие факторы риска. Риск возникновения гиперкалиемии растет, если вышеуказанные лекарственные средства применять одновременно.
Нежелательные комбинации.
С ацетилсалициловой кислотой в знеболювальних, жаропонижающих и противовоспалительных дозах(и по аналогии другие салицилаты). Увеличивается риск кровотечения(подавление функции тромбоцитов и поражения слизистой оболочки желудочно-кишечного тракта под действием салицилатов). Следует применять жаропонижающие, знеболювальни средства, которые не принадлежат к салицилатам(например парацетамол).
С нестероидными противовоспалительными средствами, включая кеторолак(системное приложение). Увеличивается риск кровотечения(подавление функции тромбоцитов и поражения слизистой оболочки желудочно-кишечного тракта под действием НПЗП). Если невозможно избежать одновременного приложения, следует проводить тщательное клиническое наблюдение.
С декстраном 40(парентеральное приложение). Повышенный риск кровотечения(притеснение декстраном 40 функции тромбоцитов).
Комбинации, которые нуждаются принятия мер предосторожностей.
С пероральными антикоагулянтами. Усиление антикоагулянтного эффекта. При замене гепарина пероральным антикоагулянтом следует усилить клинический надзор.
Комбинации, которые следует учитывать.
С ингибиторами агрегации тромбоцитов(кроме ацетилсалициловой кислоты в знеболювальних, жаропонижающих и противовоспалительных дозах), такими как абсиксимаб, ацетилсалициловая кислота в антиагрегантных дозах при кардиологических и неврологических показаниях, берапрост, клопидогрель, ептифибатид, илопрост, тиклопидин, тирофибан. Увеличивается риск кровотечения.
Особенности применения
Препарат не позволяется вводить внутримышечно.
Хотя концентрации разных низкомолекулярных гепаринив определяются в международных единицах(МО) Анти-Ха активности, их эффективность зависит не только от их Анти-Ха активности. Опасно менять один режим дозирования НМГ на другой или один НМГ на другой синтетический полисахарид, поскольку каждый режим было обоснованно специфическими клиническими исследованиями. Следовательно, при применении каждого препарата следует соблюдать особенную осторожность и выполнять специальные инструкции относительно применения.
Меры предосторожностей при применении.
Риск возникновения кровотечения. Необходимо придерживаться рекомендованных режимов дозирования(дозы и длительность лечения). Невыполнение этих рекомендаций может повлечь развитие кровотечения, в частности у пациентов группы риска(пациенты пожилого возраста, пациенты с почечной недостаточностью и др.).
Случаи тяжелых кровотечений были зарегистрированы у пациентов пожилого возраста, в частности через снижение функции нырок, который возникает с возрастом; у пациентов с почечной недостаточностью; у пациентов с массой тела ниже 40 кг; при лечении, длительность которого превысила рекомендованную среднюю длительность 10 дни; при несоблюдении терапевтических рекомендаций(в частности тех, которые касаются длительности лечения и корегування дозы в соответствии с массой тела при лечении); при одновременном приложении с препаратами, которые повышают риск развития кровотечения(см. раздел "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
В любом случае пациенты пожилого возраста та/або пациенты с почечной недостаточностью, а также пациенты, лечение которых длится больше 10 дней, должны находиться под специальным надзором.
В отдельных случаях количественное определение Анти-Ха активности может быть полезным для выявления кумуляции препарата(см. раздел "Особенности применения").
Риск гепарининдукованой тромбоцитопении(ГІТ). Всегда следует допускать возможность развития ГІТ и срочно определять уровень тромбоцитов(см. раздел "Особенности применения") при развитии у пациента, которое получает НМГ(в лечебных или профилактических дозах), таких тромботичних осложнений, как:
- обострение тромбоза, лечение которого проводится;
- флебит;
- легочный емболизм;
- острая ишемия нижних конечностей;
- инфаркт миокарда или ишемический инсульт.
Механические протезы клапанов сердца. Применение еноксапарину для профилактики тромбоэмболических осложнений у пациентов с механическими протезами клапанов сердца отдельно не изучалось. Однако несколько отдельных случаев тромбоза были зарегистрированы у пациентов с механическими протезами клапанов сердца, которые получали еноксапарин для профилактики тромбоэмболических осложнений.
Беременность. В ходе клинического исследования при участии беременных женщин с механическими протезами клапанов сердца, которые получали еноксапарин в дозе 100 Анти-Ха МО/кг два раза на сутки для уменьшения риску тромбоэмболических осложнений, в двух из восьми беременных розвився тромбоз, который повлек обструкцию клапана, которая привела к гибели женщины и плода. Отдельные случаи тромбоза механического клапану сердца у беременных женщин, которые получали еноксапарин для профилактики тромбоэмболических осложнений, были также зарегистрированы во время писляреестрацийного надзора. Следовательно, у таких пациентов риск тромбоэмболических осложнений повышен.
Предостережение при применении.
Кровотечение. Как и при применении всех других антикоагулянтов, возможное кровотечение(см. раздел "Побочные реакции"). При развитии кровотечения следует определить ее причину и назначить соответствующее лечение.
Функция почек. Прежде чем начать лечение низкомолекулярным гепарином, следует оценить состояние функции почек, в частности у пациентов в возрасте от 75 лет, путем определения клиренса креатинина(КК) за формулой Кокрофта, используя данные последнего измерения массы тела :
- для пациентов мужского пола : КК =3D(140-вик) * масса тела / (0,814 * креатинин в сыворотке), где возраст выраженно в годах, масса - в килограммах, а креатинин в сыворотке - в мкмоль/л;
- для женщин эту формулу корегують путем умножения результата на 0,85.
Если сывороточный креатинин выраженно в мг/мл, показатель следует умножить на коэффициент 8,8.
Применение НМГ в лечебных дозах пациентам с диагностированной тяжелой почечной недостаточностью(клиренс креатинина около 30 мл/хв) противопоказанное(см. раздел "Противопоказания").
Пациенты с ожирением. Пациенты с ожирением имеют повышенный риск возникновения тромбоэмболии. Безопасность и эффективность профилактических доз для пациентов с ожирением(индекс массы тела > 30 кг/м2) не были полностью определены и нет рекомендаций относительно коррекции дозы для этих пациентов. Эти пациенты должны находиться под тщательным надзором относительно возникновения симптомов тромбоэмболии.
Лабораторные показатели.
Контроль уровня тромбоцитов у пациентов, которые применяют НМГ и имеют риск гепарининдукованой тромбоцитопении(например ГІТ ІІ типа).
НМГ могут повлечь развитие ГІТ II типу - серьезной имуноопосередкованой тромбоцитопении, которая может привести к артериальным или венозным тромбоэмболическим событиям, которые могут быть опасными для жизни или ухудшать функциональный прогноз для пациентов(см. раздел "Побочные реакции"). Для своевременного выявления ГІТ за пациентами необходимо осуществлять соответствующее наблюдение.
Пациенты, которые перенесли оперативное вмешательство или недавно получили травму(в течение 3 месяцев). Независимо от того, назначается препарат с целью лечения или профилактики, у всех пациентов необходимо систематически проводить лабораторное исследование, поскольку частота ГІТ представляет > 0,1 % или даже > 1 % в хирургии и травматологии. Это исследование должно включать определение количества тромбоцитов :
- перед назначением лечения НМГ или не позже, чем в течение 24 часов после начала терапии препаратом;
- потом дважды на неделю в течение 1 месяца(период повышенного риска);
- потом 1 раз в неделю к прекращению лечения в случае длительного лечения.
Пациенты с другими состояниями, отличающимися от оперативного вмешательства или недавней травмы(в течение 3 месяцев). Независимо от того, назначается препарат с целью лечения или профилактики, необходимо систематическое выполнение лабораторных исследований согласно тем же принципам, которые применяются в хирургии и травматологии(см. выше), у пациентов:
- которые раньше получали нефракционировав гепарин(НФГ) или НМГ в последние 6 месяцы, учитывая, что частота ГІТ представляет > 0,1% или даже > 1 %;
- которые имеют значимые сопутствующие заболевания, учитывая потенциальную тяжесть ГІТ у таких пациентов.
В иных случаях, учитывая низшую частоту развития ГІТ(< 0,1 %) мониторинг количества тромбоцитов может быть ограничен такими мероприятиями:
- одноразовый контроль количества тромбоцитов в начале лечения или не позже, чем через 24 часы после начала лечения;
- контроль количества тромбоцитов при наличии клинических симптомов, которые указывают на ГІТ(любой новый эпизод артериальной та/або венозной тромбоэмболии, любое болезненное поражение кожи в месте инъекции, любые аллергические или анафилактические реакции на фоне лечения). Пациентов необходимо поинформировать о возможности возникновения таких симптомов и о необходимости сообщать о них врачу.
Следует допустить возникновение ГІТ, если количество тромбоцитов менее 150 000/мм3(или 1509/л) та/або если наблюдается относительное уменьшение количеству тромбоцитов на 30 − 50 % сравнительно с количеством тромбоцитов перед началом лечения. ГІТ развивается преимущественно через 5 − 21 день после начала лечения гепарином(с максимальной частотой развития через приблизительно 10 сутки). Однако у пациентов из ГІТ в анамнезе это осложнение может возникнуть значительно раньше. Также сообщалось об отдельных случаях развития ГІТ после 21-го дня лечения. В связи с этим следует прилагать систематические усилия для выявления пациентов с таким анамнезом путем детального опроса перед началом лечения. Во всех случаях возникновения ГІТ является неотложным состоянием и требует консультации со специалистом. Любое значительное уменьшение количеству тромбоцитов(на 30 − 50 % в сравнении с исходным уровнем) является предупредительным сигналом, даже если показатели не достигли критического уровня. Если наблюдается снижение количества тромбоцитов, то во всех случаях необходимо принять такие меры:
1. Немедленно определить количество тромбоцитов для подтверждения полученных результатов.
2. Отменить терапию гепарином, если этот анализ подтверждает значительное снижение количества тромбоцитов и если другой очевидной причины этого не выявлено. Для проведения in vitro теста на агрегацию тромбоцитов и иммунологического исследования образец необходимо поместить в пробирку с цитратным раствором. Однако при таких условиях немедленные мероприятия, которых необходимо употребить, не должны основываться на результатах in vitro теста на агрегацию тромбоцитов или иммунологического исследования, поскольку существует лишь несколько специализированных лабораторий, которые могут проводить такие тесты в привычном порядке, а их результаты можно получить, в наилучшем разе, лишь через несколько часов. Однако такие исследования являются необходимыми, потому что они могут помочь диагностировать это осложнение, поскольку риск возникновения тромбоза при продолжении лечения гепарином в таких случаях является очень высоким.
3. Проводить профилактику или лечение тромботичних осложнений, связанных с ГІТ. Если продолжение антикоагулянтной терапии является очень важным, гепарин следует заменить антитромботическим средством, которое принадлежит к другой группе препаратов, например данапароидом натрию или лепирудином, который назначают в лечебных или профилактических дозах индивидуально для каждого пациента. Замену пероральными антикоагулянтами можно проводить только после того, как количество тромбоцитов вернется к норме, поскольку существует риск обострения тромбоза при применении пероральных антикоагулянтов.
Замена гепарина пероральными антикоагулянтами. Следует усилить клинический надзор и повысить частоту выполнения лабораторных анализов(протромбиновий время, которое выражено как международное нормализованное соотношение(МЧС)) для контроля за эффектом пероральных антикоагулянтов.
В связи с существованием промежутка времени для достижения максимального эффекта перорального антикоагулянту, лечение гепарином в постоянной дозе нужно продолжать в течение времени, необходимого для поддержания МЧС в пределах желательного терапевтического диапазона при определении в двух последовательных анализах.
Мониторинг Анти-Ха активности. Поскольку большинство клинических исследований, которые продемонстрировали эффективность НМГ, были проведены с применением дозы, рассчитанной в соответствии с массой тела пациента, и без специального мониторинга лабораторных показателей, значения лабораторного контроля для оценки эффективности лечения НМГ не установлено. Однако в определенных клинических ситуациях, которые часто сопровождаются риском передозировки, лабораторные анализы, а именно мониторинг Анти-Ха активности, может быть полезным для контроля риска возникновения кровотечения.
Эти ситуации преимущественно касаются лечебных показаний к применению НМГ и связаны с дозами, которые назначают пациентам, :
- с легким и умеренным нарушением функции почек(клиренс креатинина 30 − 60 мл/хв за формулой Кокрофта). Поскольку в отличие от стандартного нефракционировав гепарина НМГ выводится преимущественно почками, любая почечная недостаточность может стать причиной возникновения относительной передозировки. Тяжелая почечная недостаточность является противопоказанием к применению НМГ в лечебных дозах(см. раздел "Противопоказания");
- с излишне большой или излишне низкой массой тела(похудение или даже кахексия, ожирение);
- с кровотечением незъясованой этиологии.
В отличие от этого, проведение лабораторного мониторинга не рекомендуется в случае применения профилактических доз, если НМГ применяется в соответствии с терапевтическими рекомендациями(в частности относительно длительности лечения), а также во время гемодиализа.
Для выявления возможной кумуляции гепарина после многократного введения рекомендуется при необходимости брать кровь на анализ на пике активности(согласно имеющимся данным), то есть через приблизительно 4 часы после третьей инъекции, если препарат вводится подкожно 2 разы на сутки.
Необходимость проведения повторных анализов Анти-Ха активности для определения уровня гепарина в крови, например, через каждые 2 − 3 сутки, решается в индивидуальном порядке в зависимости от результатов предыдущего анализа. Также может быть необходимо откорректировать дозу НМГ.
Определенно, что Анти-Ха активность изменяется в зависимости от НМГ и режима дозирования.
Среднее значение(± стандартное отклонение), которое наблюдалось через 4 часы после седьмой инъекции еноксапарину в дозе 100 Анти-Ха МО/кг/ін'єкцію 2 разы на сутки, представляло 1,20±0,17 Анти-Ха МО/мл.
Это среднее значение показателя наблюдалось во время клинических исследований, в которых определяли Анти-Ха активность хромогенным(амидолитическим) методом.
Контроль активированного частичного тромбопластинового времени(АЧТЧ). Некоторые НМГ вызывают умеренное повышение АЧТЧ. Поскольку клиническое значение этого эффекта не выяснено, нет необходимости использовать этот тест для мониторинга лечения.
Спинальная/эпидуральная анестезия у больных, которые получают профилактическое лечение НМГ. Никогда нельзя проводить эпидуральную или спинальную анестезию пациентам, которые получают терапию НМГ в лечебных дозах.
Как и в случае применения других антикоагулянтов, при применении НМГ во время проведения спинальной/эпидуральной анестезии сообщалось о редких случаях спинальных гематом, которые вызывали длительный или постоянный паралич.
Риск развития спинальной гематомы более высок в случае эпидуральной анестезии с применением катетера, чем в случае спинальной анестезии.
Риск возникновения таких редких случаев может расти при длительном использовании эпидуральных катетеров в послеоперационный период или в случае наличия в прошлом хирургических втручаннь на хребте или при деформации хребта(например анкилозирующий спондилоартрит).
Установление или удаление катетера лучше всего осуществлять тогда, когда антикоагулянтный эффект еноксапарину является низким. Однако точное время достижения достаточно низкий антикоагулянтный эффект для каждого отдельного пациента индивидуальный.
Если предоперационное застомування НМГ является необходимым(пациенты, которые долгое время прикованы к кровати, травма) и если польза от местной спинальной анестезии или люмбальной пункции была тщательным образом взвешена, пациентам, которые получили перед операцией инъекцию НМГ, можно проводить такую анестезию при условии, что между инъекцией гепарина и спинальной анестезией прошло не менее 12 часов. Однако, поскольку анти- Xa активность может храниться и после этого 12-часового интервала, все еще может возникнуть нейроаксиальная гематома. У пациентов с клиренсом креатинина < 30 мл/хв следует выдерживать по крайней мере 24 часы между инъекцией гепарина и спинальной анестезией.
Рекомендуется тщательный мониторинг неврологического состояния пациента через риск возникновения спинальной гематомы.
Почти у всех пациентов через 6 − 8 часы после анестезии или после удаления катетера можно начинать профилактическую терапию НМГ при проведении неврологического наблюдения.
Следует быть особенно осторожными при применении препарата одновременно с другими лекарственными средствами, которые влияют на гемостаз(особенно нестероидными противовоспалительными средствами, аспирином).
Состояния, которые сопровождаются особенным риском. Наблюдение за ходом лечения следует усилить в таких случаях:
- печеночная недостаточность;
- наличие в анамнезе желудочно-кишечных язв или других органических поражений, которые предопределяют кровотечения;
- сосудистое хориоретинальное заболевание;
- послеоперационный период после хирургического вмешательства на головном или спинном мозге;
- люмбальна пункция: следует учитывать риск интраспинальной кровотечения и, если возможно, откладывать ее проведение на якнайдовший время;
- одновременное приложение с лекарственными средствами, которые влияют на гемостаз(см. раздел "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
Перкутанні процедуры реваскуляризации коронарных артерий. Для минимизации риска развития кровотечения у пациентов, которым проводится перкутанне коронарное вмешательство(ПКВ) при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q или острого инфаркта миокарда с подъемом сегмента ST, следует точно придерживаться рекомендованных интервалов между введением доз еноксапарину. Важное значение имеет достижение гемостазу в месте пункции после проведения ПКВ. В случае применения специальных средств для закрытия сосуда(гемостатических устройств) следует немедленно удалить проводник. В случае ручной компрессии проводник необходимо удалить через 6 часы после последнего подкожного/внутривенного введения еноксапарину. При продолжении лечения с применением еноксапарину следующую инъекцию следует делать не раньше чем через 6 − 8 часы после удаления проводника. Необходимо наблюдать по месту пункции при ПКВ для выявления любых признаков кровотечения или гематомы.
Применение в период беременности или кормления груддю
Беременность. В исследованиях на животных не было выявлено никаких доказательств тератогенного влияния еноксапарину, потому не ожидается этого эффекта у человека.
Соответствующих клинических данных недостаточно для оценки возможных тератогенных или фетотоксичних эффектов еноксапарину при его введении в лечебных дозах в период беременности.
Поэтому, в порядке меры пресечения, еноксапарин в лечебных дозах преимущественно не следует назначать в период беременности.
В любом случае нельзя проводить спинальную или эпидуральную анестезию у пациентов, которые получают терапию НМГ в лечебных дозах.
Кормление груддю. Поскольку гастроинтестинальна абсорбция у новорожденных является маловероятной, женщинам, которые кормят груддю, лечение еноксапарином не противопоказано.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Прием препарата не влияет на способность руководить автотранспортным средством и работать с другими механизмами. Однако следует быть осторожными учитывая возможные побочные реакции(см. раздел "Побочные реакции").
Способ применения и дозы
Путь введения - подкожный(за исключением пациентов с инфарктом миокарда из елевациею сегмента ST, которым необходимо внутривенное болюсне введение).
Рекомендованный для применения взрослым.
Препарат нельзя вводить внутримышечно.
1 мл раствора для инъекций эквивалентный приблизительно 10000 Анти-Ха МО еноксапарину.
Техника подкожного введения.
Дозу еноксапарину следует откорректировать в зависимости от массы тела пациента. Перед проведением инъекции необходимо удалить лишний объем препарата. Если лишнего объема нет, то перед проведением инъекции не нужно удалять волдырьки воздуха из шприца.
Подкожное введение еноксапарину следует проводить преимущественно в положении пациента, лежа на спине. Места введения препарата следует дежурить, проводя инъекции то в левую, то в праву переднелатеральну или заднелатеральну участок брюшной стенки.
Иглу следует вводить на всю длину в складку кожи, собранную между большим и указательным пальцем, перпендикулярно к поверхности кожи. Эту складку кожи следует удерживать пальцами на протяжении всей инъекции.
Общие рекомендации.
На протяжении всего периода лечения следует регулярно контролировать количество тромбоцитов, поскольку существует риск возникновения гепарининдукованой тромбоцитопении(ГІТ) (см. раздел "Особенности применения").
Лечение диагностированного тромбоза глубоких вен(ТГВ), который сопровождается или не сопровождается тромбоэмболией легочной артерии, при отсутствии тяжелых клинических симптомов.
При подозрении на тромбоз глубоких вен следует провести соответствующее обследование для подтверждения диагноза.
Схема введения. Вводить 2 инъекции на сутки с интервалом в 12 часы.
Доза на 1 инъекцию представляет 100 Анти-Ха МО/кг.
Дозирование НМГ с учетом массы тела для пациентов с массой тела больше 100 кг или менее 40 кг не изучало. У пациентов с массой тела больше 100 кг эффективность терапии НМГ может быть несколько ниже, а у пациентов с массой тела менее 40 кг возможен повышенный риск кровотечения. Такие пациенты должны находиться под особенным клиническим наблюдением.
Длительность лечения ТГВ. При применении НМГ следует как можно раньше переходить на терапию пероральными антикоагулянтами, если не существует противопоказаний для этого. Длительность лечения НМГ не должна превышать 10 сутки, включая время, необходимое для достижения надлежащего терапевтического эффекта перорального антикоагулянту, за исключением случаев, когда этого эффекта трудно достичь(см. раздел "Особенности применения"). Следовательно, лечение пероральными антикоагулянтами следует начинать как можно раньше.
Лечение нестабильной стенокардии и острого инфаркта миокарда без зубца Q. Еноксапарин назначают в дозе 100 Анти-Ха МО/кг, которую вводят подкожно 2 разы на сутки через каждые 12 часы, в комбинации с ацетилсалициловой кислотой(рекомендованная доза − 75 − 325 мг внутренне после минимальной погрузочной дозы 160 мг).
Рекомендованная длительность лечения представляет 2 − 8 сутки, к достижению стабилизации клинического состояния.
Лечение острого инфаркта миокарда с подъемом сегмента ST, в комбинации с тромболитическим средством, у пациентов, в которых планируется или не планируется проведение перкутанного коронарного вмешательства.
Начальную внутривенную болюсну инъекцию вводят в дозе 3000 Анти-Ха МО. Следом за ней подкожно вводят 100 Анти-Ха МО/кг в течение 15 минут, потом каждые 12 часы(для первых двух подкожных инъекций максимальная суммарная доза представляет 10000 Анти-Ха МО).
Первую дозу еноксапарину следует вводить за 15 минуты до или через 30 минуты после начала тромболитической терапии(фибриноспецифичной или нет).
Рекомендованная длительность лечения представляет 8 дни или пока пациента не выпишут из стационара, если госпитализация длится менее 8 дней.
Сопутствующая терапия: после появления симптомов следует как быстрее всего начинать прием ацетилсалициловой кислоты и продолжать в дозе 75 − 325 мг на сутки в течение не менее 30 дней, если не показано другое.
Пациенты, которым проводится перкутанне коронарное вмешательство, :
- если со времени последнего подкожного введения еноксапарину к раздуванию баллона прошло менее 8 часов, дополнительное введение еноксапарину не нужно;
- если со времени последнего подкожного введения еноксапарину к раздуванию баллона прошло больше 8 часов, необходимо провести внутривенную болюсну инъекцию еноксапарину в дозе 30 Анти-Ха МО/кг. Для обеспечения точности объемов инъекции рекомендуется развести препарат до 300 МО/мл(то есть 0,3 мл еноксапарину, разведенного в 10 мл) (см. таблицу 1).
Таблица 1.
Объемы, необходимые для инъекционного введения, когда разведение препарата осуществляется для пациентов, которым проводится перкутанне коронарное вмешательство, :
|
Масса ( кг) |
Необходимая доза ( МО) |
Объем, необходимый для инъекционного введения, при разведении до 300 МО/мл(то есть 0,3 мл еноксапарину разведены в 10 мл) ( мл) |
|
45 |
1350 |
4,5 |
|
50 |
1500 |
5 |
|
55 |
1650 |
5,5 |
|
60 |
1800 |
6 |
|
65 |
1950 |
6,5 |
|
70 |
2100 |
7 |
|
75 |
2250 |
7,5 |
|
80 |
2400 |
8 |
|
85 |
2550 |
8,5 |
|
90 |
2700 |
9 |
|
95 |
2850 |
9,5 |
|
100 |
3000 |
10 |
Пациентам в возрасте от 75 лет, которые находятся на лечении по поводу острого инфаркта миокарда с подъемом сегмента ST, начальную внутривенную болюсну инъекцию еноксапарину не проводят. Каждые 12 часы им следует подкожно вводить еноксапарин в дозе 75 Анти-Ха МО/кг(только для первых двух инъекций максимальная суммарная доза представляет 7500 Анти-Ха МО).
Инструкции относительно самостоятельного ведения препарата Клексан® в шприцевой дозе с защитной системой иглы
Для предотвращения случайного укола иглой после инъекции шприцы оснащены автоматической защитной системой иглы.
1. Вымыть руки и участок, в который будет выполняться инъекция препарата, водой с мылом. Высушить их.
2. Удостовериться в том, что хорошо видно место, в которое следует вводить препарат.
3. Избрать участок в правой или левой части живота. Этот участок должен быть удален(по направлению к сторонам) от пупка по меньшей мере на 5 сантиметры.
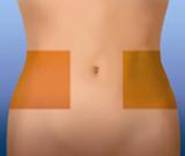
4. Изменять место инъекции, выполняя ее попеременно в праву и левую стороны живота, в зависимости от того, в какую сторону была сделана инъекция в прошлый раз. Очистить место инъекции тампоном со спиртом.
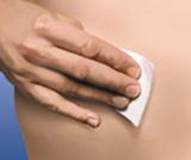
5. Осторожно снять колпачок из иглы, присоединенной к шприцу с препаратом Клексан®. Выбросить этот колпачок. Шприц является предварительно наполненным и готовым к использованию. НЕ нажимать на поршень к выполнению инъекции, чтобы избавиться от пузырьков воздуха. Это может привести к потере лекарственного средства. После того, как снят колпачок, не допускать, чтобы игла касалась почему-либо. Это необходимо для сохранения стерильности иглы.

6. Держать шприц в руке так, как карандаш при письме, и другой рукой зажать очищенную область живота между указательным и большим пальцами, чтобы образовалась складка кожи. Обязательно удерживать кожную складку в течение всей инъекции.
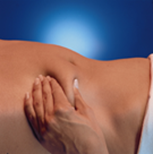
7. Держать шприц таким образом, чтобы игла была направлена книзу(вертикально под углом 90°). Ввести иглу в кожную складку на всю длину.
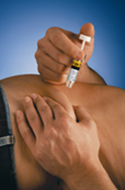
8. Нажать на поршень шприца большим пальцем. Обязательно удерживать кожную складку в течение всей инъекции.
9. Вытянуть иглу прямо в обратном направлении и отпустить складку кожи. Направить иглу вниз и в сторону от себя и других, а потом нажать на поршень, чтобы активировать защитную систему. При этом игла автоматически укроется защитным чехлом. Сразу же выбросить шприц в ближайший контейнер для острых предметов.
Примечание: защитная система, которая приводит к образованию защитного чехла, может быть активирована лишь после опорожнения шприца нажатием поршня до конца.
Для избежания образования кровоподтека не растирать место инъекции после введения препарата.
Деть. Из-за отсутствия соответствующих данных не рекомендуется применять НМГ в педиатрической практике.
Передозировка.
Случайную передозировку при подкожном введении массивных доз НМГ может привести к геморрагическим осложнениям.
В случае кровотечения для лечения некоторых пациентов можно применять протамину сульфат, учитывая такие факторы:
- эффективность протамина сульфата намного ниже, чем эффективность, зарегистрированная при передозировке нефракционировав гепарина;
- через возможность возникновения побочных эффектов(в частности анафилактический шок) следует тщательным образом взвесить соотношение риск/польза перед применением протамина сульфата.
Нейтрализацию еноксапарину осуществляют путем медленного внутривенного введения протамина(сульфату или гидрохлориду).
Необходимая доза протамина зависит:
- от введенной дозы гепарина(100 протигепаринових единиц протамина нейтрализуют активность 100 Анти-Ха МО НМГ), если с момента введения еноксапарину натрия прошло не больше 8 часов;
- от времени, которое прошло с момента введения гепарина, :
- если с момента введения еноксапарину натрия прошло больше 8 часов или если нужна вторая доза протамина, можно вводить инфузию 50 протигепаринових единиц протамина на 100 Анти-Ха МО еноксапарину натрию;
- если с момента инъекции еноксапарину натрия прошло больше 12 часов, нет необходимости вводить протамин.
Эти рекомендации касаются пациентов с нормальной функцией почек, которые получают повторные дозы.
Однако полностью нейтрализовать Анти-Ха активность невозможно.
Кроме того, нейтрализация может иметь временный характер в результате особенностей фармакокинетики всасывания НМГ, в результате чего может возникнуть необходимость распределить общую рассчитанную дозу протамина на несколько инъекций(2 − 4), которые вводятся в течение 24 часов.
После попадания НМГ в желудок, даже в больших количествах, тяжелые осложнения являются маловероятными(таких случаев зарегистрировано не было) в результате незначительного всасывания лекарственного средства в желудке и кишечнике.
Побочные реакции
Побочные реакции, которые наблюдались в клинических исследованиях и о которых сообщалось в постмаркетинговый период, детально описаны ниже.
За частотой возникновения побочные реакции распределены на такие категории: очень часто(≥1/10); часто(от ≥1/100 к <1/10); нечасто(от ≥1/1000 к <1/100); редко(от ≥1/10000 к <1/1000); очень редко(<1/10000), частота неизвестна(невозможно оценить по имеющимся данным).
Опыт применения в клинических исследованиях. В рамках клинических исследований еноксапарин применяли больше чем 15 000 пациентам.
Количество пациентов, показания и схемы дозирования детально представлено в таблице 2.
Таблица 2.
|
Показание |
Профилактика венозных тромбоембо-лій у хирургических пациентов |
Профилактика тромбоза глубоких вен у терапевтических пациентов во время острого заболевания |
Лечение тромбоза глубоких вен с эмболией легочной артерии или без нее |
Лечение нестабильной стенокардии или инфаркта миокарда без зубца Q |
Лечение инфаркта миокарда из елевациею сегмента ST |
|
Количество пациентов, которые получали еноксапарин |
1776 |
1169 |
559 |
1578 |
10 176 |
|
Схема дозирования |
40 мг подкожно один раз на сутки |
40 мг подкожно один раз на сутки |
1 мг/кг подкожно каждые 12 часы или 1,5 мг/кг подкожно один раз на сутки |
1 мг/кг подкожно каждые 12 часы |
30 мг внутренне-венозный болюсно, после чего по 1 мг/кг подкожно каждые 12 часы |
Кровотечения. В клинических исследованиях кровотечению были побочными реакциями, о которых сообщалось наиболее часто. К ним принадлежат и серьезные кровотечения, о которых сообщалось в 4,2 % пациентов(хирургического профиля). Некоторые из этих случаев были летальными.
Геморрагические осложнения расценивались как серьезные в таких случаях:
- если кровотечение повлекло значимое клиническое событие;
- если кровотечение сопровождалось снижением уровня гемоглобина на ≥ 2 г/дл или трансфузиею 2 или больше единицы препаратов крови;
- ретроперитонеальные и внутричерепные кровоизлияния всегда расценивались как серьезные.
Как и в случае применения других антикоагулянтов, кровотечение может возникать при наличии сопутствующих факторов риска, таких как:
- органические поражения со склонностью к кровотечению
- инвазивные процедуры или одновременное применение лекарственных средств, которые влияют на гемостаз(см. разделы "Особенности применения" и "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
Таблица 3.
|
Система-орган-класс за класифика-циею MedDRA |
Профілак-тика тромбоза глубоких вен у хирургических пациентов |
Профилактика тромбоза глубоких вен у терапевтических пациентов |
Консервативное лечение тромбоза глубоких вен с эмболией легочной артерии или без нее |
Нестабильная стенокардия / инфаркт миокарда без елевации сегмента ST |
Инфаркт миокарда из елевациею сегмента ST |
|
Расстройства со стороны сосудов |
Очень часто: геморрагические явления* Редко: ретропери-тонеальний кровоизлияние |
Часто: геморрагические явления* |
Очень часто: геморрагические явления* Нечасто: внутренне-черепное кровоизлияние, ретроперито-неальний кровоизлияние |
Часто: геморрагические явления* Редко: ретроперито-неальний кровоизлияние |
Часто: геморрагические явления* Нечасто: внутриш-нечерепний кровоизлияние, ретропери-тонеальний кровоизлияние |
* Например: гематома, экхимоз(не в месте инъекции), гематома раны, гематурия, носовое кровотечение и желудочно-кишечное кровотечение.
Тромбоцитопения и тромбоцитоз.
Таблица 4.
|
Система-орган-класс за класифика-циею MedDRA |
Профилактика тромбоза глубоких вен у хирургических пациентов |
Профилактика тромбоза глубоких вен у терапевтических пациентов |
Консервативное лечение тромбоза глубоких вен с эмболией легочной артерии или без нее |
Нестабильная стенокардия / инфаркт миокарда без елевации сегмента ST |
Инфаркт миокарда из елевациею сегмента ST |
|
Расстройства со стороны крови и лимфатической системы |
Очень часто: тромбоцитоз* Часто: тромбоцито-пения |
Нечасто: тромбоцито-пения |
Очень часто: тромбоцитоз* Часто: тромбоцито-пения |
Нечасто: тромбоцито-пения |
Часто: тромбоцитоз*, тромбо-цитопенія Очень редко: имуноалергична тромбо-цитопенія |
* Количество тромбоцитов > 400 Г/л
Другие нежелательные реакции, которые наблюдались в клинических исследованиях, представлены ниже независимо от показания к применению препарата и классифицированы за категориями "Система-орган-класс", за частотой возникновения и в порядке уменьшения их серьезности.
|
Система-орган-класс за классификацией MedDRA |
Нежелательные эффекты(при применении препарата при всех показаниях) |
|
Расстройства со стороны иммунной системы |
Часто: аллергическая реакция, которая в некоторых случаях может привести к прекращению лечения препаратом Редко: анафилактическая или анафилактоидна реакция |
|
Расстройства со стороны печенки и желчевыводящих путей |
Очень часто: повышение уровней печеночных ферментов(главным образом уровней трансаминаз больше чем в 3 разы от верхнего предела нормы) |
|
Расстройства со стороны кожи и подкожной клетчатки |
Часто: крапивница, зуд, эритема Нечасто: буллезный дерматит |
|
Общие расстройства и реакции в месте введения препарата |
Часто: гематома в месте инъекции*, боль в месте инъекции, другая реакция в месте инъекции(например отек, кровоизлияние, аллергическая реакция, воспаление, образование узелков, другие реакции) Нечасто: некроз кожи в месте инъекции, которая может развиться после появления пурпури или инфильтрованих и болезненных эритематозных пятен, что требует немедленного прекращения лечения препаратом; местное раздражение |
|
Изменения при лабораторных и инструментальных исследованиях |
Редко: гиперкалиемия |
* Риск повышается в случае несоблюдения рекомендованной техники осуществления инъекции или использования несоответственно инъекционного материала.
Опыт применения в постмаркетинговый период.
Побочные реакции, что приведено ниже, были выявлены в пострегистрационный период. Поскольку об этих реакциях сообщалось добровольно, их частота оценивается как "неизвестна"(не может быть оценена по имеющимся данным).
Расстройства со стороны иммунной системы. Кожные или системные аллергические эффекты(анафилактические или анафилактоидни реакции, в том числе шок), которые в отдельных случаях могут приводить к отмене препарата.
Расстройства со стороны нервной системы. Головная боль.
Расстройства со стороны сосудов. Были зарегистрированные случаи значительных геморрагических осложнений, некоторые из них были летальными. Нечастыми побочными реакциями были внутричерепные и ретроперитонеальные кровоизлияния. Также регистрировались случаи геморрагических осложнений(кровотечения), таких как гематома, экхимоз в местах, отличающихся от места инъекции, гематома раны, гематурия, носовое кровотечение и желудочно-кишечное кровотечение. Они главным образом связаны:
- с сопутствующими факторами риска : наличие органических поражений, которые имеют склонность к кровотечению, определенные комбинации лекарственных средств(см. раздел "Противопоказания" и "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий"), век, недостаточность функции почек, низкая масса тела.
- с несоблюдением терапевтических рекомендаций, в частности таких, которые касаются длительности лечения и коррекции дозы в соответствии с массой тела(см. раздел "Особенности применения").
Зарегистрированы одиночные случаи спинальной гематомы после введения НМГ во время спинальной анестезии, аналгезии или эпидуральной анестезии. Эти гематомы вызывали неврологические повреждения разной степени тяжести, в том числе длительный и постоянный паралич(см. раздел "Особенности применения").
После подкожной инъекции возможное образование гематомы в месте введения препарата. Были зарегистрированные случаи боли в месте инъекции, других реакций, включая раздражение, отек в месте инъекции, гиперчувствительность, воспаление и образование узелков. Этот риск повышается при несоблюдении рекомендованной техники проведения инъекций и при использовании несоответственно инъекционного материала. В результате зажигательной реакции могут возникнуть узелки в месте инъекции, которые исчезают в течение нескольких дней. Их появление не нуждается прекращения лечения.
Сообщалось о возникновении тромбоцитопении. Существует два ее типа.
Тип И − наиболее распространенные случаи, обычно умеренной степени тяжести(больше 100000/мм3), появляются на ранних этапах(до 5 дня) и не нуждаются прекращения лечения.
Тип ІІ − редкие случаи тяжелой имуноалергичной тромбоцитопении(ГІТ). Частота возникновения исследована недостаточно(см. раздел "Особенности применения").
Возможно бессимптомное и оборотное повышение уровня тромбоцитов.
Геморрагическая анемия.
При применении гепаринив были зарегистрированы одиночные случаи некроза кожи, преимущественно в месте инъекции. Им может предшествовать появление пурпури или инфильтрованих и болезненных эритематозных пятен. В таких случаях следует немедленно прекратить терапию.
Возникали нечастые проявления системных аллергических реакций(анафилактические/анафилактоидни реакции, включая шок) или реакций со стороны кожи(крапивница, зуд, эритема, буллезные высыпания), которые в определенных случаях могли приводить к прекращению лечения. Как и при применении нефракционировав гепаринив, не исключенная возможность развития остеопороза при удлинении длительности лечения.
Нефракционировав гепарини могут вызывать гипоальдостеронизм, который приводит к увеличению плазменных уровней калия. Редко может возникнуть клинически значимая гиперкалиемия, особенно у пациентов с хронической почечной недостаточностью и сахарным диабетом.
Сообщалось о случаях транзиторного повышения уровней трансаминаз, гепатоцеллюлярного или холестатического поражения печенки.
Зарегистрировано несколько случаев гиперкалиемии.
Сообщалось о возникновении головной боли, аллопеции.
Очень редко регистрировались случаи васкулита в результате повышения чувствительности кожи.
Достаточно редко возникала гиперэозинофилия, как самостоятельно, так и на фоне кожных реакций, которая исчезала после прекращения лечения.
Срок пригодности. 3 годы.
Условия хранения. Хранить в недоступном для детей месте. Хранить при температуре не выше 25 °C. Не замораживать.
Упаковка. № 2: по 0,8 мл в шприцевой дозе с защитной системой иглы, по 2 шприцевые дозы в блистере, по 1 блистеру в картонной коробке.
Категория отпуска. За рецептом.
Производитель. САНОФІ ВІНТРОП ІНДАСТРІА.
Местонахождение производителя и его адрес места осуществления деятельности.
180 рю Жан Жорес 94700 МЕЗОН-АЛЬФОР, Франция.
или
1051 бульвар Ендустрієль 76580 ЛЬО ТРЕТ, Франция.
Заявитель. ООО "Санофі-Авентіс Украина".
Другие медикаменты этого же производителя
Форма: таблетки, покрытые оболочкой, по 100 мг № 30(10х3), № 30(15х2), № 60(10х6), № 60(15х4), № 90(10х9), № 90(15х6) : по 10 таблетки в блистере; по 3, 6 или по 9 блистеры в картонной коробке; по 15 таблетки в блистере; по 2, 4 или по 6 блистеры в картонной коробке
Форма: таблетки по 200 мг; № 30(10х3) : по 10 таблетки в блистере; по 3 блистеры в картонной коробке; № 30(15х2) : по 15 таблетки в блистере; по 2 блистеры в картонной коробке
Форма: суппозитории влагалищные по 500 мг, № 10(5х2) : по 5 суппозитории в стрипи; по 2 стрипи в картонной коробке
Форма: таблетки по 16 мг/10 мг по 14 таблетки в блистере; по 2 или 6 блистеры в картонной коробке
Форма: таблетки, покрытые пленочной оболочкой, по 75 мг № 14(14х1) : по 14 таблетки в блистере; по 1 блистеру в картонной коробке, № 30(30х1), № 90(30х3) : по 30 таблетки в блистере; по 1 или по 3 блистеры в картонной коробке