Зомактон
Регистрационный номер: UA/10477/01/01
Импортёр: Ферринг ГмбХ
Страна: ГерманияАдреса импортёра: Витланд 11, Постфаш 21 45, Д- 24109 Киль, Германия
Форма
порошок для раствора для инъекций по 10 мг, 1 флакон с порошком в комплекте с 1 предварительно заполненным шприцем по 1 мл растворителя(м-крезол, вода для инъекций), адаптером в картонной упаковке
Состав
1 флакон содержит соматропину 10 мг
Виробники препарату «Зомактон»
Страна производителя: Германия
Адрес производителя: Витланд 11, Постфаш 21 45, Д- 24109 Киль, Германия
Страна производителя: Германия
Адрес производителя: Гердерштрассе 2 и Молкерай-Бауер-Штрассе 18, Д- 83512 Вассербург, Германия
Страна производителя: Швейцария
Адрес производителя: Чемин где ла Вергогнаусаз 50, 1162, Сан-Пре, Швейцария
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
ЗОМАКТОН
(Zomacton)
Состав
действующее вещество: соматропин;
1 флакон содержит соматропину 10 мг;
вспомогательные вещества:
1 флакон с порошком содержит маннит(E 421); натрию гидрофосфат, додекагидрат; натрию дигидрофосфат, дигидрат;
1 шприц с растворителем содержит м-крезол, воду для инъекций.
Врачебная форма. Порошок для раствора для инъекций.
Основные физико-химические свойства: белый или почти белый лиофилизированный порошок;
растворитель - прозрачный бесцветный раствор.
Фармакотерапевтична группа. Соматропін и агонисты соматропину.
Код ATХ H01A C01.
Фармакологические свойства.
Фармакодинамика.
Соматропін - идентичный гипофизарному гормону роста человека за аминокислотной последовательностью длиной 191 аминокислотный остаток и фармакокинетичним профилем. Можно считать, что Зомактон вызывает те же фармакологические эффекты, что и эндогенный гормон.
Гормон роста способствует общему пропорциональному росту костей скелета у человека.
После введения экзогенного препарата Зомактон у детей с подтвержденным дефицитом гипофизарного гормона роста наблюдается линейный рост. Зафиксированное увеличение длины тела после применения Зомактону было вызвано влиянием на эпифизарные пластины длинных костей. У детей с недостаточной выработкой гипофизарного гормона роста Зомактон увеличивает темп роста и повышает концентрацию ІGF - 1 инсулиноподобного фактора роста/соматомедину- C, как и при терапии гипофизарним гормоном роста. Отмечалось также повышение уровня щелочной фосфатазы в крови.
В ответ на применение гормона роста аналогично общему росту и увеличению массы тела, отмечается пропорциональное увеличение размеров других тканей. К этим изменениям принадлежат: повышенный рост соединительной ткани, кожи и отростков; увеличение скелетной мускулатуры с ростом размеров и количества клеток; увеличение тимусу; увеличение печенки с повышенной пролиферацией клеток; незначительное увеличение гонад, и щитовидной надпочечника. На фоне заместительной терапии гормоном роста не отмечалось ни диспропорционального роста кожи и плоских костей, ни ускоренного полового дозревания.
Гормон роста усиливает эффект задержки азота и активизирует транспорт аминокислот в ткани. Оба процесса усиливают синтез белка. Гормон роста подавляет метаболизм углеводов и образования жира. В больших дозах, при отсутствии инсулина, гормон роста действует как диабетогенное средство, вызывая эффекты, которые наблюдаются обычно при голодании(нарушение толерантности к углеводам, торможение липогенеза, мобилизация жира и кетоз).
После лечения гормоном роста отмечается накопление натрия, калия и фосфора.
Повышенное выведение кальция почками компенсируется повышенным всасываниям последнего в кишечнике. Сывороточная концентрация кальция у пациентов, которые получают Зомактон, существенно не отличается от такой у пациентов, которые получали гипофизарний гормон роста. Повышенная концентрация неорганического фосфата в сыворотке крови наблюдалась у пациентов, которые получают как Зомактон, так и гипофизарний гормон роста. Накопление этих солей свидетельствует о повышенной потребности в период роста тканей.
Фармакокинетика.
24 здоровым взрослым добровольцам было введено 1,67 мг соматропину, подкожно или с помощью безголкового инъектора ZomaJet Vision. Пиковые уровни в плазме представляли приблизительно 20 нг/мл и наблюдались в течение 3,5-4 часов после введения лекарственного средства.
При введении смеси с помощью безголкового инъектора ZomaJet Vision конечный период полувыведения представлял 2,6 часы.
Даны относительно других средств, которые содержат соматропин, указывают на то, что биодоступность соматропину, введенного подкожно, представляет приблизительно 80 % у здоровых взрослых; печенка и почки являются важными органами, которые катаболизируют белок, с помощью которых выводится смесь.
Данные доклинических исследований безопасности.
Доклинические данные не содержат ни одной информации относительно особенных опасностей для человека на основании результатов стандартных исследований токсичности многократных доз и генотоксичности.
Генно-инженерный соматропин является идентичным к эндогенному гипофизарного гормону роста человека. Он имеет те же биологические свойства и обычно вводится в физиологичных дозах. Поэтому исследования фармакологической безопасности, репродуктивной токсичности и канцерогенности не проводились, поскольку подобных эффектов не ожидается.
Клинические характеристики
Показание
Зомактон применяется для:
- длительной терапии детей с задержкой росту, связанной с недостаточной секрецией гормона роста;
- длительной терапии задержки роста, связанной с синдромом Тернера, подтвержденного хромосомным анализом.
Противопоказание
Гиперчувствительность к соматропину или любых других составляющих препарата.
Зомактон не следует применять детям, в которых уже закрылись эпифизы костей.
Не следует применять соматропин пациентам с признаками активного опухолевого процесса. Противоопухолевую терапию нужно завершить к началу терапии гормоном роста, признака внутричерепного опухолевого роста должны быть отсутствуют. При признаках опухолевого роста лечения следует прекратить.
Не следует назначать Зомактон пациентам в критических состояниях, с осложнениями после открытых кардиохирургических вмешательств, абдоминальных вмешательств, политравм, при острой дыхательной недостаточности и других подобных состояниях.
Лечение соматропином детей с хронической болезнью почек нужно прекратить при трансплантации почек.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Терапия глюкокортикоидами может ингибувати стимуляцию роста Зомактоном. Пациенты с сопутствующей недостаточностью АКТГ должны получать тщательным образом подобранную заместительную дозу глюкокортикоидов с тем, во избежание любого пригничувального эффекту на гормон роста.
Высокие дозы андрогенов, естрогенив или анаболических стероидов могут ускорить дозревание костей и тем же уменьшить прирост длины тела.
Поскольку соматропин может индуктировать инсулинорезистентность, дозу инсулина, возможно, придется отрегулировать для больных сахарным диабетом.
Даны, полученные в результате изучения врачебных взаимодействий у взрослых пациентов с дефицитом гормона роста, указывают на то, что введение соматропину может значительно повысить клиренс веществ, которые поддаются метаболизму в системе цитохрома P450 3A4(таких как половые гормоны, кортикостероиды, противосудорожные средства и циклоспорин), приводя к снижению концентраций этих веществ в плазме крови. Клиническое значение этого взаимодействия неизвестно.
Особенности применения
Не следует превышать максимальную рекомендованную суточную дозу(см. раздел "Способ применения и дозы").
Очень редко наблюдался миозит, что, возможно, обусловленно содержимым в составе препарата метакрезола как консерванту. В случае миалгии или боли в месте введения следует подозревать миозит, а в случае подтверждения - использовать врачебную форму Зомактону без метакрезола.
Зомактон не предназначен для длительной терапии детей с задержкой росту, предопределенной синдромом Прадера-Віллі, подтвержденным генетически, если его не сопровождает диагноз недостаточности гормона роста. Есть сообщение о сонном апноэ и внезапную смерть, связанную с применением гормона роста в педиатрической практике у пациентов с синдромом Прадера-Віллі, которые имели один или несколько из таких факторов риска : высокая степень ожирения, обструкция верхних дыхательных путей в анамнезе, сонное апноэ или невыявленная дыхательная инфекция.
Известные отдельные случаи доброкачественной внутричерепной гипертензии. В случае сильной или повторной головной боли, нарушение зрения, тошноты/блюющего рекомендовано обследовать глазное дно с целью выявления отека сосочка зрительного нерва. В случае подтверждения отека сосочка зрительного нерва нужно исследовать наличие доброкачественной внутричерепной гипертензии, а при подтверждении этого диагноза - прервать терапию соматропином. Теперь отсутствует достаточное количество подтверждений, которыми можно руководить при принятии клинических решений относительно пациентов с устраненной внутричерепной гипертензией. При повторном начале терапии гормоном роста необходимо тщательным образом отслеживать симптомы внутричерепной гипертензии.
У некоторых пациентов с дефицитом гормона роста, которые принимают соматропин, а также у больных, которые не лечились этим препаратом, может наблюдаться лейкемия. Однако нет подтверждений повышенной частоты лейкемии у пациентов, которые получают гормон роста при отсутствии благоприятных факторов.
Как и в случае применения всех других средств, которые содержат соматропин, у незначительного процента пациентов возможная выработка антител к соматропину. Связывающая способность этих антител незначительна и не влияет на скорость роста. У любого пациента, который не отвечает на терапию, следует провести анализ на наличие антител.
Гормон роста повышает экстратиреоидную конверсию T4 в T3, что может выявить начальную стадию гипотиреоза. Поэтому у всех пациентов целесообразная оценка функции щитовидной железы. У пациентов с гипотиреозом следует осуществлять тщательный мониторинг стандартной заместительной терапии при применении терапии соматропином.
Следует обнаруживать у пациентов наличие нарушения толерантности к глюкозе, поскольку гормон роста может индуктировать состояние инсулинорезистентности. Может возникнуть необходимость пересмотреть дозу инсулина больным сахарным диабетом после начала терапии соматропином. Состояние пациентов с диабетом или нарушением толерантности к глюкозе следует тщательным образом контролировать в течение терапии соматропином. Зомактон также следует применять с осторожностью пациентам с известной семейной склонностью к этой болезни.
У пациентов с дефицитом гормона роста, предопределенным внутричерепными повреждениями, целесообразно проводить мониторинг состояния предыдущего заболевания, его прогресса или регресса. Сообщалось о повышенном риске повторного новообразования у пациентов, которые в детстве перенесли рак, в случае терапии соматропином после первого новообразования. Внутричерепные опухоли, в частности менингиомы, у пациентов, которые получали радиотерапию председателя для лечения первого новообразования, является самыми частыми среди повторных новообразований.
В случае прогресса или рецедиву повреждения терапию Зомактоном следует прекратить. Особенное внимание следует уделять симптомам рецидива у пациентов с предыдущими злокачественными заболеваниями.
При ускоренном росте у любого ребенка возможный прогресс сколиоза. Следует контролировать появление признаков сколиоза во время применения соматропину.
У пациентов с эндокринными нарушениями возможен епифизеолиз головки бедра. Врач должен осмотреть пациентов, которые лечатся Зомактоном и в которых развилась хромота или боль в бедре или колене.
Влияние терапии гормоном роста на выздоровление изучалось в двух плацебо-контролируемых исследованиях при участии 522 тяжелобольных взрослых пациентов с осложнениями после открытых операций на сердце, хирургии брюшной полости, множественных случайных травм или же острой дыхательной недостаточности.
Уровень смертности был выше(42 % сравнительно с 19 %) у пациентов, которые лечились гормонами роста(дозы от 5,3 до 8 мг на сутки), сравнительно с пациентами, которые получали плацебо. Исходя из этой информации, таким пациентам не следует проводить терапию гормонами роста. Поскольку отсутствующая информация о заместительной терапии гормоном роста тяжелобольных пациентов, преимущества продолжения лечения в этой ситуации следует сравнить с потенциальными рисками.
Местное раздражающее действие при введении Зомактону 10 мг/мл с помощью безголкового инъектора ZomaJet Vision X изучалась в ходе 12-недельного исследования при участии детей исключительно европеоидной расы.
Невзирая на редкость подобных случаев, следует рассмотреть возможность панкреатита у пациентов, которые получают терапию соматропином, особенно у детей с болью в животе.
Зомактон содержит натрий, однако менее чем 1 ммоль(23 мг) натрию на дозу.
Применение в период беременности или кормления груддю.
Даны о влиянии Зомактону отсутствуют.
Даны о применении соматропину животным в течение беременности отсутствуют.
Зомактон не рекомендованный беременным и женщинам репродуктивного возраста, которые не применяют средств контрацепции.
Клинические исследования с применением средств, которые содержат соматропин, при участии женщин, которые кормят груддю, не проводились. Неизвестно, или выделяется соматропин с грудным молоком.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Зомактон не влияет на способность руководить автотранспортом или работать с другими механизмами.
Способ применения и дозы
Терапию Зомактоном нужно проводить под надзором квалифицированного врача, который имеет опыт лечения пациентов с дефицитом гормона роста.
Дозу и режим введения Зомактону следует подбирать индивидуально для каждого пациента.
Обычно длительность лечения представляет несколько лет и зависит от достигнутого терапевтического эффекта.
Подкожное введение гормона роста может привести к атрофии или разрастанию подкожно-жировой клетчатки в месте введения. В связи с этим следует изменять места инъекций.
Дефицит гормона роста.
Обычно рекомендуется общую дозу 0,17-0,23 мг/кг массы тела(в перечислении - 4,9 мг/м2-6, 9 мг/м2 площади поверхности тела) на неделю распределять на 6-7 подкожные инъекции(соответственно суточная доза 0,02-0,03 мг/кг массы тела, или 0,7-1 мг/м2 поверхности тела). Не следует превышать общую недельную дозу 0,27 мг/кг, или 8 мг/м2 поверхности тела(в соответствии с суточной дозой до 0,04 мг/кг).
Синдром Тернера.
Обычно рекомендованную дозу 0,33 мг/кг массы тела(приблизительно 9,86 мг/м2 поверхности тела) на неделю распределяют на 6-7 подкожные инъекции(соответственно суточная доза - 0,05 мг/кг массы тела, или 1,40-1,63 мг/м2 поверхности тела).
Растворение.
Порошок следует растворять только в растворителе, который добавляется.
Раствор с концентрацией 10 мг/мл готовится путем смешивания Зомактону из 1 мл растворителя, который находится в предварительно заполненном шприце, как описано ниже.


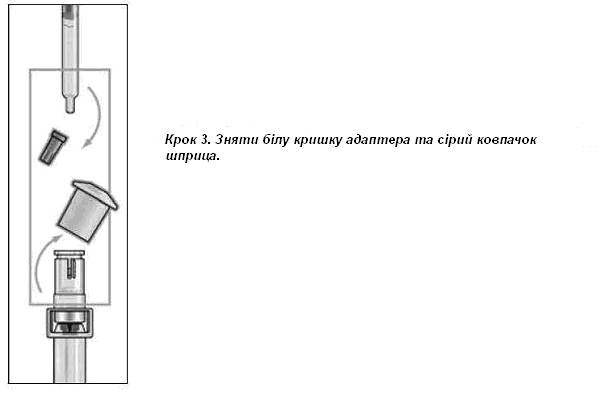


Инструкция для применения безголкового инъектора ZOMAJET VISION X добавляется в брошюре вместе с прибором.
Деть.
Применяют детям(см. раздел "Способ применения и дозы").
Передозировка
Не следует превышать рекомендованную дозу Зомактону.
Невзирая на отсутствие данных о передозировке Зомактону, острой передозировке может повлечь начальную гипогликемию, за которой наступает гипергликемия.
Последствия долговременной передозировки неизвестны. Однако, возможно, оно может повлечь симптомы, подобные тем, которые наблюдаются при чрезмерной продукции человеческого гормона роста(например акромегалию).
Побочные реакции
Подкожное введение гормона роста может привести к атрофии или разрастанию подкожно-жировой клетчатки, а также точечным кровоизлияниям и образованию кровоподтеков в месте введения. В отдельных случаях у пациентов появляется боль или свербляча эритема в месте инъекции.
Побочные реакции распределены за частотой таким образом: очень частые(≥ 1/10), частые(от ≥ 1/100 к < 1/10), нечастые(от ≥ 1/1000 к < 1/100), одиночные(от ≥ 1/10000 к < 1/1000), редкие(< 1/10000).
Нарушение со стороны системы крови и лимфатической системы : нечастые - анемия.
Нарушение со стороны сердечно-сосудистой системы: нечастые - тахикардия, артериальная гипертензия(у взрослых); одиночные - артериальная гипертензия(у детей).
Нарушение со стороны органов слуха и вестибулярного аппарата : нечастые - головокружение.
Нарушение со стороны эндокринной системы: частые - гипотиреоз.
Нарушение со стороны органов зрения : нечастые - отек диска зрительного нерва, диплопия.
Нарушение со стороны желудочно-кишечного тракта: нечастые - блюет, боль в животе, метеоризм, тошнота; одиночные - диарея.
Общие нарушения и нарушения в месте введения : очень частые - отек(у взрослых), периферический отек(у взрослых); частые - отек(у детей), периферический отек(у детей), реакции в месте введения, астения; нечастые - слабость, атрофия в месте инъекции, кровоизлияние в месте инъекции, образования в месте инъекции, гипертрофия.
Нарушение со стороны иммунной системы: частые - выработка антител.
Нарушение со стороны лабораторных показателей: одиночные - патология функции почек.
Нарушение со стороны обмена веществ и питания : очень частые - легкая гипергликемия(у взрослых); частые - нарушение толерантности к глюкозе(у детей); нечастые - гипогликемия, гиперфосфатемия; одиночные - сахарный диабет II типа.
Нарушение со стороны скелетно-мышечной и соединительной ткани: очень частые - артралгия(у взрослых), миалгия(у взрослых); частые - артралгия(у детей); миалгия(у детей), скованность конечностей(у взрослых); нечастые - атрофия мышц, боль в костях, синдром запъясткового канала, скованность конечностей(у детей).
Новообразования доброкачественны, злокачественны и неопределенны: нечастые - злокачественные новообразования, новообразования; редкие - лейкемия(у детей).
Нарушение со стороны нервной системы: очень частые - головная боль(у взрослых), парестезия(у взрослых); частые - головная боль, гипертония, бессонница(у взрослых); нечастые - сонливость, нистагм; одиночные - невропатия, повышение внутричерепного давления, бессонницы(у детей), парестезия(у детей).
Нарушение со стороны психики: нечастые - расстройства личности.
Нарушение со стороны почек и сечевидильной системы : нечастые - недержание мочи, гематурия, полиурия, нарушение частоты мочеиспускания, аномалия мочи.
Нарушение со стороны половых органов и молочных желез : нечастые - генитальные выделения, гинекомастия(у взрослых); редкие - гинекомастия(у детей).
Нарушение со стороны кожи и подкожных тканей : нечастые - липодистрофия, атрофия кожи, ексфолиативний дерматит, крапивница, гирсутизм, гипертрофия кожи.
Сообщалось о панкреатите при пострегистрационном приложении в терапии гормоном роста(частота неизвестна).
Соматропін у 1 % случая способствует выработке антител. Связывающая способность этих антител незначительна и клинического значения не имеет.
Очень редко у детей с дефицитом гормона роста, которые лечатся соматропином, развивалась лейкемия, но частота ее возникновения была очень низкой.
У детей, которые лечились гормоном роста, сообщалось о епифизеолиз головках бедра и болезни Легга-Кальве-Пертеса. Епіфеоліз головки бедра чаще случается в случае нарушений со стороны эндокринной системы, а болезнь Легга-Кальве-Пертеса встречается чаще при низком росте. Однако неизвестно, или случаются эти две патологии чаще при лечении соматропином. На эти диагнозы должны указывать дискомфорт, боль в бедре та/або колене.
Другие побочные реакции могут считаться характерными для соматропину, в частности гипергликемия через снижение чувствительности к инсулину, снижение уровня свободного тироксина и возможное развитие доброкачественной внутричерепной гипертензии.
Нельзя исключить риск возникновения реакции повышенной чувствительности.
Срок пригодности. 3 годы.
Препарат после разведения может храниться в вертикальном положении в холодильнике при температуре 2-8 °C не больше 28 дней.
Условия хранения.
Хранить в холодильнике при температуре 2-8 °C в оригинальной упаковке. Хранить в недоступном для детей месте.
Несовместимость
Учитывая отсутствие данных относительно совместимости препаратов, это лекарственное средство не следует смешивать с другими препаратами.
Упаковка
1 флакон с порошком в комплекте с 1 предварительно заполненным шприцем по 1 мл растворителя, адаптером в картонной упаковке.
Категория отпуска. За рецептом.
Производитель.
Феррінг ГмбХ, Германия/Ferring GmbH, Germany.
Местонахождение производителя и адрес места осуществления его деятельности
Вітланд 11, Постфаш 21 45, Д- 24109 Киль, Германия/Wittland 11, Postfach 21 45, D - 24109 Kiel, Germany.
Другие медикаменты этого же производителя
Форма: порошок для орального раствора по 2 саше с порошком в комплекте с мерной ложкой в картонной упаковке
Форма: порошок для раствора для инъекций по 10 мг, 1 флакон с порошком в комплекте с 1 предварительно заполненным шприцем по 1 мл растворителя(м-крезол, вода для инъекций), адаптером в картонной упаковке
Форма: раствор для инъекций, 7,5 мг/мл, по 0,9 мл в флаконе, по 1 флакону в картонной коробке
Форма: порошок лиофилизированный для приготовления раствора для инъекций по 75 МО, 10 флаконы с порошком в комплекте с 10 ампулами с растворителем(раствор натрия хлорида 0,9 %) по 1 мл в 2 ячейковых упаковках; по 2 ячейковые упаковки в коробке
Форма: порошок лиофилизированный для приготовления раствора для инъекций по 75 МО ФСГ и 75 МО ЛГ в флаконах, по 10 флаконы с порошком и по 10 ампулы с растворителем(0,9 % раствор натрия хлорида, кислота хлористоводородная разведена, вода для инъекций) по 1 мл в упаковке