Гонал-Ф®
Регистрационный номер: UA/4113/01/03
Импортёр: Арес Трейдинг С.А.
Страна: ШвейцарияАдреса импортёра: Зон Индустриель де Л'Урьетаз, 1170 Обонн, Швейцария
Форма
порошок для раствора для инъекций по 75 МО(5,5 мкг); № 1: 1 флакон с порошком в комплекте с растворителем(вода для инъекций) по 1 мл в предварительно заполненном шприце, 1 иглой для растворения и 1 иглой для введения в контурной ячейковой упаковке; по 1 контурной ячейковой упаковке в картонной коробке; № 10: 5 флаконы с порошком в комплекте с растворителем(вода для инъекций) по 1 мл в 5 предварительно заполненных шприцах, 5 иглами для растворения и 5 иглами для введения в контурной ячейковой упаковке, по 2 контурные ячейковые упаковки в картонной коробке
Состав
1 флакон с порошком содержит 75 МО фолитропину альфа(рекомбинантного человеческого фоликулостимулюючего гормона - р-лФСГ), что эквивалентно 5,5 мкг
Виробники препарату «Гонал-Ф®»
Страна производителя: Швейцария
Адрес производителя: Зон Индустриєль де Л'Урьєтаз, СН- 1170 Обонн, Швейцария
Страна производителя: Италия
Адрес производителя: Виа делле Магнолиє 15(р-н Промышленная Зона), 70026 Модуньо(Баре), Италия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
ГОНАЛ- фâ
(GONAL-fâ)
Состав
действующее вещество: фолитропин альфа;
1 флакон с порошком содержит 75 МО фолитропину альфа(рекомбинантного человеческого фоликулостимулюючего гормона - р-лФСГ), что эквивалентно 5,5 мкг;
вспомогательные вещества: сахароза, натрию гидрофосфат дигидрат, натрию дигидрофосфат моногидрат, метионин, полисорбат 20, кислота фосфорная концентрированная, натрию гидроксид;
растворитель: 1 предварительно заполненный шприц с растворителем содержит 1 мл воды для инъекций.
Врачебная форма. Порошок и растворитель для раствора для инъекций.
Основные физико-химические свойства: препарат − белый лиофилизат в виде пелети; растворитель - прозрачная бесцветная жидкость. Значение рН разведенного раствора препарата представляет 6,5 − 7,5.
Фармакотерапевтична группа. Гонадотропіни. Код ATХ G03G A05.
Фармакологические свойства.
Фармакодинамика.
ГОНАЛ- фâ − это препарат фоликулостимулюючего гормона(ФСГ), полученного с помощью методов генной инженерии из клеток яичника китайского хомяка. У женщин важнейшим эффектом парентерального введения ФСГ является развитие зрелых граафових фолликулов.
В клинических исследованиях пациентки с тяжелой недостаточностью ФСГ и лютеинизирующего гормона(ЛГ) определялись за сывороточным уровнем эндогенного ЛГ < 1,2 МО/л, однако следует принять во внимание, что уровень ЛГ, измеренный в разных лабораториях, может отличаться.
В сравнительных клинических исследованиях при проведении вспомогательных репродуктивных технологий(ДРТ) и индукции овуляции ГОНАЛ-ф® оказался эффективнее, чем мочевой ФСГ, что выражалось в низшей общей дозе и более коротком периоде лечения, необходимых для индукции фолликулярного дозревания. При проведении ДРТ применения низших доз ГОНАЛУ-ф® на протяжении более короткого периода лечения дало возможность получить большее количество ооцита и эмбрионов, которые поделились на 2-й день оплодотворения, в сравнении с мочевым ФСГ. При индукции овуляции применения ГОНАЛУ-ф® дало возможность достичь меньшей частоты отмены циклов вследствие неэффективности терапии в сравнении с мочевым ФСГ.
Результаты исследования GF 8407 − рандомизированного исследования с дизайном параллельных групп, в котором сравнивались эффективность и безопасность применения ГОНАЛУ-ф® и мочевого ФГС в рамках ДРТ
|
ГОНАЛ-ф® |
Мочевой ФСГ |
|
|
Количество полученного ооцита |
11,0 ± 5,9 |
8,8 ± 4,8 |
|
Длительность стимуляции(дней) |
11,7 ± 1,9 |
14,5 ± 3,3 |
|
Общая необходимая доза ФСГ(количество ампул по 75 МО ФСГ) |
27,6 ± 10,2 |
40,7 ± 13,6 |
|
Необходимость увеличения дозы(%) |
56,2 |
85,3 |
По всем перечисленным критериям разница между двумя группами была статистически значимой(p < 0,05).
Совместимое применение ГОНАЛУ- фâ и человеческого хорионичного гонадотропина(лХГ) в течение по меньшей мере 4 месяцев приводит к индуктированию сперматогенеза у мужчин с недостаточностью ФСГ.
Фармакокинетика.
После внутривенного введения фолитропин альфа распределяется к межклеточной жидкости с начальным периодом полувыведения, которое представляет почти 2 часы, и выводится из организма с конечным периодом полувыведения, которое представляет приблизительно сутки. Равновесный объем распределения и общий клиренс представляют 10 л и 0,6 л/час соответственно. Одна восьмая дозы фолитропину альфа выводится с мочой.
После подкожного введения абсолютная биодоступность фолитропину альфа представляет приблизительно 70 %. Многократное введение приводит к увеличению его кумуляции втрое с достижением равновесного состояния на протяжении 3 − 4 дней. Было показано, что у женщин с подавленной эндогенной секрецией гонадотропинив фолитропин альфа эффективно стимулирует развитие фолликулов и стероидогенез, невзирая на низкие уровни ЛГ, которые находятся вне предела измерения.
Клинические характеристики.
Показание
Лечение взрослых женщин
· Ановуляция(включая синдром поликистозних яичников) у женщин, которые оказались нечувствительными к лечению кломифену цитратом.
· Стимуляция развития множественных фолликулов у пациенток при проведении суперовуляции в рамках вспомогательных репродуктивных технологий(ДРТ), таких как оплодотворение in vitro(IVF), перенесение гамети к фаллопиевой трубе(GIFT) и перенесению зиготи к фаллопиевой трубе(ZIFT).
· Стимуляция развития фолликулов у женщин с тяжелой недостаточностью лютеинизирующего гормона(ЛГ) и фоликулостимулюючего гормона(ФСГ) (в комбинации с препаратом ЛГ).
Лечение взрослых мужчин
· Стимуляция сперматогенеза у мужчин с урожденным или приобретенным гипогонадотропним гипогонадизмом, одновременно с терапией человеческим хорионичним гонадотропином(лХГ).
Противопоказание
· Гиперчувствительность к действующему веществу или к любым вспомогательным веществам препарата;
· опухоли гипоталамуса или гипофиза;
· увеличения яичников или кисты, не связанные с синдромом поликистозних яичников;
· гинекологические кровотечения неизвестной этиологии;
· карциномы яичников, матки или молочных желез.
Препарат нельзя применять в случаях, если невозможно получить эффективную реакцию на лечение, например при наличии:
· первичной недостаточности яичников;
· изъянов половых органов, несовместимых с беременностью;
· фиброидних опухолей матки, несовместимых с беременностью;
· первичной тестикулярной недостаточности.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Одновременное применение препарата ГОНАЛ- фâ с другими препаратами, которые применяют для стимуляции овуляции(например, лХГ, кломифену цитрат), может усиливать фолликулярную реакцию, тогда как совместимое приложение с агонистами или антагонистами гонадотропін-рилізинг-гормону(Гн-РГ), которые индуктируют десенсибилизацию гипофиза, может привести к увеличению дозирования ГОНАЛУ- фâ, необходимого для достижения адекватной овариальной реакции. О никаких другие клинически значимые врачебные взаимодействия во время терапии ГОНАЛОМ- фâ не сообщалось.
Особенности применения
Поскольку ГОНАЛ- фâ проявляет значительную гонадотропную активность, которая может повлечь развитие от легких к серьезным побочным реакциям, препарат могут назначать лишь врачи, хорошо осведомленные с проблемами неплодия и его лечения.
Терапия гонадотропинами нуждается определенных часовых обязательств от врачей и других медицинских работников, а также соответствующей аппаратуры для мониторинга лечения. Для женщин безопасное и эффективное применение препарата ГОНАЛ- фâ предусматривает регулярный мониторинг овариальной реакции с помощью ультразвукового исследования, преимущественно с одновременным определением сывороточного уровня эстрадиола. Реакция пациентов на введение ФСГ имеет индивидуальный характер, причем некоторые пациенты реагируют на ФСГ очень слабо, а другие - излишне. Для лечения как женщин, так и мужчин нужно применять самую низкую эффективную дозу препарата в соответствии с целью лечения.
Пациенты из порфириею
Пациентам из порфириею или со случаями порфирии в семейном анамнезе ГОНАЛ- фâ следует применять под тщательным медицинским надзором. При первых признаках развития этого состояния или при его ухудшении лечения следует прекратить.
Пациенты пожилого возраста и пациенты с почечной или печеночной недостаточностью
Безопасность и эффективность применения ГОНАЛУ- фâ для пациентов пожилого возраста, а также для пациентов с почечной или печеночной недостаточностью не были установлены.
ГОНАЛ- фâ содержит менее 1 ммоля натрию(23 мг) в одной дозе, то есть он практически не содержит натрия.
Лечение женщин
Перед началом лечения бесплодным супругам необходимо пройти обследование для выявления существующих и вероятных противопоказаний для беременности. В частности, пациентов следует обследовать на наличие гипотиреоза, недостаточности надпочечников, гиперпролактинемии и назначить им соответствующее специфическое лечение.
При проведении стимуляции роста фолликулов в рамках лечения ановуляторного неплодия или процедур ДРТ у пациенток может наблюдаться увеличение яичников или развитие гиперстимуляции. Соблюдение рекомендованного дозирования и режима введения препарата ГОНАЛ- фâ, а также тщательный мониторинг терапии минимизируют частоту подобных явлений. Точная интерпретация показателей фолликулярного развития и дозревания нуждается привлечения специалиста, который имеет опыт толкования соответствующих тестов.
В клинических исследованиях было показано усиление чувствительности яичников к действию препарата ГОНАЛ- фâ при одновременном введении лютропину альфа. Если считается необходимым увеличением дозы ФСГ, ее лучше всего изменять из 7 − 14-дневными интервалами на 37,5 − 75 МО. Непосредственного сравнения применения ГОНАЛУ- фâ/ЛГ и человеческого менопаузального гонадотропина(лМГ) не проводилось. Сравнение с литературными данными дает возможность допустить, что частота овуляций, полученная при применении ГОНАЛУ- фâ/ЛГ, подобна частоте, полученной для лМГ.
Синдром гиперстимуляции яичников(СГСЯ)
Ожидаемым следствием контролируемой овариальной стимуляции является определенное увеличение размеров яичников. Это явление, которое наиболее распространено среди женщин, больных синдромом поликистозних яичников, обычно проходит без соответствующего лечения.
В отличие от неускладненого увеличения яичников, СГСЯ − это синдром, который проявляется с нарастанием степени тяжести. Он включает заметное увеличение яичников, высокие сывороточные уровни половых стероидов и роста сосудистой проницаемости, который может привести к накоплению жидкости в брюшной, плевральной и изредка в перикардиальной полостях.
В тяжелых случаях СГСЯ может наблюдаться такая симптоматика: боль и ощущение розтягнення в брюшной полости, значительное увеличение яичников, увеличения массы тела, одышка, олигурия и желудочно-кишечные симптомы, включая тошноту, блюет и диарею. При клиническом обследовании могут быть выявлены гиповолемия, гемоконцентрация, электролитный дисбаланс, асцит, гемоперитонеум, плевральные излияния, гидроторакс и острый респираторный дистрес-синдром. Очень редко тяжелый СГСЯ может быть усложнен перекручиванием яичников и тромбоэмболическими осложнениями, такими как эмболия легочной артерии, ишемический инсульт и инфаркт миокарда.
Независимые факторы риска развития СГСЯ включают синдром поликистозних яичников, высокие абсолютные или быстро растущие сывороточные уровни эстрадиола(например > 900 пг/мл или > 3300 пмоль/л при ановуляции; > 3000 пг/мл или > 11000 пмоль/л при ДРТ) и большое количество растущих фолликулов(например > 3 фолликулов диаметром ≥ 14 мм при ановуляции; ≥ 20 фолликулы диаметром ≥ 12 мм при ДРТ).
Соблюдение рекомендованного дозирования и режима введения ГОНАЛУ- фâ может минимизировать риск развития овариальной гиперстимуляции. Для раннего установления соответствующих факторов риска рекомендуется проводить мониторинг циклов стимуляции с помощью ультразвукового исследования и определения уровня эстрадиола.
Известно, что лХГ играет ключевую роль в инициации СГСЯ и что этот синдром может становиться тяжелее и более длительным при наступлении беременности. Поэтому при наличии признаков овариальной гиперстимуляции, таких как сывороточные уровни эстрадиола > 5500 пг/мл или > 20200 пмоль/л и развитие свыше 40 фолликулов в целом, рекомендуется отменить введение лХГ и посоветовать пациентке воздержаться от половых сношений или применять барьерные средства контрацепции на протяжении по меньшей мере 4 дней. СГСЯ может быстро прогрессировать(в пределах 24 часов) и в течение нескольких дней стать серьезным медицинским осложнением. Чаще всего он наблюдается после прекращения гормонального лечения и достигает максимальной частоты приблизительно на 7 − 10-й день по завершению лечения. Следовательно, после введения лХГ пациентки должны находиться под медицинским надзором по меньшей мере в течение 2 недель.
При применении ДРТ частоту развития гиперстимуляции может уменьшить аспирация всех фолликулов к овуляции.
Обычно легкие или умеренные формы СГСЯ проходят спонтанно. Если наблюдается тяжелая форма СГСЯ, лечение гонадотропинами следует прекратить, если оно еще продолжается, пациентку следует госпитализировать и начать соответствующую терапию СГСЯ.
Многоплодная беременность
Многоплодная беременность, особенно высшего порядка, несет повышенный риск неблагоприятного результата родов и перинатального периода.
При индукции овуляции частота многоплодных беременностей более высока, чем при естественном оплодотворении. Большинство множественных оплодотворений представлено двойнями. Для минимизации риска многоплодной беременности рекомендуется тщательным образом контролировать овариальную реакцию.
При проведении процедур ДРТ риск многоплодной беременности связан главным образом с количеством пересаженных эмбрионов, их качеством и возрастом пациентки.
Пациенток необходимо поинформировать о потенциальном риске многоплодной беременности к началу лечения.
Прерывание беременности
У пациенток при проведении стимуляции роста фолликулов для индукции овуляции или ДРТ частота случаев прерывания беременности в результате выкидыша или спонтанного аборта более высока, чем при естественном оплодотворении. Внематочная беременность Женщины с заболеваниями труб в анамнезе имеют риск внематочной беременности независимо от того, или она наступила в результате спонтанного оплодотворения, или лечения неплодия. Сообщалось, что распространенность внематочной беременности после проведения ДРТ более высока, чем в общей популяции.Новообразование репродуктивной системы
Есть сообщение о развитии как доброкачественных, так и злокачественных новообразований в яичниках и других органах репродуктивной системы женщин, которые для лечения неплодия применяли несколько лекарственных средств. Еще не выяснено, или увеличивает лечение гонадотропинами начальный риск развития таких опухолей у бесплодных женщин.
Урожденные изъяны
Распространенность урожденных изъянов после проведения ДРТ может быть немного выше, чем после спонтанного оплодотворения. Считают, что это является следствием разницы в характеристиках родителей(например, материнский возраст, качество спермы) и многоплодных беременностей.
Тромбоэмболические явления
У женщин, для которых в целом установленные факторы риска развития тромбоэмболических явлений, такие как индивидуальные или семейные случаи, а также у женщин с существующими или недавними тромбоэмболическими заболеваниями лечения гонадотропинами может привести к дальнейшему повышению риска обострения или появления таких явлений. У таких женщин необходимо оценить преимущество применения гонадотропинив над риском развития подобных явлений. Однако следует отметить, что собственно беременность и СГСЯ увеличивают риск развития тромбоэмболических осложнений.
Лечение мужчин
Повышенные эндогенные уровни ФСГ у пациентов являются показателем первичной тестикулярной недостаточности. Такие пациенты нечувствительные к терапии препаратами ГОНАЛ- фâ/лХГ. ГОНАЛ- фâ не следует применять, если невозможно получить эффективную реакцию на лечение.
Для оценки реакции на лечение рекомендуется проводить анализ семенной жидкости через 4 − 6 месяцы от начала лечения.
Применение в период беременности или кормления груддю.
Показаний к применению ГОНАЛУ- фâ в период беременности нет. Даны, полученные для небольшого количества случаев применения препарата в период беременности(менее 300 случаев), указывают на отсутствие урожденных изъянов или фето- или неонатальной токсичности фолитропину альфа, хотя клинических данных для исключения тератогенного эффекта ГОНАЛУ- фâ недостаточно.
ГОНАЛ- фâ не показан для применения в период кормления груддю.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Ожидается, что ГОНАЛ- фâ не влияет или почти не влияет на способность пациентов руководить автомобилем и работать с другими механизмами.
Способ применения и дозы
Применение препарата ГОНАЛ- фâ следует начинать под надзором врача, который имеет опыт лечения неплодия.
Суточные дозы, режим введения и процесс мониторинга лечения с применением ГОНАЛУ- фâ не должны отличаться от тех, которые применяются для препаратов мочевого ФСГ. Сравнительные клинические исследования показали, что в сравнении с мочевым ФСГ применяют меньшую общую дозу ГОНАЛУ-ф® на протяжении более короткого периода лечения, которое дает возможность не только оптимизировать лечение, но и минимизировать риск нежелательной овариальной гиперстимуляции.
Рекомендуется придерживаться предложенных начальных доз препарата, нижеприведенных.
Для эквивалентных доз монодозовых и многодозовых врачебных форм ГОНАЛУ-ф® была показана их биоэквивалентность.
Женщины с ановуляцией, включая синдром поликистозних яичников
ГОНАЛ- фâ назначают в виде курса ежедневных инъекций. У пациенток с менструациями лечения следует начинать на протяжении первых 7 дни менструального цикла.
Обычно применяемый режим лечения начинается из введения 75 − 150 МО ФСГ ежедневно. В случае необходимости для получения адекватной, но не чрезмерной реакции дозу препарата можно увеличивать на 37,5(лучше) или на 75 МО с 7 - или(лучше) 14-дневными интервалами. Лечение должно быть адаптированным к индивидуальной реакции пациентки, которая оценивается по результатам ультразвукового исследования размера фолликула та/або определения уровня секреции естрогенив. Максимальная суточная доза препарата обычно не превышает 225 МО ФСГ. Если пациентка в течение 4 недель не реагирует на лечение должным образом, этот лечебный цикл прекращают, проводят дополнительное обследование пациентки и повторно начинают лечение с больше, чем в предыдущем цикле, начальной дозы препарата.
Когда достигнуто оптимальной реакции, в течение 24 − 48 часы после последней инъекции ГОНАЛУ- фâ одноразово вводят 250 мкг рекомбинантного лХГ(р-лХГ) или 5000 − 10000 МО лХГ. Пациентке рекомендуется этого и следующего после введения лХГ дня иметь половые сношения. Альтернативно можно провести внутриматочное оплодотворение.
Если наблюдается чрезмерная реакция, лечение необходимо прекратить и отменить введение лХГ(см. раздел "Особенности применения"). В следующем цикле лечения необходимо начинать с дозы, ниже той, что применяли в предыдущем цикле.
Стимуляция развития множественных фолликулов у женщин при проведении суперовуляции в рамках ДРТ или оплодотворение in vitro
Режим лечения, который обычно применяют для суперовуляции, заключается в введении 150 − 225 МО ГОНАЛУ- фâ ежедневно, начиная с 2-го или 3-го дня цикла. Лечения продолжают к достижению адекватного фолликулярного развития(какой оценивается за сывороточным уровнем естрогенив та/або по данным ультразвукового исследования). На протяжении лечения дозу препарата подбирают в соответствии с реакцией пациентки, но обычно доза не должна превышать 450 МО ежедневно. В целом надлежащее фолликулярное развитие достигается в среднем на 10-й день лечения(в пределах от 5 до 20 дней).
Для индукции окончательного дозревания фолликулов через 24 − 48 часы после последней инъекции ГОНАЛУ- фâ вводят разовую инъекцию 250 мкг р-лХГ или 5000 − 10000 МО лХГ.
Для притеснения резкого подъема уровня эндогенного ЛГ и контролю за тоническим уровнем ЛГ обычно применяют пригничувальну регуляцию агонистами или антагонистами гонадотропін-рилізинг-гормону(Гн-РГ). За обычным протоколом лечения введения ГОНАЛУ- фâ начинают приблизительно через 2 недели после начала применения агониста и продолжают их совместимое введение к достижению надлежащего фолликулярного развития. Например, после 2 недель лечения агонистом начинают вводить по 150 − 225 МО ГОНАЛУ- фâ в течение первых 7 дни, изменяя в дальнейшем эту дозу в соответствии с реакцией яичников.
Общий опыт применения IVF свидетельствует, что в целом частота успешного лечения остается стабильной в течение первых четырех попыток и потом постепенно снижается.
Женщины с ановуляцией, вызванной тяжелой недостаточностью секреции ЛГ и ФСГ
У женщин с тяжелой недостаточностью секреции ЛГ и ФСГ(гипогонадотропний гипогонадизм; уровень эндогенного ЛГ в крови < 1,2 МО/л) целью комбинированной терапии с применением ГОНАЛУ- фâ и лютропину альфа является развитие одного зрелого граафового фолликула, из которого после введения лХГ высвободится ооцит. ГОНАЛ- фâ назначают в виде курса ежедневных инъекций одновременно с введением лютропину альфа. Поскольку такие пациентки страдают на аменорею и имеют низкую эндогенную секрецию естрогенив, лечение можно начинать в любое время.
Рекомендованный режим лечения начинается из введения 75 МО лютропину альфа одновременно с 75 − 150 МО ФСГ ежедневно. Лечение нужно адаптировать к индивидуальной реакции пациентки, которая оценивается за уровнем секреции естрогенив и данными ультразвукового исследования размера фолликула.
Если считается необходимым увеличением дозы ФСГ, ее лучше всего изменять из 7 − 14-дневными интервалами на 37,5 − 75 МО. В рамках одного цикла может быть приемлемым увеличение длительности стимуляции до 5 недель.
Когда достигнуто оптимальной реакции, в течение 24 − 48 часы после последней инъекции ГОНАЛУ- фâ и лютропину альфа одноразово вводят 250 мкг р-лХГ или 5000 − 10000 МО лХГ. Пациентке рекомендуется этого и следующего после введения лХГ дня иметь половые сношения. Альтернативно можно провести внутриматочное оплодотворение.
Во время лечения следует учитывать необходимость поддержки лютеиновой фазы, поскольку отсутствие веществ с лютеотропной активностью(ЛГ/лХГ) после овуляции может повлечь преждевременную недостаточность желтого тела.
Если наблюдается чрезмерная реакция, лечение необходимо прекратить и отменить введение лХГ. В следующем цикле лечения необходимо начать с дозы ФСГ, ниже той, что применяли в предыдущем цикле.
Мужчины с гипогонадотропним гипогонадизмом
ГОНАЛ- фâ применяют в дозе 150 МО трижды на неделю одновременно с введением лХГ в течение по меньшей мере 4 месяцев. Если после окончания этого курса у пациента не наблюдается реакции, комбинированное лечение можно продолжить. Современный клинический опыт свидетельствует о том, что в случае необходимости для достижения сперматогенеза лечения можно продолжать по меньшей мере в течение 18 месяцев.
Если Вы вводите ГОНАЛ- фâ самостоятельно, пожалуйста, внимательно прочитайте и выполняйте нижеследующие инструкции
ГОНАЛ- фâ предназначен для подкожного введения. Самостоятельное введение ГОНАЛУ- фâ могут проводить лишь должным образом наученные пациенты, которые в случае необходимости имеют возможность консультироваться со специалистом. Первую инъекцию ГОНАЛУ- фâ необходимо проводить под непосредственным надзором медицинского работника. Следующую инъекцию следует делать в то же время на следующий день, каждый раз изменяя участок для введения. Раствор препарата нельзя вводить, если он непрозрачен или содержит частицы.
Непосредственно перед применением порошок следует развести растворителем, который добавляется к упаковке. Чтобы предотвратить введение больших объемов раствора, в 1 мл растворителя можно разводить максимально содержимое 3 флаконов препарата.
- Вымойте руки. Важно, чтобы Ваши руки и все, что Вы будете использовать, были как можно чище.
- Подготовьте все необходимые материалы. На чистую поверхность положите один флакон с препаратом, один предварительно заполненный шприц с растворителем, одну иглу для приготовления раствора, одну тонкую иглу для подкожных инъекций, два тампона, пропитанных спиртом, а также контейнер для использованного стекла и игл.
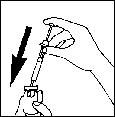
- Приготовьте раствор для инъекций. Для этого снимите защитные колпачки из флакона с препаратом и из предварительно заполненного шприца с растворителем.
|
|
К предварительно заполненному шприцу с растворителем присоедините иглу для приготовления раствора и медленно введите весь растворитель к флакону с порошком. Коловими движениями осторожно перемешайте содержимое флакона, не вынимая из него иглу шприца. Не стряхивайте флакон. |
|
|
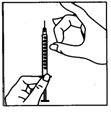
После растворения порошка(какое обычно происходит сразу) проверьте прозрачность полученного раствора и отсутствие в нем любых частиц. Переверните флакон вверх дном и медленно втяните раствор обратно к шприцу. |
( Если Вам назначили введение содержимого нескольких флаконов ГОНАЛУ- фâ, повторно вводите полученный раствор к следующим флаконам с порошком до тех пор, пока Вы не растворите содержимое назначенного количества флаконов с порошком. Если кроме ГОНАЛУ- фâ Вам назначили препарат лютропину альфа, Вы также можете смешивать эти два препарата, которые являются альтернативой введения каждого препарата отдельно. В таком случае после растворения порошка лютропину альфа втяните раствор обратно к шприцу и повторно введите его к флакону с порошком ГОНАЛУ- фâ. После его растворения втяните раствор обратно к шприцу. Проверьте раствор на наличие частиц, как описано выше, и не используйте раствор, если он непрозрачен. В 1 мл растворителя можно разводить максимально содержимое трех флаконов с порошком).
- Замените иглу на тонкую иглу для подкожных инъекций и удалите из шприца пузырьки воздуха.
|
|
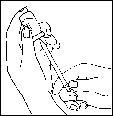
Если Вы видите пузырьки воздуха в шприце, слегка постучите по шприцу, держа его кверху иглой, пока весь воздух не соберется в его верхней части. Нажимайте на поршень шприца, пока пузырьки воздуха не будут удалены. |
- Сразу же после этого введите инъекцию: Ваш врач или медицинская сестра уже посоветовали Вам, куда делать инъекцию(например в живот или переднюю часть бедра).
|
|
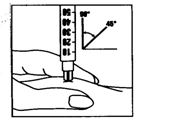
Протрите площадь, избранную для инъекции, тампоном, пропитанным спиртом. Крепко сожмите кожу и вставьте иглу под углом 45 − 90°. Введите инъекцию под кожу, как Вас научили. Не вводите инъекцию непосредственно к вене. Введите весь раствор, осторожно нажимая на поршень. Сразу же выньте иглу и коловими движениями протрите кожу тампоном, пропитанным спиртом. |
- Утилизируйте все использованные предметы: сразу же по завершению инъекции положите все иглы и пустые стеклянные емкости в контейнер для острых предметов. Также следует утилизировать неиспользованный раствор.
Деть.
ГОНАЛ- фâ не применяют для лечения детей.
Передозировка
Проявления передозировки ГОНАЛУ- фâ неизвестны, однако нельзя исключать возможности развития синдрома гиперстимуляции яичников, описанного в разделе "Особенности приложения".
Побочные реакции
Самыми распространенными побочными реакциями, о которых сообщается в связи с применением препарата, является головная боль, кисты яичников и местные реакции в месте введения инъекции(например боль, эритема, гематома, отекла та/або раздражение в месте инъекции).
Синдром гиперстимуляции яичников(СГСЯ) легкой или умеренной степени тяжести, о которой также сообщается достаточно часто, является неотъемлемым риском процедуры стимуляции, но случаи тяжелого СГСЯ нераспространены.
Очень редко возможны тромбоэмболические осложнения.
Для определения частоты побочных реакций используется такая классификация: очень распространены(≥ 1/10); распространенные(от ≥ 1/100 к < 1/10); нераспространенные(от ≥ 1/1000 к < 1/100); одиночные(от ≥ 1/10000 к < 1/1000); редкие(< 1/10000).
Лечение женщин
Расстройства со стороны иммунной системы
Редкие: реакции гиперчувствительности от легкого к тяжелой степени, включая анафилактические реакции и шок.
Расстройства со стороны нервной системы
Очень распространены: головная боль.
Расстройства со стороны сосудов
Редкие: тромбоэмболия(связана или не связана с СГСЯ).
Дыхательные, торакальни и медиастинальные расстройства
Редкие: обострение или ухудшение астмы.
Расстройства со стороны пищеварительной системы
Распространены: абдоминальная боль, ощущения розтягнення и дискомфорта в брюшной полости, тошнота, блюет, диарея.
Расстройства со стороны репродуктивной системы и молочных желез
Очень распространены: кисты яичников;
распространены: СГСЯ от легкого к умеренной степени тяжести(включая сопутствующие симптомы);
нераспространены: тяжелый СГСЯ(включая сопутствующие симптомы) (см. раздел "Особенности применения");
одиночные: осложнение тяжелого СГСЯ.
Общие расстройства и реакции в месте введения
Очень распространены: реакции в месте инъекции(например боль, эритема, гематома, отекла та/або раздражение в месте инъекции).
Лечение мужчин
Расстройства со стороны иммунной системы
Редкие: реакции гиперчувствительности от легкого к тяжелой степени, включая анафилактические реакции и шок.
Дыхательные, торакальни и медиастинальные расстройства
Редкие: обострение или ухудшение астмы.
Расстройства со стороны кожи и подкожных тканей
Распространены: акнет.
Расстройства со стороны репродуктивной системы и молочных желез
Распространены: гинекомастия, варикоцеле.
Общие расстройства и реакции в месте введения
Очень распространены: реакции в месте инъекции(например боль, эритема, гематома, отекла та/або раздражение в месте инъекции).
Другие
Распространены: увеличение массы тела.
Срок пригодности. 2 годы.
Не применять после окончания срока пригодности, отмеченного на упаковке.
Для немедленного и одноразового приложения после первого открывания и разведения.
Условия хранения.
Хранить при температуре не выше 25 оС.
Хранить в оригинальной упаковке для защиты от света.
Хранить в недоступном для детей месте.
Упаковка
- Порошок для раствора для инъекций в флаконе № 1 в комплекте с растворителем(1 мл воды для инъекций) в предварительно заполненном шприце № 1, иглой для растворения № 1, иглой для введения № 1 в контурной ячейковой упаковке; по 1 контурной ячейковой упаковке в картонной коробке.
- Порошок для раствора для инъекций в флаконах № 5 в комплекте с растворителем(1 мл воды для инъекций) в предварительно заполненных шприцах № 5, иглами для растворения № 5, иглами для введения № 5 в контурной ячейковой упаковке; по 2 контурных ячейковых упаковки в картонной коробке.
Категория отпуска. За рецептом.
Производитель.
Мерк Сероно С.А., отделение в г. Обонн/Merck Serono S.A., Succursale d'Aubonne;
Мерк Сероно С.п.А./Merck Serono S.p.A.
Местонахождение производителя и адрес места осуществления его деятельности
Зон Індустрієль де Л'Урьєтаз, СН- 1170 Обонн, Швейцария /
Zone Industrielle de l'Ouriettaz, CH-1170 Aubonne, Switzerland;
Віа делле Магноліє 15(р-н Промышленная Зона), 70026 Модуньо(Баре), Италия/
Via delle Magnolie 15 (loc. frazione Zona Industriale), 70026 Modugno (Bari), Іtaly.
Другие медикаменты этого же производителя
Форма: порошок для приготовления раствора для инъекций по 8 мг, 1 или 5 флаконы с порошком, 1 или 5 картриджи из 1,37 мл растворителя(0,3 % (г./о.) раствор м-крезола в воде для инъекций) предварительно собранных в 1 или 5 пристроил для растворения(клик.изи), что состоят из 1 или 5 корпуса устройства и 1 или 5 стерильных переходных канюль в картонной коробке
Форма: раствор для инъекций по 250 мкг/0,5 мл по 0,5 мл в предварительно заполненном шприце; по 1 предварительно заполненному шприцу в контурной ячейковой упаковке в картонной коробке
Форма: раствор для инъекций по 900 МО(66 мкг) /1,5 мл по 1,5 мл в картридже с пробкой-поршнем и рифленой крышечкой, вмещенному в ручку для введения; по 1 ручке и 20 иглы в картонной коробке
Форма: раствор для инъекций по 12 мг(8,0 мг/мл) по 1,50 мл в картриджах № 1
Форма: гель влагалищный 8 % по 1,45 г(что отвечает дозе для введения 1,125 г) в одиндозовом апликатори, вложенному в многослойную упаковку, по 6 или 15 одиндозовых апликаторив в картонной коробке