Ирина® Плюс
Регистрационный номер: UA/12155/01/01
Импортёр: Байер АГ
Страна: ГерманияАдреса импортёра: Кайзер-Вильгельм-Алее 1, 51373 Леверкузен, Германия
Форма
таблетки, покрытые оболочкой, № 28: по 21 таблетке оранжевого цвета и по 7 таблетки светло-оранжевого цвета в блистере; по 1 блистеру в картонной пачке
Состав
1 упаковка содержит 28 таблетки, покрытые оболочкой(21 таблетка оранжевого цвета и 7 таблетки светло-оранжевого цвета); 1 таблетка оранжевого цвета содержит етинилестрадиолу 0,03 мг, дроспиренону 3 мг и левомефолату кальцию 0,451 мг 1 таблетка светло-оранжевого цвета содержит левомефолату кальцию 0,451 мг
Виробники препарату «Ирина® Плюс»
Страна производителя: Германия
Адрес производителя: Мюллєрштрассе 178, 13353, Берлин, Германия
Страна производителя: Германия
Адрес производителя: Доберайнерштрассе 20, 99427 Ваймар, Германия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
ИРИНА® ПЛЮС
(YARINA® PLUS)
Состав
действующие вещества: етинилестрадиол, дроспиренон, левомефолат кальцию;
1 упаковка содержит 28 таблетки, покрытые оболочкой(21 таблетка оранжевого цвета и 7 таблетки светло-оранжевого цвета);
1 таблетка оранжевого цвета содержит етинилестрадиолу 0,03 мг, дроспиренону 3 мг и левомефолату кальцию 0,451 мг;
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, натрию карбокси-метилцеллюлоза, гидроксипропилцеллюлоза, магнию стеарат, гипромелоза, макрогол 6000, тальк, титану диоксид(Е 171), железа оксид желт(Е 172), железа оксид красен(Е 172);
1 таблетка светло-оранжевого цвета содержит левомефолату кальцию 0,451 мг;
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, натрию карбокси-метилцеллюлоза, гидроксипропилцеллюлоза, магнию стеарат, гипромелоза, макрогол 6000, тальк, титану диоксид( Е 171), железа оксид желт(Е 172), железа оксид красен(Е 172).
Врачебная форма. Таблетки, покрытые оболочкой.
Основные физико-химические свойства:
- таблетки, покрытые оболочкой, которые содержат гормоны, круглые, двояковыпуклые, оранжевого цвета, с одной стороны которых тиснено "Y+" в правильном шестиугольнике;
- таблетки, которые содержат лишь левомефолат кальцию, покрыты оболочкой, круглые, двояковыпуклые, светло-оранжевого цвета, с одной стороны которых тиснен "М+" в правильном шестиугольнике.
Фармакотерапевтична группа. Гормоны половых желез и препараты, которые применяют при патологии половой сферы. Гормональные контрацептивы для системного приложения.
Код АТХ G03А A12.
Фармакологические свойства.
Фармакодинамика.
Механизм действия
Комбинированные оральные контрацептивы(КОК) снижают риск беременности главным образом путем притеснения овуляции. Другие возможные механизмы включают изменения характера цервикального слизи, благодаря которым усложняется проникновение спермы, и изменения едометрия, что снижают вероятность имплантации.
Фармакодинамічні свойства
Дроспіренон - аналог спиронолактону, что имеет антиминералокортикоидни и антиандрогенные свойства. Эстрогенный компонент препарата Ирина® Плюс - это етинилестрадиол.
Контрацептивное действие
Специальных исследований фармакодинамичних свойств препарата Ирина® Плюс не проводили.
Фолатна добавка
В ходе двух исследований изучали влияние препарата Ирина® Плюс на уровень фолатов в плазме и эритроцитах. В рандомизированном двойном слепом исследовании с активным контролем в параллельных группах сравнивались уровни фолатов в плазме и эритроцитах у женщин(пациенток) из США во время 24-недельного лечения 3 мг дроспиренону/0,02 мг етинилестрадиолу(препарат "Джаз") + 0,451 мг кальция левомефолату и во время лечения только препаратом "Джаз". Фармакодинамічний влияние на уровень фолатов в плазме крови, в эритроцитах и на профиль циркулирующих метаболитив фолатов оценивался в течение 24 недель лечения с помощью 0,451 мг кальция левомефолату или 0,4 мг фоллиевой кислоты(эквимолярная доза 0,451 мг кальция левомефолату) в комбинации из 3 мг дроспиренону/0,03 мг етинилестрадиолу(Ирина®) со следующим немаскованим приложением на протяжении 20 недель только препарату Ирина® (фаза элиминации).
Фармакокинетика.
Препараты Ирина® Плюс и Ирина является биоэквивалентной учитывая дроспиренон и етинилестрадиол.
Абсолютная биодоступность дроспиренону при приеме таблетки с содержимым только дроспиренону представляет около 76 %. Абсолютная биодоступность етинилестрадиолу - приблизительно 40 %, что является результатом пресистемной конъюгации и эффекта первого прохождения. Абсолютная биодоступность препарата Ирина® Плюс, которая содержит комбинацию дроспиренону и етинилестрадиолу, стабилизированную бетадексу клатратом(молекулярный комплекс), не исследовалась. Етинілестрадіол имеет одинаковую биодоступность при применении в виде комплекса с бетадексу клатратом и при приеме как свободного стероиду. Сывороточные концентрации дроспиренону и етинилестрадиолу достигают максимального уровня через 1-2 часы после приема препарата Ирина® Плюс.
Фармакокинетика дроспиренону после приема одноразовых доз от 1 до 10 мг имеет дозозависимый характер. При ежедневном применении препарата "Ирина®" равновесная концентрация дроспиренону достигалась через 8 дни. Наблюдалось почти 2-3 кратное повышение показателей Сmax и AUC(0-24 часы) в сыворотке крови дроспиренону после многократного применения препарата "Ирина®" (см. таблицу 1).
Для етинилестрадиолу равновесные условия наблюдались в течение второй половины курса лечения. При ежедневном применении препарата Ирина®, показатели сывороточного уровня Сmax и AUC(0-24 часы) етинилестрадиолу повысились почти в 1,5-2 разы(см. таблицу 1).
Кальцию левомефолат за своей структурой есть идентичным L- 5-метилтетрагидрофолату(L- 5-метил-ТГФ), метаболиту витамину В9. Средняя начальная концентрация у лиц, которые не употребляют продукты, обогащенные фоллиевой кислотой, однако имеют нормальный питательный рацион, представляет 15 нмоль/л. При пероральном приеме кальция левомефолат абсорбируется и накапливается в организме. Максимальная концентрация в плазме крови, что на 50 нмоль/л выше початкого уровня, достигается через 0,5-1,5 часы после одноразового перорального приема кальция левомефолату в дозе 0,451 мг.
Равновесные условия для общего уровня фолата в плазме крови после приема 0,451 мг кальция левомефолату достигаются приблизительно через 8-16 недели, в зависимости от показателей начального уровня. Равновесная концентрация кальция левомефолату в эритроцитах достигается несколько позже, что предопределенно более длинным жизненным циклом эритроцитов - 120 дни.
Таблица 1
Фармакокінетичні параметры препарата "Ирина®" (3 мг дроспиренону и 0,03 мг етинилестрадиолу)
|
Дроспіренон Средние значения(%) |
|||||
|
Курс/сутки |
Количество пациентов |
Сmax(нг/мл) |
Tmax(год) |
AUC(0-24год) ( нг*год/мл) |
T1/2(год) |
|
1/1 |
12 |
36,9 (13) |
1,7 (47) |
288 (25) |
Не применяется |
|
1/21 |
12 |
87,5 (59) |
1,7 (20) |
827 (23) |
30,9 (44) |
|
6/21 |
12 |
84,2 (19) |
1,8 (19) |
930 (19) |
32,5 (38) |
|
9/21 |
12 |
81,3 (19) |
1,6 (38) |
957 (23) |
31,4 (39) |
|
13/21 |
12 |
78,7 (18) |
1,6 (26) |
968 (24) |
31,1 (36) |
|
Етинілестрадіол Средние значения(%) |
|||||
|
Курс/сутки |
Количество пациентов |
Сmax(нг/мл) |
Tmax(год) |
AUC(0-24год) ( нг*год/мл) |
T1/2(год) |
|
1/1 |
11 |
53,5 (43) |
1,9 (45) |
280 (87) |
Не применяется |
|
1/21 |
11 |
92,1 (35) |
1,5 (40) |
461 (94) |
Не применяется |
|
6/21 |
11 |
99,1 (45) |
1,5 (47) |
346 (74) |
Не применяется |
|
9/21 |
11 |
87 (43) |
1,5 (42) |
485 (92) |
Не применяется |
|
13/21 |
10 |
90,5 (45) |
1,6 (38) |
469 (83) |
Не применяется |
Влияние еды
Скорость абсорбции дроспиренону и етинилестрадиолу после одноразового применения препаратов, подобных к Ирина® Плюс, была ниже при приеме после еды(богатой на содержимое жиров), при этом средняя сывороточная концентрация(Сmax) обоих веществ снизилась почти на 40 %. Однако степень абсорбции дроспиренону осталась неизменной. Зато степень абсорбции етинилестрадиолу уменьшилась почти на 20 % при применении после еды.
Влияние еды на абсорбцию кальция левомефолату при применении препарата Ирина® Плюс не изучался.
Распределение
Спад сывороточных концентраций дроспиренону и етинилестрадиолу происходит в два этапа. Мнимый объем распределения дроспиренону представляет около 4 л/кг, а етинилестрадиолу - близко
4-5 л/кг.
Дроспіренон не связывается с глобулином, который связывает половые гормоны(ГЗСГ), или глобулином, который связывает кортизол(ГЗК), однако связывание с другими белками сыворотки крови представляет около 97 %. После многократного приложения в течение больше 3 курсов не отмечены никаких изменений свободной фракции(по показателям минимальной концентрации). Сообщается, что етинилестрадиол активно, однако неспецифический связывается с сывороточным альбумином(около 98,5 %) и стимулирует повышение сывороточных концентраций как ГЗСГ, так и ГЗК. Такое влияние на ГЗСГ и ГЗК, предопределенный действием етинилестрадиолу, не изменялся при изменении доз дроспиренону в диапазоне 2-3 мг.
Сообщалось о двухфазной кинетике фолатов из скорым и медленным обновлениям их запасов. Быстрое обновление запасов, которое, возможно, отображает недавно абсорбированные фолаты, отвечает показателю конечного периода полувыведения, которое представляет приблизительно 4-5 часы после одноразового перорального приема кальция левомефолату в дозе 0,451 мг. Для медленного обновления запасов, которое отображает метаболизм полиглютамату фолата, среднее время содержания представляет 100 дни или больше.
Метаболизм
Два основных метаболити дроспиренону, выявленные в плазме человека - это кислотная форма дроспиренону, что образуется в результате раскрытия лактонового кольца, и 4,5-дигидро-дроспиренон-3-сульфат, что является результатом редукции и следующего сульфирования. Установлено, что эти метаболити является фармакологически неактивными. Дроспіренон также испытывает окислительный метаболизм под действием CYP3A4.
Сообщалось, что етинилестрадиол проходит значительный пресистемний метаболизм в кишечнике и печенке. Метаболизм етинилестрадиолу и его окислительных метаболитив происходит преимущественно путем конъюгации из глюкуронидом или сульфатом. CYP3A4 в печенке отвечает за 2-гидроксилювання, что является основной реакцией окисления. 2-гидрокси метаболит проходит дальнейшую трансформацию во время метилювання и глюкуронидации перед тем, как быть выведенным с мочой и калом.
L- 5-метил-ТГФ - преобладающее соединение фоллиевой кислоты в системе кровообращения, которое транспортируется при физиологичных условиях и во время применения фоллиевой кислоты и кальция левомефолату.
Выведение
Сывороточная концентрация дроспиренону характеризуется конечным периодом полувыведения в фазе распределения около 30 часов как после одноразового, так и многократного приложения. Выведение из организма дроспиренону было почти полным через 10 дни, а выведенные количества оказались несколько выше в калении, чем в моче. Дроспіренон проходит активный метаболизм, и с мочой и калом выделяются только незначительные количества неизмененного дроспиренону. В моче и калении выявлено по меньшей мере 20 разных метаболитив. Около 38-47 % метаболитив в моче - конъюгати из глюкуронидами и сульфатами. Почти 17-20 % метаболитив, выявленных в калении, выводились в форме глюкуронидив и сульфатов.
Конечный период полувыведения в фазе распределения етинилестрадиолу представлял, по сообщениям, около 24 часов. Етинілестрадіол не выводится в неизмененном виде. Етинілестрадіол выводится с мочой и калом в форме конъюгатив из глюкуронидами и сульфатами и проходит ентерогепатичну циркуляцию.
L- 5-метил-ТГФ выводится из организма с мочой в форме неизмененных фолатов и продуктов катаболизма и с калом в процессе двухфазной кинетики.
Применение в особенных группах пациенток
Применение детям. Безопасность и эффективность применения препарата Ирина® Плюс установлена для женщин репродуктивного возраста. Ожидается, что препарат будет обнаруживать аналогичную эффективность у подростков постпубертатного возраста до 18 лет и пациенток в возрасте от 18 лет. Это лекарственное средство не назначать к началу менструаций.
Применение осибам пожилого возраста. Применение препарата Ирина® Плюс у женщин постклимактерического возраста не исследовали; препарат не назначают пациенткам этой группы.
Расовые отличия. Не отмечено клинически значимых отличий фармакокинетичних свойств дроспиренону или етинилестрадиолу у японок и представительниц европеоидной расы(возрастом 25-35 годы) при ежедневном применении препарата с содержимым 3 мг дроспиренону/0,02 мг етинилестрадиолу в течение 21 суток. Специальные исследования относительно особенностей в других этнических группах не проводились.
Нарушение функции почек. Препарат Ирина® Плюс противопоказанный для применения пациенткам с нарушением функции почек.
Влияние нарушения функции почек на фармакокинетични свойства дроспиренону(в дозе 3 мг на сутки в течение 14 дней) и влияние дроспиренону на концентрацию калия в сыворотке изучали в трех отдельных группах женщин(n =3D 28, возраст 30-65). Все лица находились на диете с низким потреблением калия. В течение исследования 7 лица продолжали принимать калийзберигаючи препараты для лечения их основного заболевания. На 14-й день терапии дроспиреноном(равновесное состояние) сывороточные концентрации дроспиренону в группе с клиренсом креатинина 50-79 мл/хв были аналогичными концентрациям в группе с клиренсом креатинина ≥ 80 мл/мин. У лиц с клиренсом креатинина 30 - 49 мл/хв сывороточные концентрации дроспиренону были в среднем на 37 % выше, чем у пациенток из контрольной группы. При лечении дроспиреноном не отмечено ни одного клинически значимого влияния на уровень калия в сыворотке крови. Невзирая на то, что в исследовании не наблюдалось гиперкалиемии, в 5 из 7 лиц, которые продолжали применение калийзберигаючих препаратов во время исследования, средняя сывороточная концентрация калия повысилась до 0,33 мекв/л(см. разделы "Противопоказания" и "Особенности применения").
Нарушение функции печенки. Препарат Ирина® Плюс противопоказанный для применения пациенткам с болезнями печенки.
Средняя экспозиция дроспиренону у женщин с нарушением функции печенки умеренной степени является почти втрое выше экспозиции у женщин с нормальной функцией печенки. Препарат Ирина® Плюс не исследовался у женщин с тяжелыми нарушениями функции печенки(см. разделы "Противопоказания" и "Особенности применения").
Медикаментозное взаимодействие
Для получения более детальной информации о взаимодействии с гормональными контрацептивами или о возможных ферментных изменениях следует пересмотреть инструкции для медицинского применения всех препаратов, которые назначают одновременно с этим лекарственным средством.
Влияние других лекарственных средств на КОК.
Вещества, которые снижают эффективность КОК. Лекарственные средства или фитопрепараты, которые индуктируют определенные ферменты, в том числе CYP3A4, могут снижать эффективность КОК или усиливать прорывные кровотечения.
Вещества, которые повышают концентрацию КОК в плазме крови. При сопутствующем применении аторвастатину и определенных КОК, что содержат етинилестрадиол, отмечается повышение показателей AUC етинилестрадиолу почти на 20 %. Аскорбиновая кислота и ацетаминофен могут приводить к увеличению концентрации етинилестрадиолу в плазме крови, вероятно, через притеснение конъюгации. В ходе клинического исследования из изучения взаимодействия препаратов, что проводы с участием 20 женщины предклимактерического возраста, при применении 1 раз в сутки таблеток с содержимым 3 мг дроспиренону и 0,02 мг етинилестрадиолу одновременно с мощным ингибитором CYP3A4 кетоконазолом в дозе 200 мг дважды на сутки в течение 10 дней отмечалось повышение AUC(0-24) дроспиренону и етинилестрадиолу соответственно в 2,68 раза(90 % ДІ: 2,44, 2,95) и 1,4 раза(90 % ДІ: 1,31, 1,49). Показатель Cmax испытал 1,97-кратное повышение(90 % ДІ: 1,79, 2,17) и 1,39-кратное повышение(90 % ДІ: 1,28, 1,52) дроспиренону и етинилестрадиолу соответственно. Невзирая на то, что не было отмечено ни одного клинически значимого влияния на безопасность или лабораторные показатели, в том числе уровень калия в сыворотке крови, следует учитывать, что в этом исследовании субъекты изучались лишь в течение 10 дней. Клинические последствия приема КОК с содержимым дроспиренону одновременно с непрерывным применением ингибитора CYP3A4/5 неизвестны(см. раздел "Особенности применения").
Ингибиторы протеазы вируса иммунодефицита человека(ВИЧ) /вируса гепатита С(ВГС) и ненуклеозидни ингибиторы обратной транскриптази. В некоторых случаях при одновременном приложении КОК с ингибиторами протеазы ВИЧ/ВГС или ненуклеозидними ингибиторами обратной транскриптази наблюдались значительные изменения(увеличение или уменьшение) плазменной концентрации эстрогена и прогестина.
Антибиотики. Есть сообщение о случаях наступления беременности во время применения гормональных контрацептивов и антибиотиков, однако клинические исследования из изучения фармакокинетичних свойств не выявили стойкого влияния антибиотиков на концентрацию синтетических стероидов в плазме крови.
Влияние КОК на другие препараты
КОК с содержимым етинилестрадиолу могут подавлять метаболизм других препаратов. Установлено, что КОК значительно снижают концентрацию ламотриджину в плазме крови, вероятно, через индуктирование глюкуронування ламотриджину. Вследствие этого возможное уменьшение контролю над судорогами, потому может нуждаться корректировка дозы ламотриджину. Для получения более детальной информации о взаимодействии из КОК или о возможных ферментных изменениях пересмотрите инструкции для медицинского применения всех препаратов, которые назначают одновременно с этим лекарственным средством.
В условиях in vitro етинилестрадиол является ингибитором обратного действия относительно изоферментов CYP2C19, CYP1A1 i CYP1A2 и необратимым ингибитором изоферментов CYP3A4/5, CYP2C8 i CYP2J2. Метаболизм дроспиренону и потенциальное влияние дроспиренону на печеночные CYP- ферменты изучали в исследованиях in vitro и in vivo. В ходе двух исследований in vitro дроспиренон не обнаруживал влияния на метаболизм модельных субстратов CYP1A2 i CYP2D6, однако подавлял метаболизм модельных субстратов CYP1A1, CYP2C9, CYP2C19 i CYP2A4, при этом наиболее чувствительным ферментом был CYP2C19. Потенциальное влияние дроспиренону на активность изоферменту CYP2C19 изучали в ходе исследования клинической фармакокинетики с применением омепразолу как маркерного субстрата. В ходе исследования при участии 24 женщин постклимактерического возраста(12 женщины с гомозиготным(дикого типа) генотипом CYP2C19 и 12 женщины с гетерозотним генотипом CYP2C19) при ежедневном пероральном применении дроспиренону в дозе 3 мг в течение 14 дней не отмечены влиянию на клиренс омепразолу(40 мг, одноразовая пероральная доза) и 5-гидроксиомепразолу, образованного под действием CYP2C19. Кроме того, не было выявлено ни одного значительного влияния дроспиренону на системный клиренс омепразолу сульфона, метаболиту, образованного с помощью CYP3A4. Эти результаты свидетельствуют, что дроспиренон не подавляет CYP2C19 i CYP3A4 в условиях in vivo.
Были проведены два дополнительных клинических исследования из изучения медикаментозного взаимодействия с использованием симвастатину и мидазоламу как маркерных субстратов для CYP3A4, в каждом из которых участвовали 24 здоровые женщины постклимактерического возраста. Результаты этих исследований показали, что дроспиренон в равновесной концентрации, достигнутой после его приложения в дозе 3 мг/сутки, не обнаруживает влияния на фармакокинетични свойстве субстратов CYP3A4.
Женщины, которые получают заместительную терапию гормонами щитообразной железы, могут нуждаться высших доз тиреоидного гормона, поскольку на фоне применения КОК сывороточная концентрация глобулина, который связывает тиреоидные гормоны, растет.
Взаимодействие с препаратами, которые могут повышать сывороточный уровень калия. У женщин, которые принимают препарат Ирина® Плюс одновременно с другими препаратами, которые могут повышать уровень калия в сыворотке крови, существует вероятность роста сывороточной концентрации калия(см. раздел "Особенности применения").
Было проведено исследование из изучения медикаментозного взаимодействия, в котором сравнивали применение дроспиренону 3 мг/эстрадиола 1 мг и плацебо у 24 женщин постклимактерического возраста с артериальной гипертензией умеренной степени, что принимали еналаприлу малеат в дозе 10 мг дважды на сутки. Уровень калия проверяли у всех участниц исследования через день в течение 2 недель. Средняя сывороточная концентрация калия в группе, которая получала дроспиренон/эстрадиол, была на 0,22 мекв/л более высокой относительно исходного уровня в плацебо-группе. Кроме этого, уровень калия в сыворотке крови измерялся в отдельных часовых точках в течение 24 часов на исходном уровне и на 14-й день. Состоянием на 14-й день соотношения между Cmax и AUC сывороточного уровня калия в группе, которая получала дроспиренон/эстрадиол, и плацебо-группе было соответственно 0,955(90 % ДІ: 0,914, 0,999) и 1,010(90 % ДІ: 0,944, 1,08). Ни у одной пациентки из обеих групп лечения не отмечено развитию гиперкалиемии(уровень калия в сыворотке крови ˃ 5,5 мекв/л).
Влияние фолатов на другие препараты. Фолаты, такие как фоллиевая кислота и левомефолат кальцию, могут изменять фармакокинетични или фармакодинамични свойства определенных антифолатов(например противоэпилептические средства, метотрексат).
Влияние других препаратов на фолаты. Сообщалось, что отдельные препараты(метотрексат, сульфасалазин, холестирамин, противоэпилептические препараты) вызывают снижение уровня фолатов.
Доклинические данные из безопасности
В ходе исследования канцерогенности у животных, что длилось 24 месяцы, при пероральном приложении 10 мг/кг/день дроспиренону или 1+0,01, 3+0,03 и 10+0,1 мг/кг/день дроспиренону и етинилестрадиолу, что представляло 0,1-2 кратную экспозицию(AUC дроспиренону) у женщин, которые получают контрацептивы, определили увеличения случаев развития карциномы гардеровой железы в группе, которая получала монотерапию высокими дозами дроспиренону. В похожем исследовании у другого вида животных при пероральном приложении 10 мг/кг/день дроспиренону или 0,3+0,003, 3+0,03 и 10+0,1 мг/кг/день дроспиренону и етинилестрадиолу, что представляло 0,8-10 кратную экспозицию у женщин, которые получают контрацептивы, определяли увеличения случаев развития доброкачественных и общего количества(доброкачественных и злокачественных) феохромацитом надпочечников в группе, которая получала монотерапию высокими дозами дроспиренону. Исследования мутагенности дроспиренону, что были проведены in vivo и in vitro, не выявили свидетельств мутагенной активности.
Долговременных исследований на животных для определения канцерогенного потенциала левомефолату не проводили. Исследования мутагенности левомефолату, что были проведены in vivo и in vitro, не выявили свидетельств мутагенной активности.
Клинические характеристики
Показание
· Пероральная контрацепция.
Препарат Ирина® Плюс предназначен для применения женщинам с целью предупреждения беременности.
· Обеспечение фолатного статуса.
Препарат Ирина® Плюс назначать женщинам, которые избрали пероральную контрацепцию как метод предупреждения беременности, для повышения уровня фолатов с целью уменьшения риску возникновения дефекта нервной трубки.
Противопоказание
Препарат Ирина® Плюс не назначать женщинам в случае наличия хотя бы одного из нижеозначенных состояний или заболеваний.
· Нарушение функции почек.
· Недостаточность коры надпочечников.
· Высокий риск развития артериального или венозного тромбоза. К этой категории, в частности, принадлежат женщины, которые, :
- жгут и имеют возраст свыше 35 лет(см. раздел "Особенности применения");
- имеют тромбоз глубоких вен или тромбоэмболию легочной артерии(ТЕЛА), в том числе в анамнезе(см. раздел "Особенности применения");
- имеют цереброваскулярное заболевание(см. раздел "Особенности применения");
- больные ишемической болезнью сердца(см. раздел "Особенности применения");
- имеют тромбогенни изъяны клапана сердца или тромбогенни нарушения сердечного ритма(например подострый бактериальный эндокардит с поражением клапана или фибрилляция передсердь(см. раздел "Особенности применения"));
- больные наследственной или приобретенной гиперкоагулопатией(см. раздел "Особенности применения");
- больные неконтролируемой артериальной гипертензией(см. раздел "Особенности применения");
- больные сахарным диабетом с сосудистыми осложнениями(см. раздел "Особенности применения");
- страдают на головные боли из вогнищевими неврологическими симптомами или мигрени с аурой или без и имеют возраст свыше 35 лет(см. раздел "Особенности применения").
· Аномальное маточное кровотечение незъясованой этиологии (см. раздел "Особенности применения".
· Рак молочной железы или другие виды рака, чувствительные к естрогенив или прогестинив, в том числе в анамнезе(см. раздел "Особенности применения").
· Опухоли печенки, доброкачественные или злокачественные, или заболевания печенки(см. раздел "Особенности применения", "Способ применения и дозы").
· Беременность(из-за отсутствия потребности в применении КОК в течение беременности) (см. раздел "Особенности применения", "Применения в период беременности или кормления груддю").
· Применение комбинации лекарственных средств для лечения гепатита С, что содержат омбітасвір/паритапревір/рітонавір из или без добавления дасабувиру в результате потенциального повышения уровня АЛТ(см. разделы "Особенности применения" и "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Для получения более детальной информации о взаимодействии с гормональными контрацептивами или о возможных ферментативных изменениях пересмотрите инструкции для медицинского применения всех препаратов, которые назначают одновременно с этим лекарственным средством.
Влияние других препаратов на КОК
Вещества, которые вызывают уменьшение эффективности КОК
Лекарственные средства и растительные препараты, которые индуктируют определенные ферменты, в том числе цитохром Р450 3А4(CYP3A4), могут снижать эффективность КОК или усиливать прорывные кровотечения. Препараты, которые могут уменьшать эффективность гормональных контрацептивов, включают: фенитоин, барбитураты, карбамазепин, бозентан, фелбамат, гризеофульвин, окскарбазепин, рифампин, топирамат и лекарственные средства, которые содержат зверобоя. Взаимодействие оральных контрацептивов и других лекарственных средств может приводить к прорывному кровотечению та/або потере эффективности контрацептива. При терапии препаратами, которые индуктируют ферменты, одновременно с применением КОК альтернативный или дополнительный методы контрацепции следует применять в течение всего срока лечения соответствующим препаратом и еще в течение 28 дней после прекращения его приложения для обеспечения полноценной контрацепции.
Вещества, которые вызывают увеличение концентрации КОК в плазме крови
При сопутствующем применении аторвастатину и определенных КОК, что содержат етинилестрадиол, отмечается повышение показателей AUC етинилестрадиолу почти на 20 %. Аскорбиновая кислота и ацетаминофен могут приводить к увеличению концентрации етинилестрадиолу в плазме крови, вероятно, через притеснение конъюгации.
Сопутствующее применение умеренных или сильных ингибиторов CYP3A4, к которым принадлежат азольни противогрибковые препараты(кетоконазол, итраконазол, вориконазол, флуконазол), верапамил, макролиды(например, кларитромицин, эритромицин), дилтиазем и грейпфрутовый сок, может вызывать повышение концентрации в плазме крови эстрогена или прогестина или их обоих веществ. В клиническом исследовании из изучения взаимодействия препаратов, что проводилось при участии женщин предклимактерического возраста, при применении 1 раз в сутки препарату, который содержал 3 мг дроспиренону/0,02 мг етинилестрадиолу, одновременно с мощным ингибитором CYP3A4 кетоконазолом в дозе 200 мг 2 разы на сутки в течение 10 дней отмечалось умеренное повышение системной экспозиции дроспиренону. Экспозиция етинилестрадиолу увеличилась незначительно(см. раздел "Особенности применения" и "Фармакологические свойства").
Ингибиторы протеазы вируса иммунодефицита человека(ВИЧ) /вируса гепатита С(ВГС) и ненуклеозидни ингибиторы обратной транскриптази
В некоторых случаях при одновременном приложении КОК с ингибиторами протеазы ВИЧ/ВГС или ненуклеозидними ингибиторами обратной транскриптази наблюдались значительные изменения(увеличение или уменьшение) плазменной концентрации эстрогена и прогестина.
Антибактериальные средства
Есть сообщение о случаях наступления беременности во время применения гормональных контрацептивов и антибиотиков, однако клинические исследования из изучения фармакокинетичних свойств не выявили стойкого влияния антибиотиков на концентрацию синтетических стероидов в плазме крови.
Влияние КОК на другие препараты
КОК с содержимым етинилестрадиолу могут подавлять метаболизм других препаратов. Установлено, что КОК значительно снижают концентрацию ламотриджину в плазме крови, вероятно, через индуктирование глюкуронування ламотриджину. Вследствие этого возможное уменьшение контролю над судорожной активностью, потому может нуждаться коррекция дозы ламотриджину. Для получения более детальной информации о взаимодействии из КОК или о возможных ферментативных изменениях следует пересмотреть инструкции для медицинского применения всех препаратов, которые назначаются одновременно с этим лекарственным средством.
КОК, что повышают концентрацию ферментов цитохрома CYP450 в плазме крови
В ходе клинических исследований на фоне применения гормональных контрацептивов с содержимым етинилестрадиолу повышения концентрации субстратов CYP3А4(например, мидазолам) в плазме крови отсутствовало или мало незначительная степень, тогда как плазменные концентрации субстратов CYP2C19(например, омепразол и вориконазол) и субстратов CYP1A2(например, теофиллин и тизанидин) могли повышаться в диапазоне от незначительного к умеренной степени.
Клинические исследования не указывают на наличие ингибиторного потенциала в дроспиренону относительно CYP- ферментов человека при применении в клинически значимых концентрациях(см. раздел "Фармакологические свойства").
Женщины, которые получают заместительную терапию гормонами щитообразной железы, могут нуждаться высших доз тиреоидного гормона, поскольку на фоне применения КОК сывороточная концентрация глобулина, который связывает тиреоидные гормоны, растет.
Взаимодействие с препаратами, которые могут повышать сывороточный уровень калия
У женщин, которые принимают препарат Ирина® Плюс одновременно с другими препаратами, которые могут повышать уровень калия в сыворотке крови, существует вероятность роста сывороточной концентрации калия(см. разделы "Особенности применения", "Фармакологические свойства").
Влияние фолатов на другие лекарственные средства
Фолаты могут изменять фармакокинетични или фармакодинамични свойства некоторых препаратив-антифолатив, в частности противоэпилептических средств(например фенитоин), метотрексату или пириметамину, что может привести к снижению фармакологического эффекта препаратив-антифолатив.
Влияние других лекарственных средств на фолаты
Сообщалось, что отдельные препараты вызывают снижение уровня фолатов путем притеснения фермента дегидрофолатредуктази(например, метотрексат и сульфасалазин), путем уменьшения абсорбции фолатов(например, холестирамин) или с помощью неизвестных механизмов(например противоэпилептические препараты, такие как карбамазепин, фенитоин, фенобарбитал, примидон и вальпроева кислота).
Влияние на результаты лабораторных исследований
Применение контрацептивных стероидов может влиять на результаты определенных лабораторных анализов, в частности это касается факторов коагуляции, уровня липидов, толерантности к глюкозе и связывающим белкам. Дроспіренон увеличивает активность ренину и альдостерону в плазме крови, которая индуктируется его умеренной антиминералокортикоидной активностью. Фолаты могут скрывать дефицит витамина В12(см. раздел "Особенности применения" и подразделение "Влияние КОК на другие препараты" раздела "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
Особенности применения
Курение и серьезные сердечно-сосудистые осложнения
Курение повышает риск развития серьезных сердечно-сосудистых осложнений на фоне применения КОК. Этот риск растет с возрастом и с количеством выжженных за день папирос. Поэтому КОК не следует применять женщинам в возрасте старше 35 годы, которые жгут(см. раздел "Противопоказания").
Тромбоэмболические расстройства и другие сосудистые заболевания
Применение препарата Ирина® Плюс следует прекратить в случае развития артериальных или венозных тромбоэмболических осложнений.
Исходя из имеющейся информации касательно КОК, что содержат дроспиренон и 0,03 мг етинилестрадиолу(препарат "Ирина®"), КОК с содержимым дроспиренону ассоциируются с большим риском развития венозной тромбоэмболии(ВTE), чем КОК, что содержат левоноргестрел или другие прогестини. По данным эпидемиологических исследований сравнения рисков ВTE, возможно как полное отсутствие любого повышения риска, так и его увеличение в три раза. Перед началом применения препарата Ирина® Плюс у женщины, которая раньше не применяли КОК, и у женщины, которая переходит из другого контрацептива, который не содержит дроспиренон, следует оценить все риски и преимущества применения КОК с содержимым дроспиренону, учитывая вероятность развития ВTE. Дополнительно к другим факторам, чрез которых применение КОК является противопоказанным, к известным факторам риска ВTE принадлежат курение, ожирение и ВTE в семейном анамнезе(см. раздел "Противопоказания").
В ряде исследований сравнивали риск ВTE у женщин, которые принимали препарат Ирина® (что содержит
0,03 мг етинилестрадиолу и 3 мг дроспиренону), и у женщин, которые применяли другие КОК, в том числе из левоноргестрелом. Результаты исследований, которые проводили по требованию или при содействии регуляторных органов, обобщены в таблице 2.
Таблица 2
Расчетные данные(относительный риск) развития венозной тромбоэмболии у женщин, которые получают препарат Ирина®, сравнительно с женщинами, которые принимают оральные контрацептивы с содержимым других прогестинив
|
Эпидемиологическое исследование(авторы, год публикации) Популяция исследования |
Препарат сравнения(все препараты - низькодозовани КОК; содержимое етинилестрадиолу представляет ≤ 0,04 мг) |
Относительный риск(ВР) ( 95% ДІ) |
|
i3 Ingenix (Seeger 2007) Женщины, которые начинают применение |
Все КОК, что имелись в США во время проведения дослідженняb |
ВР: 0,9 (0,5-1,6) |
|
EURAS (Dinger 2007) Женщины, которые начинают застосуванняа |
Все КОК, что имелись в Европе во время проведения дослидженняс Левоноргестрел/ЕЕ |
ВР: 0,9 (0,6-1,4) ВР: 1,0 (0,6-1,8) |
|
Исследование за финансирование FDA(2011) Женщины, которые не пользовались комбинированными гормональными контрацептивами по меньшей мере в течение предыдущих 6 мисяцива Все женщины, которые применяют комбинированные гормональные контрацептивиа ( в том числе те, которые начинают и продолжают применение комбинированного гормонального контрацептива, что изучается в исследовании) |
Другие КОК, имеющиеся во время проведения дослідженняd Левоноргестрел/0,03 мг ЕЕ Другие КОК, имеющиеся во время проведения дослідженняd Левоноргестрел/0,03 мг ЕЕ |
ВР: 1,8 (1,3-2,4) ВР: 1,6 (1,1-2,2) ВР: 1,7 (1,4-2,1) ВР: 1,5 (1,2-1,8) |
а) в том числе женщины, которые не пользовались комбинированными гормональными контрацептивами по меньшей мере в течение предыдущих 6 месяцы
b) включая низькодозовани КОК, что содержат такие прогестини: норгестимат, норэтиндрон, левоноргестрел, дезогестрел, норгестрел, медроксипрогестерон или етинодиолу диацетат
с) включая низькодозовани КОК, что содержат такие прогестини: левоноргестрел, дезогестрел, диеногест, хлормадинону ацетат, гестоден, ципротерону ацетат, норгестимат или норэтиндрон
d) включая низькодозовани КОК, что содержат такие прогестини: норгестимат, норэтиндрон или левоноргестрел
Кроме вышеприведенных "регуляторных исследований", также проводили другие исследования с разными целями. В целом было проведено два проспективных когортних исследование(см. таблицу 2) : постмаркетинговое исследование из изучения безопасности(США) Ingenix(Seeger 2007) и Европейское постмаркетинговое исследование из изучения безопасности EURAS(Европейское активное мониторинговое исследование) (Dinger 2007). В продолжении исследования EURAS, Долговременном активном мониторинговом исследовании(LASS), не привлекали дополнительные лица, а проводили дальнейшую оценку риска развития ВТЕ. Также было проведено три ретроспективных когортних исследование: одно в США за финансирование FDA(см. таблицу 2), и два - в Дании(Lidegaard 2009, Lidegaard 2011). Кроме этого, были проведены два исследования "случай-контроль": одно в Дании - аналитическое исследование MEGA(van Hylckama Vlieg 2009) и одно в Германии(Dinger 2010). В добавление к этому проводились два когортних исследование типа "случай-контроль", в которых оценивался риск развития нелетальной идиопатической ВТЕ : исследование PharMetrics(Jick 2011) и исследование GPRD(Parkin 2011). Результаты всех этих исследований приведены на Рис. 1.
Рисунок 1. Риск развития ВТЕ на фоне применения препарата "Ирина®" и при применении КОК, что содержат левоноргестрел(откорректированный риск#)
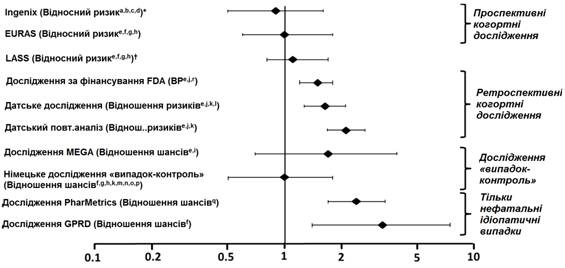
Отношения рисков отображены на логарифмической шкале; отношение рисков <1 означает низший риск развития ВТЕ при применении дроспиренону, а ˃1 означает повышенный риск развития ВТЕ дроспиренону.
* Препарат сравнения "другие КОК", в том числе содержимым левоноргестрелу.
† LASS - продолжение исследования EURAS.
# Некоторые дополнительные параметры обозначены надстрочными буквами: а) интенсивное курение; b) артериальная гипертензия; с) ожирение; d) семейный анамнез; е) возраст; f) ІМТ; g) время применения; h) ВТЕ в анамнезе; і) период включения; j) календарный год; k) образование; l) длительность использования; m) способность к деторождению; n) хроническое заболевание; о) сопутствующие лекарственные средства; р) курение; q) длительность экспозиции; r) место
( Ссылка: Ingenix(Seeger 2007), EURAS(Европейское активное мониторинговое исследование) (Dinger 2007), LASS(Довготривалe активное мониторинговое исследование) (Dinger, неопубликованный документ), Исследование за финансирование FDA(Sidney 2011), Датское исследование(Lidegaard 2009), Датский повторный анализ(Lidegaard 2011), исследование MEGA(van Hylckama Vlieg 2009), Немецкое исследование "случай-контроль"(Dinger 2010), PharMetrics(Jick 2011), исследование GPRD (Parkin 2011) 10).
Невзирая на повышение абсолютных показателей риска развития ВТЕ у женщин, которые принимают гормональные контрацептивы, сравнительно с лицами, которые не применяли их, частота возникновения ВТЕ в период беременности является еще больше, особенно в послеродовой период(см. мал.2). По оценкам, риск ВТЕ у женщин, которые пользуются КОК, представляет от 3 до 9 случаев на 10000 жінко-років. Наивысший риск ВТЕ наблюдается в течение первого года применения КОК. Данные большого проспективного когортного исследования из изучения безопасности разных КОК позволяют сделать предположение, что такое повышение риска, если сравнивать с лицами, которые не принимают КОК, является наивысшим в течение первых 6 месяцы применение КОК. Результаты этого исследования указывают, что наибольший риск развития ВТЕ отмечается в начале использования КОК или после возобновления приема(потом перерывы длительностью 4 недели или больше) КОК(того же или другого).
После прекращения применения КОК риск развития тромбоэмболических осложнений, вызванный приемом оральных контрацептивов, постепенно исчезает.
На мал.2 отображен риск развития ВТЕ у женщин, которые не являются беременными и не используют оральные контрацептивы; для женщин, которые принимают оральные контрацептивы; для беременных женщин и женщин в послеродовой период. Риск возникновения ВТЕ в перспективе выглядит таким образом: если проследить по состоянию здоровья 10000 женщин, которые не являются беременными и не принимают оральные контрацептивы, в течение 1 года, выяснится, что ВТЕ возникнет в 1-5 из таких женщин.
Рис. 2. Вероятность развития ВТЕ
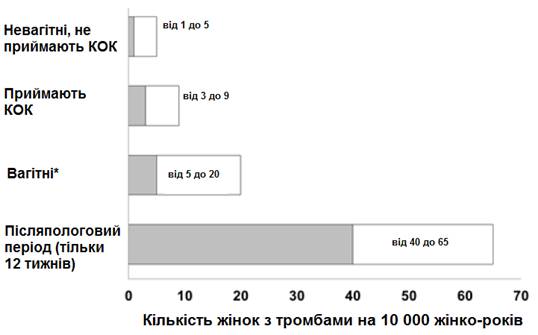
* Даны относительно беременных рассчитанные согласно фактической длительности беременности в соответствии с результатами контрольных исследований. Исходя из данных, что беременность длится девять календарных месяцев, частота представляет 7 - 27 случаи на 10000 жінко-років.
В случае возможности необходимо прекратить применение препарата Ирина® Плюс по крайней мере за 4 недели до больших операций или других хирургических вмешательств, при которых повышается риск тромбоэмболии, и не использовать препарат в течение 2 недель после таких операций.
Женщины, которые не кормят груддю, могут начинать прием препарата Ирина® Плюс не раньше чем через 4 недели после родов. Риск послеродовой тромбоэмболии снижается через 3 недели после родов, тогда как именно в это время риск овуляции повышается.
Применение КОК также вызывает повышение риска артериальных тромбозов, в частности инсульту и инфаркту миокарда, особенно у женщин с другими факторами риска развития упомянутых расстройств.
Установлено, что КОК повышают как относительный, так и популяционный риск развития цереброваскулярных явлений(ишемический и геморрагический инсульт), хотя в целом риск является выше у женщин старшего возраста(˃35 годы), больных артериальной гипертензией, которые жгут. Применение КОК также повышает риск инсульта у женщин с другими основными факторами риска.
Применение оральных контрацептивов женщинам с факторами риска развития цереброваскулярных заболеваний нуждается осторожности.
Применение препарата Ирина® Плюс следует прекратить при потере зрения незъясованой этиологии, проптози, диплопии, отеке диска зрительного нерва и сосудистых поражениях сетчатки. Необходимо немедленно сделать обследование относительно выявления возможного тромбоза ретинальних вен(см. раздел "Побочные реакции").
Гиперкалиемия
Препарат Ирина® Плюс содержит 3 мг прогестина дроспиренону, который имеет антиминералокортикоидни свойства, в том числе может вызывать гиперкалиемию у пациенток, которые принадлежат к группе повышенного риска. Указанное свойство дроспиренону аналогично действию спиронолактону в дозе 25 мг. Препарат Ирина® Плюс противопоказанный для применения пациенткам с заболеваниями, которые провоцируют развитие гиперкалиемии(например, нарушение функции почек, нарушения функции печенки и недостаточность коры надпочечников). У женщин, которые получают ежедневную длительную терапию хронических состояний или заболеваний препаратами, способными повышать уровень калия в сыворотке крови, необходимо на протяжении курса лечения контролировать сывороточную концентрацию калия. К лекарственным средствам, которые могут повышать уровень калия в сыворотке крови, принадлежат ингибиторы АПФ, антагонисты рецепторов ангиотензина ІІ, калийзберигаючи диуретики, калиевые добавки, гепарин, антагонисты альдостерону и НПЗП. Следует рассмотреть возможность осуществления мониторинга сывороточных концентраций калия у пациенток из группы повышенного риска, которые проходят сопутствующую долговременную терапию с применением мощного ингибитора цитохрома CYP3A4. Мощные ингибиторы CYP3A4 включают азольни противогрибковые препараты(например, кетоконазол, итраконазол, вориконазол), ингибиторы протеазы ВИЧ/ВГС(например, индинавир, боцепревир) и кларитромицин(см. раздел "Фармакологические свойства").
Рак молочной железы и репродуктивных органов
Женщинам, которые болеют или болели раньше раком молочной железы, не следует принимать препарат Ирина® Плюс, поскольку рак молочной железы - это гормонозалежна опухоль.
Существуют убедительные доказательства того, что КОК не повышают частоту развития рака молочных желез. Невзирая на то, что в отдельных исследованиях выдвигалось предположение, что КОК могут увеличивать частоту возникновения рака молочных желез, данные последних исследований не подтверждают этот факт.
Результаты некоторых исследований свидетельствуют, что применение КОК ассоциируется с ростом риска развития рака шейки матки или интраепителиальной неоплазии. Однако не достигнуто единственной мысли относительно того, насколько эти результаты могут быть предопределены отличиями в половом поведении и другими факторами.
Важнейшим фактором риска рака шейки матки является папиломавирусна инфекция человека.
Заболевание печенки
При появлении желтухи применения препарата Ирина® Плюс прекращают. У пациенток с нарушением функции печенки возможное нарушение метаболизма стероидных гормонов. При острых или хронических нарушениях функции печенки может возникнуть необходимость прекратить прием КОК, пока показатели функции печенки не вернутся к норме и будет исключена причинная связь с приемом КОК.
Возникновение аденомы печенки ассоциируется с применением КОК. За расчетами, этот риск представляет 3,3 случаи на 100000 женщин, которые принимают КОК. Разрыл аденомы печенки может иметь летальные последствия через внутрибрюшное кровотечение.
Исследования показали повышение риску развития печеночно-клеточного рака у лиц, которые применяют КОК в течение длительного времени(˃8 годы). Однако риск возникновения рака печенки у женщин, которые применяют КОК представляет менее 1 випадка на миллион лиц.
В одиночных случаях у женщин, которые применяют КОК, наблюдались доброкачественные, а еще реже - злокачественные опухоли печенки, которые в отдельных случаях приводили к опасному для жизни внутрибрюшному кровотечению. В случае возникновения жалоб на сильную боль в эпигастральном участке, увеличения печенки или признака внутрибрюшного кровотечения при дифференциальной диагностике следует учитывать возможность наличия опухоли печенки при применении КОК.
У женщин, которые имеют в анамнезе случаи холестаза, связанного с беременностью, возможное развитие холестаза, который ассоциируется с применением оральных контрацептивов. У женщин с холестазом, предопределенным КОК, в анамнезе могут развиваться рецидивы при повторном приложении КОК.
Риск повышения уровня печеночных ферментов при одновременном применении препаратов для лечения вирусного гепатита С
В ходе клинических исследований при участии пациентов, которые получали терапию для лечения вирусного гепатита С лекарственными средствами, которые содержат омбітасвір/паритапревір/рітонавір из или без добавления дасабувиру, повышения уровня АЛТ в свыше 5 раз выше верхнего предела нормы(ВМН), включая некоторые случаи повышения в свыше 20 раз выше ВМН, наблюдалось значительно чаще у женщин, которые применяли лекарственные средства, которые содержат етинилестрадиол, такие как КОК. Следует прекратить применение препарата Ирина® Плюс перед началом терапии комбинацией омбітасвір/паритапревір/рітонавір из/ без добавления дасабувиру(см. раздел "Противопоказания"). Возобновить применение препарата Ирина® Плюс можно приблизительно через 2 недели по завершению курса применения лекарственных средств для терапии вирусного гепатита С.
Повышение артериального давления
У женщин с хорошо контролируемой артериальной гипертензией следует отслеживать показатели артериального давления и прекратить применение препарата Ирина® Плюс при их значительном повышении. Женщинам с неконтролируемой артериальной гипертензией или гипертензией с сопутствующими другими сосудистыми заболеваниями не должны принимать КОК.
У женщин, которые принимали КОК, наблюдалось о повышении артериального давления, которое возникает чаще у женщин старшего возраста и при длительном применении препарата. Частота возникновения артериальной гипертензии растет с увеличением концентрации прогестина.
Заболевание желчного пузыря
Результаты исследований указывают на незначительное повышение относительного риска развития заболеваний желчного пузыря у женщин, которые применяют КОК.
Влияние на углеводный и липидный обмен
Женщины со склонностью к развитию сахарного диабета и пациентки, которые страдают на диабет, должны находиться под тщательным надзором во время применения препарата Ирина® Плюс. КОК могут вызывать дозозависимое снижение толерантности к глюкозе.
Для женщин с неконтролируемой дислипидемиею следует рассмотреть возможность использования альтернативных средств контрацепции. У незначительной части женщин на фоне применения КОК происходят неблагоприятные изменения липидного обмена.
У женщин с гипертриглицеридемией или наличием в семейном анамнезе этого расстройства при применении КОК повышается риск развития панкреатита.
Головная боль
Если у женщины, которая принимает препарат Ирина® Плюс, возникают головные боли, которые имеют рецидивный характер, являются стойкими или интенсивными, следует тщательным образом выучить случай и, в случае необходимости, отменить применение препарата Ирина® Плюс.
Увеличение частоты или тяжести мигреней на фоне применения КОК(что может быть предшественником цереброваскулярного расстройства) может быть основанием для немедленной отмены КОК.
Нерегулярные кровотечения
На фоне применения КОК у пациенток иногда возникают нерегулярные(прорывные или внутрицикличные) кровотечения и кровомазання, особенно в течение первых трех месяцев приема. В случае стойких кровотечений или появления кровотечения после предыдущего регулярного цикла следует обследовать женщину на наличие беременности и относительно злокачественных новообразований. Если патология и беременность исключена, нерегулярные кровотечения могут исчезнуть со временем или после перехода на другой КОК.
Данные десяти клинических исследований контрацептивной эффективности препарата Ирина® (N =3D 2467) показали, что количество женщин, которые применяли препарат Ирина® и у которых были незапланированные кровотечения, уменьшились с 12 % в цикле 2 до 6 % (цикл 13). 25 пациентки с 3009 в ходе исследований применения препарата Ирина® и препарату Ирина® Плюс(<1 %) прекратили участие в исследованиях через жалобы на кровотечении. Жалобы описаны как метрорагия, влагалищное кровотечение, меноррагия, аномальные кровотечения отмены и менометроррагия.
Среднее количество дней кровотечения в большинстве пациенток(86-88 %) представляли 4-7 дни. У пациенток, которые применяли препарат Ирина® Плюс, может наблюдаться отсутствие кровотечения отмены, даже если они не беременные. Согласно записям пациенток в дневниках, проанализированным в ходе исследований контрацептивной эффективности препарата Ирина®, в течение 2-13 циклов, от 6 до 10 % имели циклы без кровотечений отмены. У некоторых женщин может встречаться аменорея или олигоменорея, вызванная приемом противозачаточных таблеток, особенно если такие расстройства отмечались раньше.
При отсутствии кровотечения отмены следует рассмотреть возможность наличия беременности. Если пациентка не придерживалась назначенного режима применения препарата(пропустила прием одной или больше таблетки, которые содержали гормоны, или начала принимать их на день позже, чем должна была бы начать), при первом отсутствии кровотечения отмены необходимо учитывать вероятность беременности и принять необходимые диагностические меры. Если пациентка придерживалась назначенного режима применения препарата и у нее отсутствуют два кровотечения отмены подряд, необходимо исключить беременность.
Применение КОК перед беременностью или на ранних сроках беременности
Расширенные эпидемиологические исследования не показали ни одного повышения риску появления врожденных пороков развития плода у женщин, которые принимали оральные контрацептивы к беременности. В исследованиях также не выявлено признаков тератогенного эффекта, в том числе не определенно аномалий развития сердца и дефектов уменьшения конечностей, при неумышленном приложении женщинами препарата на ранних сроках беременности. При подтверждении беременности нужно прекратить прием препарата Ирина® Плюс та начать применение витаминных добавок для беременных с содержимым фолатов.
Оральные контрацептивы не следует применять для индуктирования кровотечению отмены как тест на беременность(см. раздел "Способ применения и дозы").
Депрессия
Женщины с депрессией в анамнезе должны находиться под тщательным надзором; при рецидивах депрессии тяжелой степени препарат Ирина® Плюс следует отменить.
Влияние на результаты лабораторных исследований
Применение контрацептивных стероидов может влиять на результаты определенных лабораторных анализов, в частности это касается факторов коагуляции, уровня липидов, толерантности к глюкозе и связывающим белкам. Женщины, которые получают заместительную терапию гормонами щитообразной железы, могут нуждаться высших доз тиреоидного гормона, поскольку на фоне применения КОК сывороточная концентрация глобулина, который связывает тиреоидные гормоны, растет. Дроспіренон увеличивает активность ренину и альдостерону в плазме крови, которая индуктируется его умеренной антиминералокортикоидной активностью. Фолаты могут скрывать дефицит витамина В12.
Мониторинг
Женщины, которые принимают КОК, должны ежегодно посещать своего врача с целью контроля артериального давления и проведения других необходимых обследований.
Другие состояния
У женщин с наследственным ангионевротическим отеком экзогенные естрогени могут индуктировать или усиливать симптомы ангионевротического отека.
В одиночных случаях может развиваться хлоазма, особенно у женщин, которые раньше имели хлоазму беременных. Женщины со склонностью к появлению хлоазми должны избегать влияния солнечного или ультрафиолетового излучения во время приема КОК.
Случаи болезни Крона и язвенного колита также наблюдались во время применения КОК.
Каждая таблетка оранжевого цвета препарата содержит 45 мг лактозы, каждая таблетка светло-оранжевого цвета содержит 48 мг лактозы. При наличии редких наследственных состояний непереносимости галактозы, дефицита лактазы Лаппа или мальабсорбции глюкозы-галактозы, в случае пребывания на безлактозной диете следует учитывать отмеченное количество лактозы.
Применение в период беременности или кормления груддю.
Беременность. У женщин, которые неумышленно принимали КОК на ранних сроках беременности, риск возникновения дефектов развития у младенцев повышается незначительно или вообще не повышается. Эпидемиологические исследования и результаты анализов цели не выявили увеличения риска возникновения врожденных пороков развития половых и других органов(в том числе пороков сердца и дефектов уменьшения конечностей) после приема низькодозових КОК перед зачатием или на ранних сроках беременности.
Применение КОК с целью стимулирования кровотечения отмены не следует использовать в качестве тест на беременность. Не следует принимать КОК во время беременности для лечения угрозы выкидыша или повторных выкидышей.
Женщины, которые не кормят груддю, могут начинать применение КОК не раньше чем через 4 недели после родов.
Женщины, которые кормят груддю. Женщинам, которые кормят груддю, следует порекомендовать в случае возможности применять другие средства контрацепции к прекращению грудного кормления. КОК с содержимым естрогенив могут снижать продуцирование молока у женщин, которые кормят груддю. После налаживания грудного выкармливания такое притеснение продуцирования является маловероятным, однако у отдельных женщин оно может возникать в любое время. Стероидные гормоны, которые входят в состав оральных контрацептивов, или их метаболити в незначительных количествах проникают в грудное молоко.
После перорального применения таблеток с содержимым 3 мг дроспиренону и 0,03 мг етинилестрадиолу(препарат Ирина®), около 0,02 % дозы дроспиренону было выявлено на протяжении 24 часов в грудном молоке женщин после родов. Таким образом, максимальная суточная доза, которую получает младенец, представляет около 0,003 мг дроспиренону.
Имеющиеся результаты исследований указывают на отсутствие неблагоприятного влияния фолатов на младенцев, которые находятся на грудном кормлении.
Способность влиять на скорость реакции при управлении автотранспортом или с механизмами.
Не проводили исследований относительно влияния на способность руководить автотранспортом или механизмами. Не сообщалось о влиянии на способность руководить автотранспортом или работать с механизмами у женщин, которые принимают комбинированные оральные контрацептивы.
Способ применения и дозы
Как принимать препарат Ирина® Плюс
Принимают по 1 таблетке перорально в одно и то же время каждого дня. При пропуске приема таблеток или неправильном применении препарата эффективность может снижаться.
Для достижения максимального контрацептивного эффекта препарат Ирина® Плюс следует применять согласно назначению и с соблюдением указаний, отмеченных на блистерний упаковке. В случае пропуска приема 1 таблетки ее следует принять как можно быстрее.
Как начать применение препарата Ирина® Плюс
Начинать прием препарата Ирина® Плюс необходимо в первый день менструального цикла(начало в 1-й день цикла) или в первое воскресенье после начала менструального цикла(начало в воскресенье).
· Начало в 1-й день цикла
В течение первого цикла применения препарата Ирина® Плюс женщина должна принимать по
1 оранжевой таблетке препарата ежедневно, начиная с 1-го дня менструального цикла(первый день менструации - это 1-й день циклу). Пациентка должна принимать по 1 оранжевой таблетке препарата Ирина® Плюс на день в течение 21 дня подряд, после чего на протяжении 22-28 дней цикла принимать по 1 светло-оранжевой таблетке на сутки. Препарат Ирина® Плюс следует принимать согласно указаниям, которые содержатся на упаковке, в одно и то же время каждого дня, желательно после ужина или перед сном, запивая небольшим количеством жидкости, в случае необходимости. Прием препарата Ирина® Плюс не зависит от употребления еды. В случае первого приема таблеток Ирина® Плюс не в 1-й день менструального цикла, а позже, контрацептивная эффективность препарата наступает только после первых 7 дни его непрерывного приложения. В таком случае необходимо дополнительное использование негормональных средств контрацепции в течение первых 7 дни приему препарата Ирина® Плюс. Следует учитывать возможность наступления овуляции и оплодотворения к началу применения препарата.
· Начало в воскресенье
В течение первого цикла применения препарата Ирина® Плюс женщина должна принимать по
1 оранжевой таблетке Ирина® Плюс ежедневно в течение 21 дня подряд, после чего на протяжении 22-28 дней цикла принимать по 1 светло-оранжевой таблетке на сутки. Препарат Ирина® Плюс следует принимать согласно указаниям, отмеченным на упаковке, в одно и то же время каждого дня, желательно после ужина или перед сном, запивая небольшим количеством жидкости, в случае необходимости. Прием препарата Ирина® Плюс не зависит от употребления еды. Контрацептивная эффективность препарата Ирина® Плюс наступает не раньше чем через 7 дни его непрерывного приложения. Необходимое дополнительное применение негормональных средств контрацепции в течение первых 7 дни приему препарата Ирина® Плюс. Следует учитывать возможность наступления овуляции и оплодотворения к началу применения препарата.
Пациентка должна начинать второй и все следующие 28-дневные курсы приема препарата Ирина® Плюс в тот же день недели, что и первый курс и следовать одинаковой схеме применения. Прием оранжевых таблеток начинать на следующий день после приема последней светло-оранжевой таблетки, которая содержит фолат, независимо от того, наступила менструация или еще ожидается. Каждый раз, когда следующий курс препарата Ирина® Плюс начинается не следующего дня после приема последней светло-оранжевой таблетки, а позже, пациентка должна пользоваться другим методом контрацепции, пока период приема оранжевых таблеток препарата Ирина® Плюс не будет представлять 7 дни подряд.
Переход из других противозачаточных таблеток
При переходе из других противозачаточных таблеток применения препарата Ирина® Плюс начинать в день, когда необходимо было бы начать прием таблеток с новой упаковки предыдущего орального контрацептива.
Переход из другого метода контрацепции, кроме противозачаточных таблеток
При переходе из трансдермального пластыря или влагалищного кольца препарат Ирина® Плюс начинать принимать в день наступление срока следующего применения отмеченных средств контрацепции. При переходе из инъекционных контрацептивов препарат Ирина® Плюс начинают применять в день, когда должна была бы быть проведена следующая инъекция. При переходе из внутриматочного средства или имплантата препарат Ирина® Плюс начинать принимать в день их удаление.
Кровотечение отмены обычно наступает на протяжении 3 дней после приема последней оранжевой таблетки. В случае появления кровомазання или прорывного кровотечения во время приема препарата Ирина® Плюс необходимое продолжение его приложения согласно режиму, вышеприведенному. Такие кровотечения обычно являются временными и не имеют клинического значения, однако в случае стойкого или длительного кровотечения женщину должен осмотреть врач.
Невзирая на то, что частота беременности при применении препарата Ирина® Плюс согласно инструкции является низкой, в случае отсутствия кровотечения отмены следует учитывать возможность беременности. В случае несоблюдения пациенткой назначенного режима применения(пропуск приема 1 или больше активные таблетки или начало их приложения не в нужный день, а позже) при первом отсутствии кровотечения отмены необходимо учитывать возможность беременности и принять соответствующие диагностические меры. Если пациентка придерживалась назначенного режима и у нее отсутствуют два кровотечения подряд, следует исключить наличие беременности. При подтверждении беременности применения препарата Ирина® Плюс нужно прекратить.
Риск наступления беременности растет с каждой пропущенной активной таблеткой оранжевого цвета.
Что делать в случае пропуска приема таблетки
Пропущен прием 1 оранжевой таблетки в упаковке.
Принять таблетку, как только пациентка вспомнит о пропуске. Принимать следующую таблетку в обычное время. Это значит, что в таком случае возможный прием 2 таблеток в один день.
В случае полового акта нет потребности в дополнительных методах контрацепции.
Пропущен прием 2 оранжевых таблеток в ряду "Неделя 1" или "Неделя 2" блистерной упаковки.
Принять 2 таблетки в день, в который упомянуто о пропуске, и 2 таблетках на следующий день.
Дальше принимать по 1 таблетке на день до окончания упаковки.
Если в следующие 7 дни после возобновления приема таблеток состоится половой акт, следует учитывать возможность наступления беременности. Следует использовать дополнительный метод контрацепции(например, презерватив и спермицид) в течение этих 7 дни.
Пропущен прием 2 оранжевых таблеток в ряду "Неделя 3" блистерной упаковки.
Если применение препарата Ирина® Плюс было начато в 1-й день цикла, прекратить прием препарата из данной упаковки и начать прием таблеток с новой упаковки в тот же день.
Если применение препарата Ирина® Плюс было начато в воскресенье, продолжать прием по 1 таблетке на день до воскресенья. В воскресенье прекратить прием препарата из данной упаковки и начать прием таблеток с новой упаковки в тот же день.
Если в следующие 7 дни после возобновления приема таблеток состоится половой акт, следует учитывать возможность наступления беременности. Следует использовать дополнительный метод контрацепции(например, презерватив и спермицид) в течение этих 7 дни.
Ожидается, что в данном цикле будет отсутствовать кровотечение отмены. Однако при условии отсутствия двух кровотечений отмены подряд в двух циклах необходимо исключить наличие беременности.
Пропущен прием 3 или больше оранжевые таблетки в ряду в течение любой недели
Если применение препарата Ирина® Плюс было начато в 1-й день цикла, следует прекратить прием препарата из данной упаковки и начать прием таблеток с новой упаковки в тот же день.
Если применение препарата Ирина® Плюс было начато в воскресенье, продолжать прием по 1 таблетке на день до воскресенья. В воскресенье прекратить прием препарата из данной упаковки и начать прием таблеток с новой упаковки в тот же день.
Если в следующие 7 дни после возобновления приема таблеток состоится половой акт, следует учитывать возможность наступления беременности. Следует использовать дополнительный метод контрацепции(например, презерватив и спермицид) в течение этих 7 дни.
Ожидается, что в данном цикле будет отсутствовать кровотечение отмены. Однако при условии отсутствия двух кровотечений отмены подряд в двух циклах необходимо исключить наличие беременности.
Пропущен прием любой из 7 светло-оранжевых таблеток в ряду "Неделя 4"
Изъять пропущенную таблетку из блистерной упаковки.
Продолжать прием по 1 таблетке на день до окончания таблеток в блистерний упаковке.
Потребности в дополнительных методах контрацепции нет.
Если, невзирая на вышеприведенные рекомендации, пациентка не уверена в том, каким образом действовать в случае пропуска приема таблеток
Использовать дополнительный метод контрацепции(например, презерватив и спермицид) во время полового акта.
Обратиться за консультацией к врачу и продолжать прием препарата по 1 активной оранжевой таблетке 1 раз в день, если не получено других рекомендаций.
Если прорывное кровотечение появляется после пропуска приема таблеток, обычно это является временным явлением и не имеет последствий. В случае пропуска пациенткой приема одной или больше светло-оранжевые таблетки контрацептивная защита хранится при условии, что в нужный день она начнет новый курс приема таблеток оранжевого цвета.
Через повышенный риск развития тромбоэмболии женщинам в послеродовой период, которые не кормят груддю, и женщинам после аборта во втором триместре беременности необходимо начинать прием препарата Ирина® Плюс не раньше чем через 4 недели после родов. Если женщина начинает применение препарата Ирина® Плюс после родов и еще не имела менструального кровотечения, следует проверить ее на наличие беременности и поинформировать о необходимости использование дополнительного метода контрацепции, пока период непрерывного приема таблеток Ирина® Плюс не будет представлять 7 дни.
Рекомендации в случае расстройств со стороны желудочно-кишечного тракта.
В случае тяжелого блюет или диареи возможно неполное всасывание препарата. В таком случае следует применять дополнительные средства контрацепции.
Если блюет началось на протяжении 3-4 часов после приема таблетки Ирина® Плюс, эта ситуация похожа на пропуск приема препарата, потому следует придерживаться рекомендаций на случай пропуска приема таблеток.
Фолаты.
Рабочая группа США из профилактических мер рекомендует женщинам репродуктивного возраста ежедневно дополнять свой рацион по крайней мере 0,4 мг(400 мкг) фоллиевой кислоты. Перед назначением препарата Ирина® Плюс необходимо узнать, или принимает женщина фолаты, и учитывать это. Если применение препарата Ирина® Плюс прекращается через наступление беременности, следует обеспечить продолжение получения фолатов женщиной.
Применение лицам пожилого возраста.
Применение препарата Ирина® Плюс у женщин постклимактерического возраста не исследовалось; препарат не назначать пациенткам этой возрастной группы.
Пациентки с нарушением функции почек.
Препарат Ирина® Плюс противопоказанный для применения пациенткам с нарушением функции почек.
Влияние нарушения функции почек на фармакокинетични свойства дроспиренону(в дозе 3 мг на сутки в течение 14 дней) и влияние дроспиренону на концентрацию калия в сыворотке изучалось на трех отдельных группах женщин(n =3D 28, возраст 30-65). Все лица находились на диете с низким потреблением калия. В течение исследования 7 лица продолжали принимать калийзберигаючи препараты для лечения их основного заболевания. На 14-й день терапии дроспиреноном(равновесное состояние) сывороточные концентрации дроспиренону в группе с клиренсом креатинина
50-79 мл/хв были аналогичными концентрациям в группе с клиренсом креатинина ≥ 80 мл/мин. У лиц с клиренсом креатинина 30-49 мл/хв сывороточные концентрации дроспиренону были в среднем на 37 % выше, чем у пациенток из контрольной группы. При лечении дроспиреноном не отмечено ни одного клинически значимого влияния на уровень калия в сыворотке крови. Невзирая на то, что в исследовании не наблюдалось гиперкалиемии, в 5 из 7 лиц, которые продолжали применение калийзберигаючих препаратов во время исследования, средняя сывороточная концентрация калия повысилась до 0,33 мекв/л(см. разделы "Противопоказания" и "Особенности применения").
Пациентки с нарушением функции печенки.
Препарат Ирина® Плюс противопоказанный для применения пациенткам с болезнями печенки.
Средняя экспозиция дроспиренону у женщин с нарушением функции печенки умеренной степени является почти втрое выше экспозиции у женщин с нормальной функцией печенки. Препарат Ирина® Плюс не исследовался у женщин с тяжелыми нарушениями функции печенки(см. разделы "Противопоказания" и "Особенности применения").
Расовые отличия.
Не отмечено клинически значимых отличий фармакокинетичних свойств дроспиренону или етинилестрадиолу у японок и представительниц европеоидной расы(возрастом 25-35 годы) при ежедневном применении препарата с содержимым 3 мг дроспиренону/0,02 мг етинилестрадиолу в течение 21 суток. Специальных дослидженнь относительно особенностей в других этнических группах не проводили.
Деть.
Безопасность и эффективность применения препарата Ирина® Плюс установлены для женщин репродуктивного возраста. Ожидается, что препарат обнаруживает аналогичную эффективность у подростков постпубертатного возраста, до 18 лет и у пациенток в возрасте от 18 лет. Это лекарственное средство не назначать к началу менструаций.
Передозировка
Сообщение о серьезных неблагоприятных последствиях передозировки, в том числе при приеме препарата детьми, отсутствующие. Передозировка может приводить к появлению у женщин кровотечения отмены и тошноты.
Дроспіренон - это аналог спиронолактону, что имеет антиминералокортикоидни свойства. При передозировке следует осуществлять мониторинг концентрации калия и натрия в сыворотке крови и отслеживать признаки метаболического ацидоза.
Левомефолат кальция в дозе 17 мг на сутки(что в 37 разы выше, чем доза левомефолату кальция в препарате Ирина® Плюс) хорошо переносился при длительном лечении до 12 недель.
Побочные реакции
Серьезные побочные реакции, отмеченные при применении КОК, описаны в других разделах этой инструкции для медицинского приложения:
- серьезные сердечно-сосудистые расстройства и инсульт(см. раздел "Особенности применения");
- сосудистые события(см. раздел "Особенности применения");
- заболевание печенки(см. раздел "Особенности применения").
Побочные реакции, которые часто наблюдаются у женщин, которые применяют КОК, :
- нерегулярные маточные кровотечения;
- тошнота;
- болезненность молочных желез;
- головная боль.
Даны, полученные в ходе клинических исследований
Поскольку условия проведения клинических исследований широко отличаются, частота побочных реакций, отмеченная в одних исследованиях, не может непосредственно сравниваться с частотой, зарегистрированной в других клинических исследованиях, и может не отображать реальную частоту, которая встречается на практике.
Клинические исследования из изучения контрацептивного действия и обеспечения фолатного статуса
Данные отображают опыт применения препарата "Ирина®" (3 мг дроспиренон/0,03 мг етинилестрадиол) в адекватном контролируемом исследовании контрацептивного действия(N =3D 2837) и обеспечения фолатного статуса(N =3D 172).
Относительно контрацептивного действия(N =3D 326) в США проведено мультицентровое открытое исследование участием здоровых женщин в возрасте от 18 до 35 лет, которые применяли препарат "Ирина®" до 13 циклов. Второе регистрационное клиническое исследование(N =3D 442) - мультицентровое, рандомизированное, открыто сравнительное Европейское исследование применения препарата "Ирина®" сравнимо из 0,150 мг дезогестрелу/0,03 мг етинилестрадиолу у здоровых женщин в возрасте от 17 до 40 лет, которые получали препараты до 26 циклов. Для исследования первичной эффективности с применением препарата Ирина® Плюс для обеспечения фолатного статуса было проведено рандомизированное одинцентровое Европейское исследование при участии 172 здоровых женщин в возрасте от 18 до 40 лет для сравнения фармакодинамичних эффектов препарата "Ирина®" + 0,451 мг левомефолату кальция и совместимого применения препарата "Ирина®" с фоллиевой кислотой в течение 24 недель лечения со следующим 20-недельным открытым исследованием применения препарата "Ирина®".
Побочные реакции, отмеченные во время применения за двумя показаниями, сбегаются и приводятся с указанием частоты в соответствии с объединенными массивами данных. Самыми распространенными побочными реакциями(≥ 2 %) были: предменструальний синдром(12,4 %), головная боль/мигрень(10,3 %), болезненность/чувствительность молочных желез/ощущения дискомфорта в молочных железах(8,1 %), тошнота/блюющего(4,4 %), изменения настроения(депрессия, депрессивное состояние, раздраженность, изменения настроения, изменения настроения и аффективная лабильность(2,3 %)), абдоминальный біль/дискомфорт/ болезненность(2,2 %).
Побочные реакции(≥1%), которые требовали прекращения участия в исследованиях
Клинические исследования из изучения контрацептивного действия. Из 2837 женщин 6,7 % прекратили участие в исследованиях через побочные реакции, самыми распространенными из которых были головные боли/мигрень(1,5 %).
Клинические исследования из изучения эффективности добавления фолатов. Не наблюдались реакции, которые приводили к прекращению участия в исследованиях.
Серьезные побочные реакции
Клинические исследования из изучения контрацептивного действия : депрессия, легочная эмболия, токсичная кожная сыпь, лейомиома матки.
Клиническое исследование из изучения эффективности добавления фолатов : не отмечено никаких серьезных побочных реакций.
Опыт писляреестрацийного приложения
Приведены дальше побочные реакции были выявлены во время писляреестрацийного применения препарата "Ирина®". Поскольку сообщения об этих реакциях посылали добровольно и они касались популяций неопределенного размера, не всегда возможно достоверно оценить их частоту или установить причинную связь с применением препарата.
Со стороны сосудов: венозные и артериальные тромбоэмболические явления(в том числе легочная эмболия, тромбоз глубоких вен, интракардиальний тромбоз, тромбоз интракраниального венозного синуса, тромбоз сагитальной пазухи твердой мозговой оболочки, тромбоз вен сетчатки, инфаркт миокарда и инсульт), артериальная гипертензия.
Гепатобіліарні расстройства: заболевание желчного пузыря.
Со стороны иммунной системы: повышенная чувствительность.
Со стороны питания и нарушения обмена веществ : гиперкалиемия.
Со стороны кожи и подкожной основы : хлоазма.
Срок пригодности
36 месяцы.
Условия хранения
Хранить в недоступном для детей месте при температуре не выше 25° С.
Упаковка
Блистер с 28 таблетками, покрытыми оболочкой, и календарной шкалой в картонной пачке.
Категория отпуска
За рецептом.
Производитель
Байер АГ / Bayer AG.
Местонахождение производителя и его адрес места осуществления деятельности
Мюллєрштрассе 178, 13353, Берлин, Германия / Mullerstrasse 178, 13353, Berlin, Germany.
Другие медикаменты этого же производителя
Форма: крем 0,1 % по 5 г или 15 г в тубе; по 1 тубе в картонной коробке
Форма: раствор для инъекций, 1 ммоль/мл, по 5 мл, или по 7,5 мл, или по 10 мл в стеклянном шприце, вложенном в прозрачную пластиковую коробку, закрытую бумагой; по 5 шприцы в картоний коробке; по 5 мл, или по 7,5 мл, или по 10 мл в пластиковом шприце, вложенном в прозрачную пластиковую коробку, закрытую полиэтиленом; по 5 шприцы в картоний коробке
Форма: таблетки, покрытые оболочкой, по 21 таблетке в блистере с календарной шкалой; по 1 блистеру в пачке
Форма: таблетки, покрытые пленочной оболочкой, по 1,5 мг № 42: по 21 таблетке в блистере; по 2 блистеры в картонной пачке; № 84: по 21 таблетке в блистере; по 4 блистеры в картонной пачке
Форма: таблетки, покрытые пленочной оболочкой, по 3 мг + таблетки, покрытые пленочной оболочкой, по 1 мг + таблетки, покрытые пленочной оболочкой, 3 мг/2 мг + таблетки, покрытые пленочной оболочкой, 2 мг/2 мг + таблетки, покрытые пленочной оболочкой(плацебо); № 28: 2 темно-желтые таблетки + 5 красные таблетки + 17 свитло-жовтих таблетки + 2 темно-красных таблеток + 2 белые таблетки плацебо в блистере; по 1 блистеру в картонном кошельке