Релвар™ Еллипта
Регистрационный номер: UA/14564/01/01
- Cклад
- Клинические характеристики
- Показание
- Противопоказание
- Особенности применения
- Способ применения и дозы
- 1 Прочитать перед началом применения
- Счетчик доз
- Крышка
- 2 Как подготовить дозу
- 3 Как делать ингаляцию препарата
- 4 Закрыть ингалятор и прополоскать рот
- Передозировка
- Побочные реакции
- Классы систем органов
- Нежелательная реакция
- Частота
- Упаковка
Импортёр: ГлаксоСмитКляйн Экспорт Лимитед
Страна: Великая БританияАдреса импортёра: 980 Грейт Уест Роуд, Брентфорд, Миддлсекс, TW8 9GS, Большая Британiя
Форма
порошок для ингаляций, дозированный по 184 мкг/22 мкг/дозу по 14 или 30 дозы в порошковом ингаляторе № 1
Состав
1 доза, которые доставляются, содержит 184 мкг флютиказону фуроату и 22 мкг вилантеролу(в форме трифенатату); это отвечает предварительно распределенной дозе 200 мкг флютиказону фуроату и 25 мкг вилантеролу(в форме трифенатату)
Виробники препарату «Релвар™ Еллипта»
Страна производителя: Великая Британия
Адрес производителя: Прайори Стрит, Веа, Хертфордшир, SG12 0DJ, Великая Британия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
РЕЛВАР™ ЕЛЛІПТА
(RELVAR™ ELLIPTA)
Cклад
действующие вещества: флютиказону фуроат, вилантерол;
1 доза, которые доставляются, содержит 184 мкг флютиказону фуроату и 22 мкг вилантеролу(в форме трифенатату);
Это отвечает предварительно отмеряемой дозе 200 мкг флютиказону фуроату и 25 мкг вилантеролу(в форме трифенатату);
вспомогательные вещества: лактоза, моногидрат; магнию стеарат.
Врачебная форма. Порошок для ингаляций.Основные физико-химические свойства: белый порошок в светло-сером ингаляторе с блекло-синим колпачком распылителя и дозатором.
Фармакотерапевтична группа. Лекарственные средства, которые применяются при обструктивных заболеваниях дыхательных путей. Адренергические препараты для ингаляционного приложения.
Код АТХ R03A K10.
Фармакологические свойства.
Фармакодинамика.
Механизм действия
Флютиказону фуроат и вилантерол представляют два класса препаратов(синтетический кортикостероид и селективный агонист бета2-рецепторів длительного действия).
Фармакодинамічні эффекты
Флютиказону фуроат
Флютиказону фуроат - это синтетический трехфтористый кортикостероид с мощным противовоспалительным действием. Точный механизм, с помощью которого флютиказону фуроат влияет на симптомы астмы и ХОЗЛ, неизвестен. Кортикостероиды показали широкий диапазон действий на разнообразные типы клеток(в частности на эозинофилы, макрофаги, лимфоциты) и медиаторы(например на цитокины и хемокини, привлеченные к воспалению).
Вілантеролу трифенатат
Вілантеролу трифенатат - это селективный агонист бета2-адренергічних рецепторов длительного действия(ТДБА).
Фармакологические эффекты агонистов бета2-адренорецепторів, включая вилантеролу трифенатат, по меньшей мере частично связаны со стимуляцией внутриклеточной аденилатциклазы, фермента, который катализирует превращение аденозинтрифосфата(АТФ) к циклическому, 3',5 '- аденозинмонофосфату(циклический АМФ). Повышены уровни циклического АМФ вызывают расслабление гладких мышц бронхов и подавляют выделение медиаторов реакции гиперчувствительности немедленного типа из клеток, особенно из лаброцитив.
Между кортикостероидами и ТДБА возникают молекулярные взаимодействия, с помощью чего стероиды активируют ген бета2-рецептора, увеличивая количество рецепторов и их чувствительность, а ТДБА готовят глюкокортикоидни рецепторы к стероидозалежной активации и улучшают клеточную ядерную транслокацию. Эти синергичные взаимодействия отображаются в улучшенной противовоспалительной активности, которая была показана in vitro и in vivo в ряде клеток воспаления, связанных с патофизиологией астмы и ХОЗЛ. Исследование биопсии дыхательных путей при применении флютиказону фуроата и вилантеролу также показали синергичное действие между кортикостероидами и ТДБА, которая возникает в клинических дозах препаратов у пациентов из ХОЗЛ.
Фармакокинетика.
Абсорбция. Абсолютная биодоступность флютиказону фуроата и вилантеролу при ингаляции в виде флютиказону фуроата/вилантеролу сложила в среднем 15,2% и 27,3% соответственно. Пероральная биодоступность флютиказону фуроата и вилантеролу была низкой, в среднем 1,26% и < 2% соответственно. Принимая во внимание эту низкую пероральную биодоступность, системное влияние флютиказону фуроата и вилантеролу после ингаляционного приложения преимущественно связан со всасыванием ингалеваной части дозы, которая попала к легким.
Распределение. После внутривенного введения флютиказону фуроат и вилантерол широко распределяются, средний объем распределения в равновесном состоянии 661 л и 165 л соответственно.
Флютиказону фуроат и вилантерол имеют слабую связь с эритроцитами. Связывание флютиказону фуроата и вилантеролу с белками плазмы in vitro в плазме крови человека было высоким, в среднем > 99,6% и 93,9% соответственно. У пациентов с почечной или печеночной недостаточностью связывания с белками плазмы in vitro не уменьшалось.
Флютиказону фуроат и вилантерол являются субстратами для P- гликопротеина(P - gp), однако маловероятно, что одновременное применение флютиказону фуроата/вилантеролу с ингибиторами P - gp изменит системное влияние флютиказону фуроата/вилантеролу, поскольку они являются молекулами, которые хорошо всасываются.
Биотрансформация. На основе данных in vitro, основные пути метаболизма флютиказону фуроата и вилантеролу у человека опосредствуют преимущественно CYP3A4.
Флютиказону фуроат преимущественно метаболизуеться путем гидролиза S- фторметил-карботиоатной группы к метаболитив с существенно уменьшенной кортикостероидной активностью. Вілантерол преимущественно метаболизуеться O‑дезалкилуванням к метаболитив из существенно уменьшенной b1 - и b2- агонистической активностью.
Выведение. После перорального приложения флютиказону фуроат выводится у людей преимущественно путем метаболизма, при этом метаболити почти полностью выделяются с калом, а < 1% возобновленной радиоактивной дозы выделяется с мочой.
После перорального применения вилантерол выводится преимущественно путем метаболизма с дальнейшим выделением метаболитив с мочой и калом на уровне приблизительно 70% и 30% радиоактивной дозы соответственно в исследовании с использованием меченых изотопов у человека. Ожидаемый период полувыведения вилантеролу из плазмы после одноразовой ингаляции флютиказону фуроата/вилантеролу в среднем представлял 2,5 часы. Эффективный период полувыведения для накопленного вилантеролу, определенный после ингаляции повторных доз вилантеролу по 25 мкг, равняется 16 часы у пациентов с астмой и 21,3 часы у пациентов из ХОЗЛ.
Деть. Для подростков(в возрасте от 12 лет) отсутствующие рекомендации относительно изменения дозы.
Фармакокинетика флютиказону фуроата/вилантеролу у пациентов в возрасте до 12 лет не исследовалась. Безопасность и эффективность флютиказону фуроата/вилантеролу для детей в возрасте до 12 лет не устанавливались.
Особенные группы пациентов
Пациенты пожилого возраста(> 65 годы)
Влияние возраста на фармакокинетику флютиказону фуроата и вилантеролу определялся в исследованиях фазы ІІІ у пациентов с ХОЗЛ и астмой. Не было доказательств влияния возраста(12-84 годы) на фармакокинетику флютиказону фуроата и вилантеролу у пациентов с астмой.
Для пациентов с астмой и пациентов из ХОЗЛ нет рекомендаций относительно изменения дозы.
Нарушение функции почек. Исследование клинической фармакологии флютиказону фуроата/вилантеролу показало, что почечная недостаточность тяжелой степени(клиренс креатинина < 30 мл/хв) не приводит к существенно более сильному влиянию флютиказону фуроата или вилантеролу, или более выраженных системных влияний кортикостероиду или бета2-агоніста сравнительно с соответствующими показателями при нормальной функции почек.
Нет необходимости у коррекции дозы для пациентов с почечной недостаточностью.
Влияние гемодиализа не исследовалось.
Нарушение функции печенки. После применения в течение 7 дней повторных доз флютиказону фуроата/вилантеролу отмечалось увеличение системного влияния флютиказону фуроата(до три раза, что определенно по показателю AUC(0-24)) у пациентов с печеночной недостаточностью(классификация по Чайлд-П'ю, класс A, B или C) в сравнении со здоровыми пациентами. Это увеличение системного влияния флютиказону фуроата у пациентов с печеночной недостаточностью средней степени тяжести(классификация по Чайлд-П'ю, класс В; флютиказону фуроат/вилантерол 184/22 мкг) связывалось с уменьшением сывороточного кортизола в среднем - 34% в сравнении со здоровыми добровольцами. Нормализованное за дозой системное влияние флютиказону фуроата было аналогичным у пациентов с печеночной недостаточностью средней и тяжелой степени(Чайлд-П'ю, класс B или C).
После применения в течение 7 дней повторных доз флютиказону фуроата/вилантеролу не отмечалось существенного увеличения системного влияния вилантеролу(Cmax и AUC) у пациентов с печеночной недостаточностью легкой, средней или тяжелой степени(Чайлд-П'ю, класс A, B или C).
Не было клинически значимых влияний комбинации флютиказону фуроата/вилантеролу на системные бета-адренергични эффекты(частота сердечных сокращений или уровень калия в сыворотке крови) у пациентов с печеночной недостаточностью легкой или средней степени(вилантерол, 22 мкг) или с тяжелой печеночной недостаточностью(вилантерол, 12,5 мкг) в сравнении со здоровыми добровольцами.
Другие особенные группы
В случае заболевания на астму показатель AUC(0-24) флютиказону фуроата у пациентов-выходцев из Восточной Азии, Японии и Юго-восточной Азии(12-13% пациентов) был в среднем на 33-53% более высоким в сравнении с другими группами пациентов. Однако не было доказательств большего системного влияния в этой популяции, ассоциируемого с большим влиянием на суточное выделение кортизолу с мочой. В среднем Cmax вилантеролу прогнозируется на уровне выше 220-287%, а AUC(0-24) сравнимая для пациентов азиатского происхождения и пациентов других групп по происхождению. При этом не было доказательств того, что это высшее значение Cmax вилантеролу приводило к клинически существенным влияниям на частоту сердечных сокращений.
Пол, масса тела и ІМТ
Не было доказательств влияния пола, массы тела и индекса массы тела(ІМТ) на фармакокинетику флютиказону фуроата на основе данных фармакокинетичного анализа в фазе ІІІ среди 1213 пациентов с астмой(712 женщин) и 1225 пациенты из ХОЗЛ(392 женщины).
Не было доказательств влияния пола, массы тела и ІМТ на фармакокинетику вилантеролу на основе данных популяционного фармакокинетичного анализа среди 856 пациентов с астмой(500 женщины) и 1091 пациент из ХОЗЛ(340 женщины).
Нет необходимости у коррекции дозы в зависимости от пола, массы тела или ІМТ.
Клинические характеристики
Показание
Астма
Регулярное лечение астмы у взрослых и детей в возрасте от 12 лет, если необходимое применение комбинированного лекарственного средства(бета2-агоніст длительного действия и ингаляционный кортикостероид) :
· пациенты, заболевание которых недостаточно контролируется ингаляционными кортикостероидами и ингаляционными бета2-агоністами короткого действия в случае необходимости.
Противопоказание
Повышенная чувствительность к действующим веществам или любым вспомогательным веществам препарата.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Клинически существенные взаимодействия препаратов, опосредствованные флютиказону фуроатом/вилантеролом в клинических дозах, считаются маловероятными в связи с низкими плазменными концентрациями, которые достигаются после ингаляции.
Блокаторы Беты
Блокаторы бета2-адренергічних рецепторов могут ослаблювати или делать антагонистичное действие к агонистам бета2-адренергічних рецепторов. Необходимо избегать одновременного применения неселективных и селективных блокаторов бета2-адренергічних рецепторов, если не будет убедительных причин их приложения.
Ингибиторы CYP3A4
Флютиказону фуроат и вилантерол быстро выводятся в результате расширенного эффекта первого прохождения, опосредствованного ферментом печенки CYP3A4.
Необходимо осторожность при одновременном приложении с сильными ингибиторами CYP3A4(например кетоконазолом, ритонавиром), поскольку существует возможность повышенного системного влияния флютиказону фуроата и вилантеролу, потому необходимо избегать одновременного приложения. Исследование взаимодействия повторной дозы ингибитора CYP3A4 было проведено при участии здоровых добровольцев с применением комбинации флютиказону фуроата/вилантеролу(184/22 мкг) и сильного ингибитора CYP3A4 кетоконазолу(400 мг). Одновременное приложение повышало среднюю AUC(0‑24) флютиказону фуроата и Cmax на 36% и 33% соответственно. Повышение влияния флютиказону фуроата связывалось с 27% уменьшением взвешенного среднего значения сывороточного кортизола за 0-24 часы. Одновременное приложение повышало среднюю AUC(0 - t) и Cmax вилантеролу на 65% и 22% соответственно. Повышение влияния вилантеролу не связывалось с повышением системного влияния на частоту сердечных сокращений, уровень калия в крови или длительность интервала QTcF, связанного с бета2-агоністом.
Ингибиторы P- гликопротеина
Флютиказону фуроат и вилантерол являются субстратами P- гликопротеина(P - gp). Исследование клинической фармакологии среди здоровых добровольцев с одновременным применением вилантеролу и сильнодействующего ингибитора P - gp, а также ингибитора CYP3A4 среднего действия верапамилу не показало любого существенного влияния на фармакокинетику вилантеролу. Исследование клинической фармакологии со специфическим ингибитором P - gp и флютиказону фуроатом не проводилось.
Симпатомиметики
Одновременное приложение с другими симпатомиметиками(как монотерапия или в составе комбинированной терапии) может повлечь возникновение нежелательных реакций на флютиказону фуроат/вилантерол. Препарат Релвар Елліпта нельзя применять одновременно с другими агонистами бета2-адренергічних рецепторов длительного действия или препаратами, которые содержат агонисты бета2-адренергічних рецепторов длительного действия.
Особенности применения
Ухудшение заболевания
Флютиказону фуроат/вилантерол нельзя применять для лечения острых симптомов астмы или острого нападения при ХОЗЛ, когда необходимы бронходилататори короткого действия. Повышенная частота применения бронходилататорив короткого действия для облегчения симптомов указывает на ухудшение контроля, и в таком случае пациента должен осмотреть врач.
Пациенты не должны прекращать лечения флютиказону фуроатом/вилантеролом при астме или ХОЗЛ без консультации с врачом, поскольку симптомы могут вернуться после прекращения лечения.
Во время лечения флютиказону фуроатом/вилантеролом могут возникнуть нежелательные явления и обострения, связанные с астмой. Пациентам необходимо рекомендовать продолжить лечение, но обратиться за консультацией к врачу, если симптомы астмы не контролируются или ухудшаются после ингаляции препаратом Релвар Елліпта.
Парадоксальный бронхоспазм
Парадоксальный бронхоспазм может возникать с внезапным быстрым увеличением свистящих хрипов после применения дозы. Это нуждается срочного лечения ингаляционными бронходилататорами короткого действия. Следует немедленно отменить препарат Релвар Елліпта, оценить состояние пациента и при необходимости назначить альтернативное лечение.
Влияние на сердечно-сосудистую систему
При применении симпатомиметиков, включая Релвар Елліпта, возможные нарушения со стороны сердечно-сосудистой системы, такие как сердечные аритмии, например суправентрикулярна тахикардия и экстрасистолия. Поэтому флютиказону фуроат/вилантерол необходимо с осторожностью применять пациентам с тяжелыми заболеваниями сердечно-сосудистой системы.
Пациенты с печеночной недостаточностью
Пациентам с печеночной недостаточностью средней и тяжелой степени необходимо применять дозу 92/22 мкг, проводя при этом контроль за возникновением системных нежелательных реакций, связанных с кортикостероидами(см. раздел "Фармакокинетика").
Системные эффекты кортикостероидов
Системные эффекты могут возникать при применении любого ингаляционного кортикостероида, особенно в высоких дозах, назначенных на длительное время. Эти эффекты возникают с намного меньшей достоверностью, чем при применении пероральных кортикостероидов. Возможные системные эффекты включают синдром Кушинга, кушингоидни признаки, притеснения надпочечников, уменьшения минеральной плотности костей, замедления роста у детей и подростков, катаракту и глаукому и реже - ряд физиологичных и поведенческих реакций, включая психомоторную гиперактивность, нарушение сна, тревожность, депрессию или агрессию(в частности у детей).
Флютиказону фуроат/вилантерол необходимо с осторожностью применять пациентам с туберкулезом легких и пациентам с хроническими или нелечеными инфекциями.
Гипергликемия
Сообщалось о повышении уровня глюкозы крови у пациентов с диабетом, и это необходимо учитывать при назначении препарата пациентам с сахарным диабетом в анамнезе.
Пневмония у пациентов из ХОЗЛ
Релвар Елліпта, 184/22 мкг, не показанный пациентам из ХОЗЛ. Нет дополнительной пользы от дозы 184/22 мкг в сравнении с дозой 92/22 мкг, а также существует потенциально повышенный риск возникновения пневмонии и системных побочных реакций, обусловленных кортикостероидами(см. раздел "Побочные реакции").
Повышение частоты возникновения пневмонии наблюдалось у пациентов из ХОЗЛ, которые получают флютиказону фуроат/вилантерол. Также была повышенная частота пневмоний, которые приводили к госпитализации. В некоторых случаях эти пневмонии имели летальное следствие(см. раздел "Побочные реакции"). Врачи должны принимать во внимание возможность развития пневмонии у пациентов из ХОЗЛ, поскольку клинические признаки таких инфекций частично сбегаются с симптомами обострения ХОЗЛ. Факторы риска возникновения пневмонии у пациентов из ХОЗЛ, которые получают флютиказону фуроат/вилантерол, включают курение, наличие пневмонии в анамнезе, индекс массы тела < 25 кг/м2 и прогнозируемый объем форсированного выдоха(ОФВ1) < 50%. Эти факторы должны браться к вниманию при назначении флютиказону фуроата/вилантеролу; необходимо пересмотреть лечение в случае возникновения пневмонии.
Пневмонии у пациентов с астмой наблюдались чаще при высших дозах. Частота возникновения пневмонии у пациентов с астмой, которые принимают флютиказону фуроат/вилантерол 184/22 мкг, была выше в сравнении с пациентами, которые принимают флютиказону фуроат/вилантерол 92/22 мкг или плацебо(см. раздел "Побочные реакции"). Факторов риска определенно не было.
Вспомогательные вещества
Пациенты с редкими наследственными состояниями, такими как непереносимость галактозы, недостаточность лактазы или нарушения всасывания глюкозы и галактозы, не должны применять этот препарат.
Применение в период беременности или кормления груддю.
Беременность. Исследования на животных показали репродуктивную токсичность при применении доз, которые не отвечают клинически значимым. Недостаточно данных относительно применения флютиказону фуроата и вилантеролу трифенатату беременным женщинам.
Применение флютиказону фуроата/вилантеролу беременным можно рассматривать лишь в случае, когда ожидаемая польза для женщины преобладает любой возможный риск для плода.
Период кормления груддю. Существует недостаточно информация относительно выделения флютиказону фуроату или вилантеролу трифенатату та/або их метаболитив с грудным молоком. Однако другие кортикостероиды и бета2-агоністи определялись в грудном молоке человека. Риск для детей, которые находятся на грудном выкармливании, не может быть исключен.
Необходимо принимать решение касательного прекращения грудного выкармливания или терапии флютиказону фуроатом/вилантеролом, принимая во внимание пользу грудного выкармливания для ребенка и пользу терапии для женщины.
Фертильность. Отсутствующие даны относительно влияния препарата на репродуктивную функцию у человека. Исследования на животных не показали влияния флютиказону фуроату/вилантеролу трифенатату на репродуктивную функцию.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Флютиказону фуроат или вилантерол не имеют влияния на способность руководить транспортным средством и использовать разные механизмы.
Способ применения и дозы
Дозы
Астма
Взрослые и дети в возрасте от 12 лет
Одна ингаляция препарата Релвар Елліпта 184/22 мкг один раз на сутки.
Обычно пациенты чувствуют улучшение функции легких в течение 15 минут после ингаляции.
Пациента следует проинформировать о том, что необходимо регулярное ежедневное приложение для поддержания контроля симптомов астмы и что применение необходимо продолжить даже в случае отсутствия симптомов.
Если в период между ингаляциями возникают симптомы, для немедленно их послабление необходимо применить бета2-агоніст короткого действия.
Начальную дозу препарата Релвар Елліпта 92/22 мкг следует рассматривать для взрослых и детей в возрасте от 12 лет, которым необходима низкая или средняя доза ингаляционных кортикостероидов в комбинации из бета2-агоністами длительного действия. Если пациенты недостаточно контролируются с помощью препарата Релвар Елліпта, 92/22 мкг, дозу можно увеличить до 184/22 мкг, что может обеспечить дополнительное улучшение контроля астмы.
Пациенты должны проходить регулярное обследование медицинскими работниками для того, чтобы доза флютиказону фуроата/вилантеролу, которую они получают, оставалась оптимальной и изменялась лишь по рекомендации врача. Дозу необходимо корректировать к самой низкой дозе, при которой поддерживается эффективный контроль симптомов.
Релвар Елліпта в дозировании 184/22 мкг назначают для взрослых и детей в возрасте от 12 лет, которым необходима высшая доза ингаляционных кортикостероидов в комбинации из бета2-агоністами длительного действия.
Максимальная рекомендованная доза препарата Релвар Елліпта 184/22 мкг один раз на сутки.
Пациенты с астмой должны получать дозирование препарата Релвар Елліпта, которое содержит дозу флютиказону фуроата(ФФ) в соответствии со степенью тяжести их заболевания. Медицинские работники, которые назначают препарат, должны знать о том, что у пациентов с астмой флютиказону фуроат(ФФ) 100 мкг один раз на сутки приблизительно эквивалентный флютиказону пропионату(ФП) 250 мкг два раза на сутки, тогда как ФФ 200 мкг один раз на сутки приблизительно эквивалентный 500 мкг ФП два раза на сутки.
Деть в возрасте до 12 лет
Безопасность и эффективность препарата Релвар Елліпта у детей в возрасте до 12 лет не изучались для лечения бронхиальной астмы.
Данные отсутствуют.
Особенные группы пациентов
Пациенты пожилого возраста(> 65 годы)
Нет необходимости у коррекции дозы для этой популяции(см. раздел "Фармакокинетика").
Пациенты с нарушением функции почек
Нет необходимости у коррекции дозы в этой популяции(см. раздел "Фармакокинетика").
Пациенты с нарушением функции печенки
Исследования при участии пациентов с печеночной недостаточностью легкой, средней и тяжелой степени показали повышение системного влияния флютиказону фуроата( Cmax и AUC) (см. раздел "Фармакокинетика").
Необходимо с осторожностью применять препарат пациентам с печеночной недостаточностью, поскольку они могут подлежать большему риску системных нежелательных реакций, связанных с кортикостероидами.
Для пациентов с печеночной недостаточностью средней или тяжелой степени максимальная доза представляет 92/22 мкг(см. раздел "Особенности применения"), применяя препарат Релвар Елліпта в соответствующей врачебной форме.
Способ применения
Релвар Елліпта предназначен лишь для ингаляций.
Его необходимо применять в одно и то же время каждого дня.
Окончательное решение относительно вечернего или утреннего приложения необходимо оставить на рассмотрение врача.
Если доза пропущена, следующую необходимо применить в обычное время следующего дня.
В случае хранения препарата в холодильнике необходимо, чтобы ингалятор находился при комнатной температуре в течение по меньшей мере одного часа перед применением.
После ингаляции пациенты должны прополоскать рот водой, не глотая ее.
Если ингалятор применяется впервые, нет необходимости проверять правильность его работы и любым особенным образом готовить его к применению. Необходимо придерживаться поэтапной инструкции.
Ингалятор Елліпта запакован в лоток, который содержит саше с десикантом для уменьшения содержимому влаги. После открытия саше с десикантом необходимо утилизировать.
Когда ингалятор вынимается из лотка, он будет находиться в закрытом положении. Пациента следует проинформовати, что нельзя открывать лоток с ингалятором, пока пациент не будет готов к ингаляции дозы.
Дата конечного приложения должна быть вписана пациентом в специально отведенном месте, обозначенном "Не использовать потом, :". Дата конечного приложения представляет 6 недели из даты открытия лотка с ингалятором. Не применять ингалятор потом дать конечного приложения. После первого открытия лоток можно выбросить.
Поэтапные инструкции, нижеприведенные для ингалятора Елліпта, который содержит 30 дозы, также применяются для ингалятора Елліпта, который содержит 14 дозы.
Инструкции из использования ингалятора(рис 1)
1 Прочитать перед началом применения
Если крышка ингалятора открывается и закрывается без ингаляции препарата, доза будет потеряна. Потерянная доза будет надежно храниться в ингаляторе, но уже не будет доступна для ингаляции.
Нельзя случайно применить избыточную или двойную дозу препарата за одну ингаляцию.
|
|
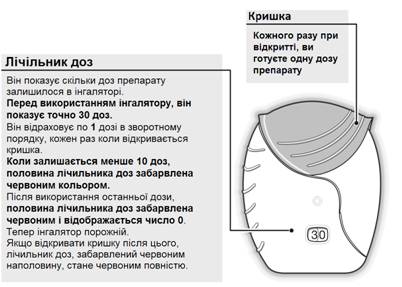 Рис. 1
Рис. 1
2 Как подготовить дозу
Открыть крышку, когда будет готовность к применению дозы. Не стряхивать ингалятор.
Потянуть крышку вниз, пока не услышите щелкания(рис. 2).
Теперь препарат готов к ингаляции. Счетчик доз отчисляет в обратном порядке на 1 для подтверждения использования.
Если счетчик доз не отчисляет дозу в обратном порядке после того, как вы услышали щелкание, ингалятор не работает. Необходимо вернуть его фармацевту для получения совета.
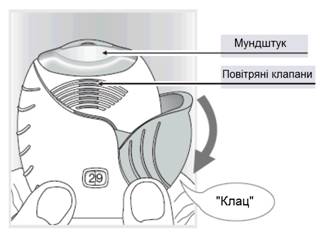 Рис. 2
Рис. 2
3 Как делать ингаляцию препарата
Удерживать ингалятор на расстоянии от рта и сделать выдох без лишнего усилия.
Не выдыхать в ингалятор.
Разместить мундштук между губами и плотно сжать их вокруг мундштука(рис. 3).
Не перекрывать воздушные клапаны пальцами.
Сделать один длинный, ровный, глубокий вдох. Удерживать вдох как можно дольше(по меньшей мере 3-4 секунды).
· Вынуть ингалятор из рта.
· Медленно и осторожно выдохнуть.
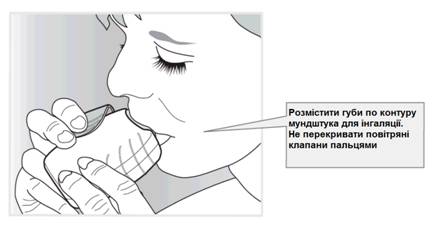 Рис. 3
Рис. 3
Возможно, не будет чувствоваться вкус или ощущение препарата, даже в случае правильного приложения ингалятору.
4 Закрыть ингалятор и прополоскать рот
Если есть необходимость в очистке мундштука, используйте сухую ткань перед закрытием крышки.
Подтянуть крышку кверху, пока она будет двигаться, чтобы закрыть мундштук(рис. 4).
Прополоскать рот водой после применения ингалятора. Это уменьшит достоверность болевых ощущений в роте и горле как проявлений косвенного действия.
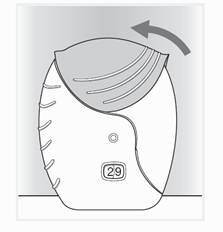 Рис. 4
Рис. 4
Деть.
Безопасность и эффективность препарата Релвар Елліпта для детей в возрасте до 12 лет не изучались для лечения бронхиальной астмы. Данные отсутствуют.
Передозировка
Симптомы и признаки
Передозировка флютиказону фуроата/вилантеролу может вызывать симптомы в связи с действием отдельных компонентов, включая те, которые отмечаются при передозировке бета2-агоністами и отвечают известным эффектам класса ингаляционных кортикостероидов(см. раздел "Особенности применения").
Лечение
Специфическое лечение при передозировке флютиказону фуроатом/вилантеролом отсутствует. В случае передозировки пациента необходимо лечить с помощью пидтримуючеи терапии с соответствующим мониторингом, если это необходимо.
Кардіоселективні блокаторы беты должны рассматриваться лишь при сильной передозировке вилантеролом, которое вызывает клиническую обеспокоенность и не отвечает на пидтримуючи мероприятия. Кардіоселективні блокаторы беты необходимо применять с осторожностью пациентам с бронхоспазмом в анамнезе.
Дальнейшее ведение пациента должно отвечать клиническим показанием.
Побочные реакции
Обзор профиля безопасности
Для определения частоты возникновения нежелательных реакций, связанных с флютиказону фуроатом/вилантеролом, использовались данные больших клинических исследований астмы и ХОЗЛ. В программе клинического исследования астмы относительно интегрированной оценки нежелательных реакций в целом были включены 7034 пациенты. В программе клинического исследования ХОЗЛ относительно интегрированной оценки нежелательных реакций в целом было включено 6237 пациенты.
Нежелательными реакциями, о которых чаще всего сообщалось при применении флютиказону фуроата и вилантеролу, были головная боль и назофарингит. За исключением пневмонии и переломов, профиль безопасности был одинаковым у пациентов с астмой и ХОЗЛ. Во время клинических исследований пневмония и переломы наблюдались чаще у пациентов из ХОЗЛ.
В таблице ниже системные реакции поданы за системно-органным классом и частотой.
Классификация частоты возникновения побочных эффектов :
очень часто ³ 1/10;
часто ³ 1/100 и < 1/10;
нечасто ³ 1/1000 и < 1/100;
редко ³ 1/10000 и < 1/1000;
очень редко < 1/10000.
В каждой группе частоты возникновения нежелательные реакции представлены в порядке уменьшения серьезности.
Классы систем органов |
Нежелательная реакция |
Частота |
|
Инфекции и инвазия |
Пневмония*, инфекция верхних дыхательных путей, бронхит, грипп, кандидоз ротовой полости и горла |
Часто |
|
Со стороны иммунной системы |
Реакции гиперчувствительности, включая анафилаксию, ангионевротический отек, высыпание, крапивница |
Редко |
|
Со стороны психики |
Тревога |
Редко |
|
Со стороны нервной системы |
Головная боль Тремор |
Очень часто Редко |
|
Со стороны сердечной системы |
Экстрасистолия Сердцебиение Тахикардия |
Нечасто Редко Редко |
|
Со стороны дыхательной системы, органов грудной клетки и средостения |
Назофарингит Орофарингеальний боль, синусит, фарингит, ринит, кашель, дисфония |
Очень часто Часто |
|
Со стороны желудочно-кишечного тракта |
Боль в животе |
Часто |
|
Со стороны скелетно-мышечной и соединительной ткани |
Боль в суставах, боль в спине, переломы**, мышечные спазмы |
Часто |
|
Общие расстройства и нарушения в месте введения |
Лихорадка |
Часто |
*, ** См. ниже "Отдельные побочные реакции"
Отдельные побочные реакции
Пневмония
В интегрированном анализе двух дублированных однолетних исследований у пациентов из ХОЗЛ с обострением за прошлый год(n =3D 3255) количество случаев пневмонии на 1000 пацієнто-років сложили 97,9 для флютиказону фуроата/вилантеролу 184/22, 85,7 для флютиказону фуроата/вилантеролу 92/22 и 42,3 в группе вилантеролу 22. Для пневмонии тяжелой степени соответствующее количество случаев на 1000 пацієнто-років сложили 33,6; 35,5 и 7,6 соответственно, тогда как для серьезной пневмонии соответствующие случаи на 1000 пацієнто-років сложили 35,1 для флютиказону фуроата/вилантеролу 184/22, 42,9 для флютиказону фуроата/вилантеролу 92/22 и 12,1 для вилантеролу 22. Количество летальных случаев пневмонии, откорректированных по экспозиции препарата, сложили 8,8 для флютиказону фуроата/вилантеролу 184/22 в сравнении с 1,5 для флютиказону фуроата/вилантеролу 92/22 и 0 для вилантеролу 22.
В интегрированном анализе 11 исследования среди пациентов с астмой(7034 пациенты) частота возникновения пневмонии на 1000 пацієнто-років сложила 18,4 для флютиказону фуроата/вилантеролу 184/22 в сравнении с 9,6 для флютиказону фуроата/вилантеролу 92/22 и 8,0 в группе плацебо.
Переломы
В двух дублированных 12-месячных исследованиях среди общего количества 3255 пациенты из ХОЗЛ частота переломов костей в целом была низкой во всех группах лечения с высшей частотой во всех группах препарата Релвар Елліпта(2%) в сравнении с группой вилантеролу в дозе 22 мкг(< 1%). Хотя в группах препарата Релвар Елліпта было больше переломы в сравнении с группой вилантеролу в дозе 22 мкг, переломы, которые обычно связывались с применением кортикостероидов(например компрессионные переломы хребта/переломы хребта в пояснично-грудном отделе, переломы бедренной кости и вертлюжной впадины), возникали в < 1% в группах лечения препаратом Релвар Елліпта и вилантеролу.
В интегрированном анализе 11 исследования среди пациентов с астмой(7034 пациенты) частота возникновения переломов сложила < 1% и она обычно связывалась с травмой.
Срок пригодности. 2 годы.
Срок пригодности после открытия лотка - 6 недели.
Условия хранения.
Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Хранить в оригинальной упаковке для защиты от влаги.
Применять в течение 6 недель после открытия лотка.
В специально отведенном месте пациенту необходимо отметить конечную дату, после которой ингалятор необходимо выбросить. Дата должна быть отмечена сразу же после исключения ингалятора из лотка.
Упаковка
Порошок для ингаляций, дозированный, по 184 мкг/22 мкг/дозу, по 14 или 30 дозы в порошковом ингаляторе № 1 в картонной упаковке.
Категория отпуска. За рецептом.
Производитель.
Глаксо Оперейшнс ЮКК Лімітед, Великая Британия /Glaxo Operations UK Limited, United Kingdom.
Местонахождение производителя и его адрес места осуществления деятельности
Глаксо Оперейшнс ЮКК Лімітед, Прайорі Стріт, Веа, Хертфордшир, SG12 0DJ, Великая Британия/Glaxo Operations UK Limited, Priory Street, Ware, Hertfordshire, SG12 0DJ
United Kingdom.
Другие медикаменты этого же производителя
Форма: таблетки, покрытые пленочной оболочкой, по 5 мг, по 30 таблетки в блистере в картонной коробке
Форма: гранулы для приготовления 100 мл(125 мг/5 мл) суспензии, 1 флакон с гранулами вместе с мерным колпачком и мерной ложечкой в картонной коробке
Форма: таблетки по 400 мг; по 1 таблетке в блистере; по 1 блистеру в коробке из картона
Форма: суспензия(DTPa - IPV) для инъекций по 0,5 мл(1 доза) и лиофилизат(Hib), cуспензия(DTPa - IPV) для инъекций по 0,5 мл(1 доза) в предварительно наполненном одноразовом шприце № 1 в комплекте с двумя иглами и лиофилизат(Hib) в флаконе № 1, что смешиваются перед использованием: по 1 предварительно наполненному одноразовому шприцу в комплекте с двумя иглами и 1 флаконом с лиофилизатом(Hib) в вакуумной стерильной упаковке; по 1 вакуумной стерильной упаковке в картонной коробке
Форма: гель по 5 г, по 15 г, по 25 г или по 50 г геля в тубе; по 1 тубе в картонной коробке