Инфанрикс™ Ипв Хиб / Infanrix™ Ipv Hib Комбинированная Вакцина Для Профилактики Дифтерии, Столбняка, Коклюша(Ацелюлярний Компонент), Полиомиелита И Заболеваний, Возбудителем Которых Является Haemophilus Influenzae Типа B
Регистрационный номер: UA/15832/01/01
Импортёр: ГлаксоСмитКляйн Экспорт Лимитед
Страна: Великая БританияАдреса импортёра: 980 Грейт Уест Роуд, Брентфорд, Миддлсекс, TW8 9GS, Большая Британiя
Форма
суспензия(DTPa - IPV) для инъекций по 0,5 мл(1 доза) и лиофилизат(Hib), cуспензия(DTPa - IPV) для инъекций по 0,5 мл(1 доза) в предварительно наполненном одноразовом шприце № 1 в комплекте с двумя иглами и лиофилизат(Hib) в флаконе № 1, что смешиваются перед использованием: по 1 предварительно наполненному одноразовому шприцу в комплекте с двумя иглами и 1 флаконом с лиофилизатом(Hib) в вакуумной стерильной упаковке; по 1 вакуумной стерильной упаковке в картонной коробке
Состав
0,5 мл(1 доза) растворенной вакцины содержит: дифтерийного анатоксину(D) не меньше чем 30 международные единицы(МО) (25 Lf(флоккулирующих единиц)); столбнякового анатоксину(T) не менее чем 40 МО(10 Lf); кашлюкового анатоксину(PT) 25 мкг; филаментозного гемаглютинину(FHA) 25 мкг; пертактину(PRN) 8 мкг; инактивированного полиовирусу(IPV) : - типа 1(Mahoney) 40 D- антигенных единиц(DU), - типа 2(MEF - 1) 8 DU, - типа 3(Saukett) 32 DU; конъюгату капсульного полисахарида(PRP) Haemophilus influenzae типа b 10 мкг, ковалентный связанного со столбняковым анатоксином(Т) адсорбируемым ~30 мкг
Виробники препарату «Инфанрикс™ Ипв Хиб / Infanrix™ Ipv Hib Комбинированная Вакцина Для Профилактики Дифтерии, Столбняка, Коклюша(Ацелюлярний Компонент), Полиомиелита И Заболеваний, Возбудителем Которых Является Haemophilus Influenzae Типа B»
Страна производителя: Бельгия
Адрес производителя: Рю где лъИнститю, 89 1330 м. Риксенсарт, Бельгия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
ІНФАНРИКС™ ІПВ Хіб
(INFANRIX™ IPV Hib)
Комбинированная вакцина для профилактики дифтерии, столбняка, коклюша
( ацелюлярний компонент), полиомиелита и заболеваний
возбудителем которых является Haemophilus influenzae типа b
Состав
действующие вещества:
0,5 мл(1 доза) растворенной вакцины содержит:
дифтерийного анатоксину(D) не меньше чем 30 международные единицы(МО) (25 Lf(флоккулирующих единиц));
столбнякового анатоксину(T) не менее чем 40 МО(10 Lf);
кашлюкового анатоксину(PT) 25 мкг;
филаментозного гемаглютинину(FHA) 25 мкг;
пертактину(PRN) 8 мкг;
инактивированного полиовирусу(IPV) :
- типа 1(Mahoney) 40 D- антигенных единиц(DU)
- типа 2(MEF - 1) 8 DU
- типа 3(Saukett) 32 DU;
конъюгату капсульного полисахарида(PRP) Haemophilus influenzae типа b 10 мкг, ковалентный связанного со столбняковым анатоксином(Т) адсорбируемым ~30 мкг;
вспомогательные вещества: лактоза, натрию хлорид, алюминий(в форме солей: алюминию гидроксид) за Al3+, среда 199, вода для инъекций.
Хлорид калия, динатрию фосфат, фосфат калия однозамещен, полисорбат 80, глицин, формальдегид, неомицину сульфат, полимиксину сульфат присутствующие в остаточных количествах как следствие производственных процессов.
Врачебная форма. Суспензия(DTPa - IPV) для инъекций и лиофилизат(Hib), что смешиваются перед использованием.
Основные физико-химические свойства: ІНФАНРИКС™ ІПВ Хіб - комбинированная вакцина для профилактики дифтерии, столбняка, коклюша(ацелюлярний компонент), полиомиелита и заболеваний, возбудителем которых является Haemophilus influenzae типа b.
DTPa - IРV являет собой мутную жидкость после стряхивания(в шприце); белый осадок и бесцветный супернатант(сверхосадочная жидкость) после седиментации(осаждение). Лиофилизированная вакцина представлена в виде белого порошка или брикету(в стеклянном флаконе). После возобновления лиофилизированной вакцины Hib жидкостью DTPa - IPV - прозрачная бесцветная жидкость.
Фармакотерапевтична группа. Комбинированные бактериальные и вирусные вакцины. Код АТХ J07C A06.
Иммунологические и биологические свойства.
Фармакодинамика.
Дифтерийный и столбняковый анатоксины, полученные из культур Corynebacterium diphtheriae и Clostridium tetani, инактивируют и очищают. Компоненты ацелюлярной кашлюковой вакцины(РТ, FHA, пертактин) готовят путем выращивания культуры Bordetella pertussis в фазе I, из какой РТ, FHA и пертактин экстрагируют и очищают. FHA и пертактин обрабатывают формальдегидом, РТ обрабатывают глутеральдегидом и формальдегидом и необоротный инактивируют.
Три вируса полиомиелита культивируют на перещеплювальний линии Vero, очищают и инактивируют формальдегидом.
Полисахарид Hib готовят из Haemophilus influenzae типа b, штамму 20752, и сочетают со столбняковым анатоксином. После очистки конъюгат лиофилизують у присутствия лактозы как стабилизатора.
Результаты, полученные в клинических исследованиях для каждого из компонентов вакцины, представленные в таблицах ниже.
Таблица 1
Количество лиц(в процентах) с титрами антител ≥ контрольных уровней после первичной вакцинации препаратом ІНФАНРИКС™ ІПВ Хіб
|
Уровень антител |
3-5 месяцы N=3D86 ( 1 дослид-ження) % |
1,5-3,5-6 месяцы N=3D62 ( 1 дослид-ження) % |
2-3-4 месяцы N=3D337 ( 3 дослид-ження) % |
2-4-6 месяцы N=3D624 ( 6 дослид-жень) % |
3-4-5 месяцы N=3D127 ( 2 дослид-ження) % |
3-4,5-6 месяцы N=3D198 ( 1 дослид-ження) % |
|
Против дифтерийного анатоксину ( 0,1 МО/мл)* |
94,1 |
100 |
98,8 |
99,3 |
94,4 |
99,5 |
|
Против столбнякового анатоксину ( 0,1 МО/мл)* |
100,0** |
100 |
99,7 |
99,8 |
99,2 |
100 |
|
Против кашлюкового анатоксину ( 5 EL. O/мл) |
99,5** |
100 |
99,4 |
100 |
98,4 |
100 |
|
Против филаментозного гемаглютинину ( 5 EL. O/мл) |
99,7** |
100 |
100 |
100 |
100 |
100 |
|
Против пертактину ( 5 EL. O/мл) |
99,0** |
100 |
100 |
100 |
100 |
100 |
|
Против вируса полиомиелита 1 типа ( 1: 8 разведение)* |
93,0 |
н/д |
99,1 |
99,5 |
100 |
100 |
|
Против вируса полиомиелита 2 типа ( 1: 8 разведение)* |
95,3 |
н/д |
95,7 |
99,0 |
99,2 |
100 |
|
Против вируса полиомиелита 3 типа ( 1: 8 разведение)* |
98,8 |
н/д |
100 |
100 |
99,2 |
99,4 |
|
Против PRP(Hib) ( 0,15 мкг/мл)* |
83,7 |
100 |
98,5 |
98,5 |
100 |
98,4 |
|
Против PRP(Hib) ( 1,0 мкг/мл) |
51,2 |
87,1 |
68,5 |
76,0 |
97,6 |
81,2 |
N - количество пациентов;
н/д - нет данных;
* уровни, которых достаточно для защиты от возбудителя;
** результаты после введения второй дозы в исследованиях, в каких DTPa - HBV - IPV+Hib назначалась в 3, 5 и 11 месяцы жизнь ребенка.
Таблица 2
Количество лиц(в процентах) с титрами антител ≥ контрольных уровней после ревакцинации препаратом ІНФАНРИКС™ ІПВ Хіб
|
Уровень антител |
Ревакцинация на 11/12 месяце жизни потом 3-5-месячного первичного курса вакцинации N=3D184(1 исследование) % |
Ревакцинация в течение второго года жизни после трех доз первичного курса вакцинации N=3D1326(9 исследования) % |
|
Против дифтерийного анатоксину ( 0,1 МО/мл)* |
100 |
99,8 |
|
Против столбнякового анатоксину ( 0,1 МО/мл)* |
99,9** |
99,9 |
|
Против кашлюкового анатоксину ( 5 EL. O/мл) |
99,9** |
99,7 |
|
Против филаментозного гемаглютинину ( 5 EL. O/мл) |
99,9** |
100 |
|
Против пертактину ( 5 EL. O/мл) |
99,5** |
99,9 |
|
Против вируса полиомиелита 1 типа ( 1: 8 разведение)* |
99,4 |
99,9 |
|
Против вируса полиомиелита 2 типа ( 1: 8 разведение)* |
100 |
100 |
|
Против вируса полиомиелита 3 типа ( 1: 8 разведение)* |
99,4 |
100 |
|
Против PRP(Hib) ( 0,15 мкг/мл)* |
100 |
100 |
|
Против PRP(Hib) ( 1,0 мкг/мл) |
96,7 |
99,2 |
N - количество пациентов;
* уровни, которых достаточно для защиты от возбудителя;
** результаты после введения 3 дозы в исследованиях, в каких DTPa - HBV - IPV+Hib назначалась в 3, 5 и 11 месяцы жизнь ребенка.
Эффективность Hib- компоненту(комбинированного из DTPa, DTPa - IPV или DTPa - HBV - IPV) была изучена в масштабном исследовании постмаркетингового надзора, которое проводилось в Германии. По данным наблюдения, длительностью свыше 4,5 года, эффективность вакцин DTPa+Hib или DTPa - IPV+Hib достигала 96,7 % после полной схемы первичной вакцинации и 98,5 % после бустерной дозы(независимо от первичной прививки). По данным наблюдения длительностью свыше 7 лет, эффективность Hib- компонентов двух гексавалентних вакцин представляла 89,6 % после полной схемы первичной вакцинации и 100% после полной схемы первичной вакцинации плюс бустерной дозы(независимо от Hib- вакцины, которая использовалась для первичной прививки).
Фармакокинетика.
Оценка фармакокинетичних свойств для вакцин не проводится.
Клинические характеристики
Показание
ІНФАНРИКС™ ІПВ Хіб предназначается для активной иммунизации детей в возрасте от 2 месяцев против дифтерии, столбняка, коклюша, полиомиелита и инфекций, возбудителем которых является Haemophilus influenzae типа b.
ІНФАНРИКС™ ІПВ Хіб также показана для ревакцинации детей, которым раньше проводилась вакцинация против коклюша, дифтерии, столбняка, полиомиелита и заболеваний, возбудителем которых является Haemophilus influenzae типа b.
ІНФАНРИКС™ ІПВ Хіб не защищает от заболеваний, которые вызваны другими типами Haemophilus influenzae, от менингитов, обусловленных другими возбудителями.
Прививка детей на территории Украины осуществляется согласно требованиям действующих приказов МОЗ Украины.
Противопоказание
ІНФАНРИКС™ ІПВ Хіб не следует назначать лицам с известной гиперчувствительностью к любому компоненту вакцины или лицам, в которых возникли признаки гиперчувствительности после предыдущего введения вакцин для профилактики дифтерии, столбняка, коклюша, инактивированной полиовакцини или Хіб-вакцин.
ІНФАНРИКС™ ІПВ Хіб противопоказанная для прививки детей, в которых возникла энцефалопатия неизвестной этиологии в течение 7 дней после предыдущей прививки вакциной, которая содержала кашлюковий компонент.
Как и при применении других вакцин, введения ІНФАНРИКС™ ІПВ Хіб должно быть отложенный у лиц с острыми тяжелыми заболеваниями, которые сопровождаются лихорадкой. Однако наличие незначительной инфекции не является противопоказанием.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Согласно принятой на это время в педиатрии практикой одновременных прививок разными вакцинами, ІНФАНРИКС™ ІПВ Хіб можно назначать одновременно с вакциной для профилактики гепатита В. Разведенную вакцину ІНФАНРИКС™ ІПВ Хіб и другую вакцину для инъекционного введения нужно вводить в разные места.
Как и при применении других вакцин, у пациентов, которые получают иммуносупрессивную терапию, или у пациентов с иммунодефицитом может не достигаться адекватный иммунный ответ.
Особенности применения
Согласно надлежащей клинической практике, вакцинации должны предшествовать изучение анамнеза(особенно относительно предыдущей вакцинации и возможных случаев побочных реакций) и медицинский обзор.
ІНФАНРИКС™ ІПВ Хіб следует назначать с осторожностью лицам с тромбоцитопенией или нарушениями свертывания крови, поскольку при внутримышечном введении вакцины у таких лиц может возникнуть кровотечение.
ІНФАНРИКС™ ІПВ Хіб содержит следовые количества неомицина и полимиксина, потому вакцину необходимо назначать с осторожностью лицам с известной гиперчувствительностью к любому из этих антибиотиков.
Как и при применении всех других инъекционных вакцин, на случай возникновения анафилактических реакций после введения вакцины нужно проводить наблюдение за пациентом в течение не менее 30 минут и мать наготове все необходимое для проведения соответствующего лечения.
Синкопе(потеря сознания) может возникнуть под время или к любой инъекционной вакцинации как психогенная реакция на инъекцию иглой. Вакцинацию необходимо проводить только в положении вакцинированного сидя или лежа и оставить его в том же положении(сидя или лежа) в течение 15 минут после вакцинации для предупреждения травматизации.
Как и все вакцины для профилактики дифтерии, столбняка и коклюша, эту вакцину следует вводить глубоко внутримышечно в переднелатеральну участок бедра. Желательно, чтобы место инъекции каждого в следующий раз изменялось.
Ожидаемый иммунологический ответ может отсутствовать после прививки пациентов с иммуносупрессией, например, в тех, кто принимает имуносупресанти.
Если любая из нижеприведенных реакций была связана во времени с введением DTP- содержащей вакцины, решение относительно назначения следующих доз вакцины, которая содержит кашлюковий компонент, следует тщательным образом обдумать. К таким реакциям принадлежат:
- температура ³40,0 °C(при ректальном измерении) в течение 48 часов после вакцинации, не связанная с другими причинами, которые можно идентифицировать;
- коллапс или шокоподобное состояние(гипотонично-гипореспонсивний эпизод) в течение 48 часов после вакцинации;
- постоянный, непрерывный плач ребенка, который длится ³3 часов, в течение 48 часов после вакцинации;
- судороги с лихорадкой или без нее, что развиваются в течение 3 дней после вакцинации.
Однако, поскольку эти реакции не ассоциируют необоротными последствиями, могут быть такие обстоятельства(например высокая заболеваемость на коклюш), при которых потенциальные преимущества прививки будут превышать потенциальный риск.
У детей с прогрессирующими неврологическими заболеваниями, в том числе инфантильными спазмами, неконтролируемой эпилепсией или прогрессирующей энцефалопатией, иммунизацию кашлюковим компонентом(ацелюлярним или цильноклитинним) лучше отложить до той поры, пока состояние ребенка не стабилизируется. Однако решение относительно целесообразности назначения протикашлюковой вакцины необходимо принимать индивидуально, тщательным образом взвесив риск и преимущества.
Хіб-компонент не защищает от заболеваний, вызванных другими типами Haemophilus influenzae инфекции или от менингита, вызванного другими микроорганизмами.
Фебрильні судороги в анамнезе ребенка, судороги в семейном анамнезе, синдром внезапной детской смерти(СРДС) в семейном анамнезе или побочные реакции после прививки вакцинами DTP, IPV и/или Hib в семейном анамнезе не являются противопоказаниями для прививки.
Вич-инфекция не является противопоказанием для прививки.
Было описано выведение с мочой капсульного полисахарида антигену после назначения Hib- вакцины, потому в течение 1-2 недель после прививки определения этого антигену в моче при подозрении на Hib- инфекции может не иметь диагностического значения.
ІНФАНРИКС™ ІПВ Хіб ни при каких обстоятельствах нельзя вводить внутривенно.
При назначении первичной иммунизации преждевременно рожденным младенцам(≤ 28 недели гестации) следует иметь в виду потенциальный риск развития у них апноэ и необходимость контроля за дыхательной функцией в течение 48-72 часов после вакцинации, особенно в случае наличия в анамнезе младенца недоразвивания дыхательной системы. Поскольку польза вакцинации у этой группы младенцев является высокой, от вакцинации не следует отказываться или ее откладывать.
ІНФАНРИКС™ ІПВ Хіб содержит менее 1 ммоль(23 мг) /дозу натрия, то есть практически свободный от натрия.
Применение в период беременности или кормления груддю
Поскольку вакцина ІНФАНРИКС™ ІПВ Хіб не предназначена для применения взрослым женщинам, данные о безопасности применения вакцины в период беременности или лактации отсутствуют.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Препарат применяют детям.
Способ применения и дозы
Схема первичной вакцинации включает 3 дозы вакцины, которые вводятся в первом полугодии жизни и могут назначаться из 2-месячного возраста ребенка. Между дозами следует выдерживать интервал не менее 1 месяца.
Бустерная доза рекомендована в течение второго года жизни, не раньше чем через 6 месяцы после окончания схемы первичной вакцинации.
Применяют ІНФАНРИКС™ ІПВ Хіб путем глубокого внутримышечного введения в переднелатеральну участок бедра. Желательно, чтобы каждая следующая доза вводилась в другое место.
ІНФАНРИКС™ ІПВ Хіб следует назначать с осторожностью лицам с тромбоцитопенией или нарушениями свертывания крови, поскольку при внутримышечном введении вакцины у таких лиц может возникнуть кровотечение. Место инъекции следует крепко прижать(не растирая) по меньшей мере на две минуты.
Инструкция относительно приготовления вакцины перед использованием.
Лиофилизат вакцины Hib, суспензию вакцины DTPa - IPV и растворенную комбинированную вакцину ІНФАНРИКС™ ІПВ Хіб необходимо проверить визуально на наличие любых посторонних частей та/або изменение физических свойств. Если такие изменения имеют место, вакцину использовать нельзя.
Поскольку при хранении в суспензии DTPa - IPV может образовываться осадок, необходимо потрусить ее перед растворением в ней лиофилизата вакцины Hib.
Препарат следует растворять, добавляя все содержимое контейнера, который содержит компонент DTPa, - IPV, к флакону с лиофилизатом вакцины Hib. Смешивать вместе можно лишь компоненты одной вакцины, не используя другие вакцины или компоненты другой серии этой вакцины. После добавления суспензии DTPa - IPV к лиофилизату вакцины Hib смесь необходимо хорошо стрясти, чтобы их содержимое перемешалось.
Растворенная вакцина ІНФАНРИКС™ ІПВ Хіб являет собой более мутную суспензию, чем жидкий компонент DTPa - IPV отдельно. Это не ухудшает качество вакцины. Если наблюдаются другие изменения внешнего вида вакцины, ее использовать нельзя.
Вакцину следует использовать сразу же после ее растворения.
Для проведения инъекции наберите в шприц все содержимое флакона. Снимите и не используйте первую иглу, с помощью которой проводили смешивание компонентов вакцины. Для выполнения инъекции присоедините другую иглу.
Инструкция относительно использования предварительно наполненного шприца с адаптером с насадкой Люера(PRTC - пластиковый жесткий винтовой колпачок)
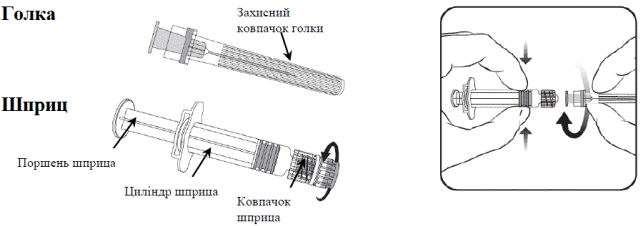
1. Держа цилиндр шприца в одной руке(не держитесь за поршень шприца), открутите колпачок шприца, вращая его против часовой стрелки.
2. Вставьте иглу в шприц, закрутите ее полностью к упору по часовой стрелке(см. рисунок).
3. Снимите защитный колпачок иглы, который может быть кое-что плотно закреплен.
4. Приготовьте вакцину для применения как описано выше.
Любой неиспользованный продукт или остатки готового препарата должны быть уничтожены согласно действующим требованиям.
Деть.
Вакцину ІНФАНРИКС™ ІПВ Хіб применяют детям в возрасте от 2 месяцев(смотри раздел "Показания"). Вакцину ІНФАНРИКС™ ІПВ Хіб не рекомендовано применять взрослым, подросткам и детям в возрасте от 5 лет.
Передозировка
По данным пислялицензийного фармаконагляду пришло несколько сообщений о случаях передозировки. Побочные явления, что возникали при передозировке, были подобными тем, которые наблюдались при применении рекомендованных доз вакцины Інфанрикс™ ІПВ Хіб.
Побочные реакции.
Данные клинических исследований
Представлен ниже профиль безопасности вакцины определен на основе данных, полученных от больше чем 3500 лица.
Как и при введении любых DTPa- вакцин или DTPa- содержащих комбинированных вакцин, при введении бустерной дозы препарата ІНФАНРИКС™ ІПВ Хіб наблюдалось увеличение местных проявлений и частоты развития лихорадки(в сравнении с первичной иммунизацией).
Побочные явления, которые наблюдались при применении вакцины, приведенные в соответствии с частотой развития, :
Очень часто:³ 1/10
Часто:³ 1/100 к < 1/10
Нечасто: ³ 1/1000 к < 1/100
Редко: ³ 1/10000 к < 1/1000
Очень редко: < 1/10000
Инфекционные и паразитарные заболевания
Нечасто: инфекции верхних дыхательных путей.
Нарушение со стороны кровеносной и лимфатической системы
Нечасто: лимфаденопатия.
Нарушение метаболизма и алиментарные расстройства
Очень часто: потеря аппетита.
Нарушение психики
Очень часто: повышенная возбудимость, непрерывный плач, беспокойство.
Нарушение функции нервной системы
Очень часто: бессонница.
Нарушение респираторной системы, органов грудной клетки и средостения
Нечасто: кашель, бронхит, ринорея.
Нарушение желудочно-кишечного тракта
Часто: диарея, блюет.
Нарушение функции кожи и подкожных тканей
Нечасто: висипка, крапивница.
Редко: зуд, дерматит.
Общие расстройства и реакции в месте введения
Очень часто: реакции в месте инъекции, такие как боль и покраснение, местная припухлость(≤ 50 мм), лихорадка(³ 38 °C).
Часто: реакции в месте инъекции, такие как инфильтрат, местная припухлость (>50 мм) 1.
Нечасто: лихоманка2(> 39,5 °C), повышенная утомляемость, диффузный отек конечности, в которую вводилась вакцина, иногда с привлечением смежного суглоба1.
Данные постмаркетингового надзора
Нарушение со стороны кровеносной и лимфатической системы
Тромбоцитопенія4.
Нарушение иммунитета
Аллергические реакции(в том числе анафілактичні3 и анафилактоидни реакции).
Нарушение функции нервной системы
Судороги(с лихорадкой или без нее), коллапс или шокоподобное состояние(гипотонично-гипореспонсивний эпизод).
Нарушение со стороны респираторной системы, органов грудной клетки и средостения
Апное3(см. раздел "Особенности применения" для апноэ у преждевременно рожденных младенцев(≤ 28 недели гестации)).
Нарушение со стороны кожи и подкожных тканей
Ангионевротический набряк3.
Общие расстройства и реакции в месте введения :
Отек всей конечности, в которую вводилась вакцина1, везикулы в месте ін'єкції3.
1Діти, которым первичная иммунизация проводилась вакциной против коклюша с ацелюлярним компонентом, более склонные к развитию реакций в виде припухлости или отека после бустерной дозы в сравнении с детьми, которым первичная прививка проводилась вакциной против коклюша с цильноклитинним компонентом. Эти реакции проходят в среднем за 4 дни.
2часто при ревакцинации.
3спостерігалися при применении DTPa- содержащих вакцин, производства "ГлаксоСмітКляйн".
4спостерігалася при применении противодифтерийной и противостолбнячной вакцин.
Срок пригодности. 36 месяцы. Дата окончания срока пригодности вакцины отмечена на упаковке.
Условия хранения.
Вакцину ІНФАНРИКС™ ІПВ Хіб необходимо хранить при температуре от 2 до 8 °С. При транспортировке следует придерживаться рекомендованных условий хранения. DTPa - IРV суспензию и приготовленную для введения вакцину нельзя замораживать. Не использовать, если вакцина была заморожена.
Несовместимость.
ІНФАНРИКС™ ІПВ Хіб не следует смешивать с другими вакцинами в одном шприце.
Упаковка
Суспензия(DTPa - IPV) для инъекций по 0,5 мл(1 доза) в предварительно наполненном одноразовом шприце № 1 в комплекте с двумя иглами и лиофилизат(Hib) в флаконе № 1, что смешиваются перед использованием.
Предварительно наполненные шприцы и флаконы изготовлены из нейтрального стекла типа И, что отвечает требованиям Европейской фармакопеи.
Категория отпуска. За рецептом.
Производитель. ГлаксоСмітКляйн Біолоджікалз С.А., Бельгия / GlaxoSmithKline Biologicals S.A., Belgium.
Местонахождение производителя и адрес места осуществления его деятельности.
Рю где лъИнститю, 89 1330 м. Ріксенсарт, Бельгия / Rue de l'Institut, 89 1330 Rixensart, Belgium.
Другие медикаменты этого же производителя
Форма: порошок для раствора для инъекций по 2 г, 1 флакон с порошком в картонной коробке
Форма: лиофилизированный порошок для инъекций, 1 флакон с порошком в комплекте с растворителем(вода для инъекций) по 0,5 мл(1 доза) в предварительно наполненном шприце(в комплекте с двумя иглами или без игл) или в ампулах в вакуумной стерильной упаковке; по 1 вакуумной стерильной упаковке в картонной коробке; 1 флакон с порошком в комплекте с растворителем(вода для инъекций) по 0,5 мл(1 доза) в предварительно наполненном шприце(в комплекте с двумя иглами) в вакуумной стерильной упаковке; по 10 вакуумных стерильных упаковок в картонной коробке; 1 флакон с порошком в комплекте с растворителем(вода для инъекций) по 0,5 мл(1 доза) в предварительно наполненном шприце в вакуумной стерильной упаковке; по 1, 10, 20 или 50 вакуумных стерильных упаковок в картонной коробке; 1 флакон с порошком в комплекте с растворителем(вода для инъекций) по 0,5 мл(1 доза) в ампуле в вакуумной стерильной упаковке; по 1, 10 или 100 вакуумных стерильных упаковок в картонной коробке
Форма: суспензия для инъекций 1440 ОТ ELISA по 1 мл(1 доза для взрослых) в флаконах; по 1 флакону в картонной коробке или предварительно наполненных шприцах в комплекте с иглой; по 1 шприцу в картонной коробке
Форма: таблетки, покрытые пленочной оболочкой, по 5 мг, по 30 таблетки в блистере в картонной коробке
Форма: гранулы для приготовления 100 мл(250 мг/5 мл) суспензии, 1 флакон с гранулами вместе с мерным колпачком и мерной ложечкой в картонной коробке