Лирика
Регистрационный номер: UA/3753/01/04
Импортёр: Пфайзер Інк.
Страна: СШААдреса импортёра: 235 Ист 42-га Стрит, Нью-Йорк, НЙ 10017-5755, США
Форма
капсулы по 75 мг по 14 капсулы в блистере; по 1 или по 4 блистеры в картонной коробке; по 21 капсуле в блистере; по 1 или по 4 блистеры в картонной коробке
Состав
1 капсула содержит 75 мг прегабалину
Виробники препарату «Лирика»
Страна производителя: Германия
Адрес производителя: Бетрибштетте Фрайбург, Мусвальдаль 1, 79090 Фрайбург, Германия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
(LYRICA®)
Состав
действующее вещество: прегабалин;
1 капсула содержит 50 мг, 75 мг, 150 мг или 300 мг прегабалину;
вспомогательные вещества: лактоза, моногидрат; крахмал кукурузный; тальк; оболочка капсулы : желатин, титану диоксид(Е 171), натрию лаурилсульфат, кремнию диоксид коллоидный безводен, железа оксид красен(Е 172) (для капсул по 75 мг и 300 мг); чернила: шеллак, железа оксид черный(Е 172), этанол безводный(для капсул по 75 мг и 150 мг), пропиленгликоль; калию гидроксид(для капсул по 50 мг и 300 мг).
Врачебная форма. Капсулы.
Основные физико-химические свойства.
- Капсулы по 50 мг: твердые непрозрачные(белые/белые) желатиновые капсулы с черной полосой, размеру 3, что содержат порошок белого или почти белого цвета. Отпечаток на корпусе "PGN 50", на крышечке - "Pfizer" черными чернилами.
- Капсулы по 75 мг: твердые непрозрачные(белые/помаранчевые) желатиновые капсулы, размеру 4, что содержат порошок белого или почти белого цвета. Відпечаток на корпусе "PGN 75", на крышечке - "Pfizer" черными чернилами.
- Капсулы по 150 мг: твердые непрозрачные(белые/белые) желатиновые капсулы, размеру 2, что содержат порошок белого или почти белого цвета. Відпечаток на корпусе "PGN 150", на крышечке - "Pfizer" черными чернилами.
- Капсулы по 300 мг: твердые непрозрачные(белые/помаранчевые) желатиновые капсулы, размеру 0, что содержат порошок белого или почти белого цвета. Отпечаток на корпусе "PGN 300", на крышечке - "Pfizer" черными чернилами.
Фармакотерапевтична группа. Противоэпилептические средства, другие противоэпилептические средства.
Код АТХ N03A X16.
Фармакологические свойства.
Фармакодинамика.
Действующее вещество - прегабалин, что является аналогом гамма-аминомасляной кислоты [(S)- 3 -(аминометил) -5-метилгексанова кислота].
Механизм действия.
Прегабалін связывается со вспомогательной субъединицей(a2 - d белок) потенциалзалежних кальциевых каналов в центральной нервной системе(ЦНС).
Клиническая эффективность и безопасность.
- Нейропатичний боль.
Во время исследований была продемонстрирована эффективность препарата для лечения диабетической нейропатии, постгерпетической невралгии и поражения спинного мозга. Эффективность препарата при других видах нейропатичного боли не изучали.
Прегабалін изучали в ходе 10 контролируемых клинических исследований длительностью до 13 недель с режимом дозирования препарата дважды на сутки и в ходе исследований длительностью до 8 недель с режимом дозирования трижды на сутки. В целом профили безопасности
и эффективности для режимов дозирования дважды и трижды на сутки были подобными.
В ходе клинических исследований длительностью до 12 недель, в которых лекарственное средство применяли для лечения нейропатичного боли, уменьшения боли периферического и центрального происхождения наблюдалось после первой недели и хранилось в течение всего периода лечения.
В ходе контролируемых клинических исследований из изучения периферической нейропатичного боли в 35 % пациентов, которые применяли прегабалин, и в 18 % пациентов, которые получали плацебо, наблюдалось улучшение на 50 % за шкалой оценки боли. Среди пациентов, в которых не возникало сонливости, такое улучшение наблюдалось у 33 % пациентов, которые применяли прегабалин, и в 18 % пациентов из группы плацебо. Среди пациентов, в которых возникала сонливость, часть пациентов, которые ответили на терапию, представляла 48 % в группе прегабалину и 16 % в группе плацебо.
В ходе контролируемого клинического исследования из изучения нейропатичного боли центрального происхождения у 22 % пациентов, которые применяли прегабалин, и в 7 % пациентов, которые получали плацебо, наблюдалось улучшение на 50 % за шкалой оценки боли.
- Эпилепсия.
Дополнительное лечение. Прегабалін изучали в ходе 3 контролируемых клинических исследований длительностью 12 недели с режимом дозирования дважды или трижды на сутки. В целом профили безопасности и эффективности для режимов дозирования дважды и трижды на сутки были подобными.
Уменьшение частоты судорожных нападений наблюдалось уже на первой неделе.
Деть. Эффективность и безопасность прегабалину в качестве вспомогательного средства при эпилепсии для детей в возрасте до 12 лет и для подростков не установлены. Побочные реакции, которые наблюдались в исследовании из изучения фармакокинетики и переносимости, к которому были включенные пациенты в возрасте от 3 месяцев до 16 лет(n=3D65) с парциальными судорожными нападениями, были подобны побочным реакциям у взрослых. Результаты 12-недельного плацебо-контролируемого исследования при участии 295 детей в возрасте от 4 до 16 лет, целью которого была оценка эффективности и безопасности прегабалину как дополнительной терапии парциальных судорожных нападений, и открытого исследования из изучения безопасности длительностью 1 год при участии 54 детей в возрасте от 3 месяцев до 16 лет с эпилепсией указывают на то, что такие побочные реакции, как пирексия и инфекции верхних дыхательных путей, у детей наблюдаются чаще, чем у взрослых пациентов с эпилепсией(см. разделы "Способ применения и дозы", "Побочные реакции" и "Фармакокинетика").
В 12-недельном плацебо-контролируемом исследовании детям назначали прегабалин по 2,5 мг/кг/сутки(максимум 150 мг/сутки), прегабалин по 10 мг/кг/сутки(максимум 600 мг/сутки) или плацебо. По крайней мере 50%-зменшення парциальных судорожных нападений, в сравнении с исходным уровнем, наблюдался в 40,6 % пациентов, которые получали прегабалин в дозе 10 мг/кг на сутки(р=3D0,0068 сравнительно с плацебо), 29,1 % пациентов, которые получали прегабалин в дозе 2,5 мг/кг/сутки(р=3D0,2600 сравнительно с плацебо) и 22,6 % тех, кто получал плацебо.
Монотерапия(у пациентов с впервые диагностированным заболеванием). Прегабалін изучали в ходе 1 контролируемого клинического исследования длительностью 56 недели с режимом дозирования дважды на сутки. При применении прегабалину не была достигнута не меньшая эффективность в сравнении с применением ламотриджину, согласно оценке через 6 месяцы конечной точки - отсутствию судорожных нападений. Прегабалін и ламотриджин были одинаково безопасными и хорошо переносились.
- Генерализовано тревожное расстройство.
Прегабалін изучали в ходе 6 контролируемых исследований длительностью 4-6 недели, одного исследования длительностью 8 недели при участии пациентов пожилого возраста и одного длительного исследования из изучения профилактики рецидива с двойной слепой фазой профилактики рецидива длительностью 6 месяцы.
Уменьшение симптомов генерализуемого тревожного расстройства в соответствии со шкалой Гамільтона для оценки тревожности(HAM - A) наблюдалось уже на неделе 1.
В ходе контролируемых клинических исследований(длительностью 4-8 недели) у 52 % пациентов, которые применяли прегабалин, и в 38 % пациентов из группы плацебо наблюдалось улучшение не меньше чем на 50 % за общим количеством баллов за шкалой HAM - A от исходного уровня к конечной точке.
Во время контролируемых исследований нечеткость зрения чаще наблюдалась у пациентов, которые применяли прегабалин, чем у пациентов, которые получали плацебо. В большинстве случаев это явление исчезало при продолжении терапии. Офтальмологическое обследование(включая проверку остроты зрения, формальную проверку поля зрения и исследования глазного дна при расширенном зрачке) в рамках контролируемых клинических исследований выполнялось в свыше 3600 пациентов. Среди этих пациентов острота зрения ухудшилась в 6,5 % пациентов в группе прегабалину и в 4,8 % пациентов в группе плацебо. Изменения поля зрения выявлены в 12,4 % пациентов, которые применяли прегабалин, и в 11,7 % пациентов из группы плацебо. Изменения на глазном дне выявлены в 1,7 % пациентов, которые получали прегабалин, и в 2,1 % пациентов в группе плацебо.
- Фибромиалгия.
Эффективность препарата Лирика была установлена в одном 14-недельном двойном слепом плацебо-контролируемом мультицентровом исследовании(F1) и в одном
6-недельном рандомизированном исследовании отмены(F2). В эти исследования привлекались пациенты с диагнозом "фибромиалгия" на основе критериев Американского колледжа ревматологии(распространенная боль в течение 3 месяцев в анамнезе и боль присутствующая в 11 или больше с 18 специфических болевых точек). Исследования продемонстрировали снижение боли по визуальной аналоговой шкале. Улучшение дополнительно было продемонстрировано по общей оценке пациента и по опросу относительно влияния фибромиалгии.
Деть. Было проведено плацебо-контролируемое исследование длительностью 15 недели при участии 107 детей возрастом 12-17 годы с фибромиалгией, которые применяли препарат Лирика в дозе
75-450 мг на сутки. По результатам оценки первичной конечной точки эффективности(изменение общей интенсивности боли от базового уровня до недели 15; рассчитано с помощью 11-бальной шкалы оценивания) было продемонстрировано численно большее улучшение состояния пациентов, которые применяли прегабалин, сравнительно с пациентами, которые принимали плацебо, но это улучшение не достигло статистической значимости. Самыми частыми побочными реакциями, которые наблюдались в клинических исследованиях, были головокружение, тошнота, головная боль, увеличение массы тела и утомляемость. Общий профиль безопасности у подростков был подобным такому у взрослых с фибромиалгией.
Фармакокинетика.
Фармакокінетичні показатели прегабалину в равновесном состоянии были подобными у здоровых добровольцев, пациентов с эпилепсией, которые принимали противоэпилептические препараты, и у пациентов с хронической болью.
Абсорбция.
Прегабалін быстро всасывается при приеме натощак и достигает максимальных концентраций в плазме крови в течение 1 часа после однократного или многократного приложения. Рассчитанная биодоступность прегабалину при пероральном приложении представляет ≥ 90 % и не зависит от дозы. При многократном приложении равновесное состояние достигается через 24-48 часы. Скорость всасывания прегабалину снижается при одновременном приеме с едой, которая приводит к уменьшению максимальной концентрации(Cmax) приблизительно на 25-30 % и удлинение значений tmax приблизительно до 2,5 часа. Однако прием прегабалину одновременно с едой не имел клинически значимого влияния на степень его абсорбции.
Распределение.
В ходе доклинических исследований было показано, что прегабалин проникает сквозь гематоэнцефалический барьер у мышей, крыс и обезьян. Было установлено, что прегабалин проникает сквозь плаценту у крыс и выделяется в молоко крыс в период лактации. У человека объем распределения прегабалину после перорального приложения представляет приблизительно 0,56 л/кг. Прегабалін не связывается с белками плазмы крови.
Метаболизм.
У человека прегабалин испытывает незначительный метаболизм. После введения дозы меченого радиоактивной меткой прегабалину около 98 % радиоактивного вещества выводилось с мочой в виде неизмененного прегабалину. Часть N- метилеваной производной прегабалину - основного метаболиту препарата, который определялся в моче, - представляла 0,9 % от введенной дозы. Во время доклинических исследований не происходило рацемизации S- энантиомера прегабалину в R- энантиомер.
Выведение.
Прегабалін выводится из системного кровотока в неизмененном виде, преимущественно почками. Средний период полувыведения прегабалину представляет 6,3 часы. Плазменный и почечный клиренс прегабалину прямо пропорциональные клиренсу креатинина(см. раздел "Фармакокинетика. Почечная недостаточность").
Пациентам с нарушением функции почек или пациентам на гемодиализе необходимая коррекция дозы препарата(см. раздел "Способ применения и дозы", таблица 1).
Линейность/нелинейность.
Фармакокинетика прегабалину является линейной для всего рекомендованного диапазона доз. Варіабельність фармакокинетики прегабалину среди пациентов является низкой(< 20 %). Фармакокинетика при многократном приложении является предсказуемой на основании данных, полученных при применении однократной дозы. Таким образом, нет потребности в плановом контроле концентраций прегабалину в плазме крови.
Пол.
Результаты клинических исследований свидетельствуют об отсутствии клинически значимого влияния пола на концентрации прегабалину в плазме крови.
Почечная недостаточность.
Клиренс прегабалину прямо пропорциональный клиренсу креатинина. Кроме этого, прегабалин эффективно удаляется из плазмы с помощью гемодиализа(после 4 часов гемодиализа концентрация прегабалину в плазме крови уменьшается приблизительно на 50 %). Поскольку препарат выводится в основном почками, пациентам с почечной недостаточностью необходимо уменьшать дозу препарата, а после гемодиализа - применять дополнительную дозу(см. раздел "Способ применения и дозы", таблица 1).
Печеночная недостаточность.
Специальных фармакокинетичних исследований у пациентов с печеночной недостаточностью не проводились. Поскольку прегабалин не испытывает значительного метаболизма и выводится с мочой преимущественно в неизмененном виде, то маловероятно, чтобы нарушение функции печенки имело значимое влияние на концентрацию прегабалину в плазме крови.
Деть.
Фармакокинетику прегабалину оценивали у детей с эпилепсией(возрастные группы: от 1 до 23 месяцев, от 2 до 6 лет, от 7 до 11 лет и от 12 до 16 лет) при применении доз 2,5 мг/кг/сутки, 5 мг/кг/сутки, 10 мг/кг/сутки и 15 мг/кг/сутки в ходе исследования из изучения фармакокинетики и переносимости.
После перорального приложения прегабалину детям натощак время достижения максимальной концентрации в плазме было в целом аналогичным во всех возрастных группах и представлял от 0,5 часа до 2 часов после приема.
Значения Cmax и площади под кривой зависимости концентрации от времени(AUC) прегабалину росли линейно с увеличением дозы в каждой возрастной группе. У детей с массой тела до 30 кг значения AUC было ниже на 30 %, что обусловлено увеличением на 43 % клиренса, откорректированного за массой тела, у этих пациентов в сравнении с пациентами с массой тела ≥ 30 кг.
Конечный период полувыведения прегабалину представлял в среднем около 3-4 часов у детей в возрасте до 6 лет и 4-6 часы у детей в возрасте от 7 лет.
В ходе популяционного фармакокинетичного анализа было показано, что клиренс креатинина был значимой ковариатой для клиренса перорального прегабалину, а масса тела была значимой ковариатой для мнимого объема распределения перорального прегабалину, и эта связь была аналогичной у детей и взрослых пациентов.
Фармакокинетику прегабалину у пациентов возрастом меньше чем 3 месяцы не изучали(см. раздел "Способ применения и дозы", "Побочные реакции" и "Фармакодинамика").
Пациенты пожилого возраста.
Клиренс прегабалину имеет тенденцию к уменьшению с возрастом. Такое уменьшение клиренсу прегабалину при его приложении перорально согласуется с уменьшением клиренса креатинина, связанным с увеличением возраста. Пациентам с нарушением функции почек, связанным с возрастом, может нуждаться уменьшение дозы прегабалину(см. раздел "Способ применения и дозы", таблица 1).
Кормление груддю.
Фармакокинетику прегабалину при его приложении в дозе 150 мг каждые 12 часы(суточная доза 300 мг), оценивали в 10 женщин, которые кормили груддю, по меньшей мере через 12 недели после родов. Кормление груддю не влияло или имело незначительное влияние на фармакокинетику прегабалину. Прегабалін попадал в грудное молоко, при этом его средние концентрации в равновесном состоянии представляли около 76 % от концентраций в плазме крови матери. Рассчитанная доза, которую получает младенец с грудным молоком(при среднем потреблении молока 150 мл/кг/добу) от женщины, которая принимает прегабалин в дозе 300 мг/сутки или в максимальной дозе 600 мг/сутки, представляет 0,31 или 0,62 мг/кг/сутки соответственно. Эти рассчитанные дозы представляют приблизительно 7 % от общей суточной дозы у матери в пересчете на мг/кг.
Клинические характеристики
Показание
Нейропатичний боль.
Препарат Лирика показан для лечения нейропатичного боли периферического или центрального происхождения у взрослых.
Эпилепсия.
Препарат Лирика показан взрослым в качестве дополнительного лечения при парциальных судорожных нападениях со вторичным генерализованием или без нее.
Генерализуемое тревожное расстройство.
Препарат Лирика показан для лечения генерализуемого тревожного расстройства у взрослых.
Фибромиалгия.
Противопоказание
Гиперчувствительность к действующему веществу или к любому из вспомогательных веществ, перечисленных в разделе "Состав".
Взаимодействие с другими лекарственными средствами и другие виды взаимодействия
Поскольку прегабалин екскретуеться преимущественно в неизмененном виде с мочой, испытывает незначительный метаболизм в организме человека(≤ 2 % дозы выделяется с мочой в форме метаболитив), не ингибуе метаболизм других препаратов in vitro и не связывается с белками плазмы крови, то маловероятно, что прегабалин может вызывать фармакокинетичну взаимодействую или быть объектом такого взаимодействия.
Исследование in vivo и популяционный фармакокинетичний анализ.
Таким образом, в исследованиях in vivo не наблюдалось клинически значимого фармакокинетичной взаимодействия между прегабалином и фенитоином, карбамазепином, вальпроевой кислотой, ламотриджином, габапентином, лоразепамом, Оксикодоном или этанолом. Популяционный фармакокинетичний анализ продемонстрировал, что пероральные противодиабетические средства, диуретики, инсулин, фенобарбитал, тиагабин и топирамат не имеют клинически значимого влияния на клиренс прегабалину.
Пероральные контрацептивы, норетистерон и(или) етинилестрадиол.
Одновременное применение прегабалину с пероральными контрацептивами, норетистероном и(или) етинилестрадиолом не влияет на фармакокинетику равновесного состояния ни одного из этих лекарственных средств.
Лекарственные средства, которые влияют на ЦНС.
Прегабалін может потенцировать эффекты этанола и лоразепаму. В контролируемых клинических исследованиях одновременное многократное пероральное применение прегабалину с Оксикодоном, лоразепамом или этанолом не приводило к клинически значимому влиянию на функцию дыхания. В период постмаркетингового надзора сообщалось о случаях дыхательной недостаточности и запятых у пациентов, которые принимали прегабалин вместе с другими лекарственными средствами, которые подавляют функцию ЦНС. Прегабалін, вероятно, усиливает нарушения когнитивных и основных проворных функций, вызванные Оксикодоном.
Взаимодействия у пациентов пожилого возраста.
Специальных исследований фармакодинамичной взаимодействия при участии добровольцев пожилого возраста не проводились. Исследования взаимодействия лекарственных средств проводили лишь у взрослых пациентов.
Особенности применения
Пациенты с сахарным диабетом.
В соответствии с действующей клинической практикой, некоторые пациенты с сахарным диабетом, масса тела которых увеличилась во время терапии прегабалином, могут нуждаться коррекции дозы сахароснижающих лекарственных средств.
Реакции гиперчувствительности.
После выхода препарата на рынок сообщалось о развитии реакций гиперчувствительности, включая ангионевротический отек. При возникновении таких симптомов ангионевротического отека, как отек лица, периоральний отек или отек верхних дыхательных путей, применения прегабалину следует немедленно прекратить.
Головокружение, сонливость, потеря сознания, спутывание сознания и нарушения психики.
Применение прегабалину сопровождалось появлением головокружения и сонливости, которая может увеличить риск возникновения травматических случаев(падение) у пациентов пожилого возраста. Также после выхода препарата на рынок сообщалось о случаях потери сознания, спутывания сознания и нарушения психики. В связи с этим пациентам следует рекомендовать быть осторожными, пока им не станут известны возможные эффекты этого лекарственного средства.
Расстройства зрения.
Во время контролируемых исследований нечеткость зрения чаще наблюдалась у пациентов, которые принимали прегабалин, чем у пациентов, которые получали плацебо. В большинстве случаев это явление исчезало при продолжении терапии. В ходе клинических исследований, в которых проводили офтальмологическое обследование, частота случаев ухудшения остроты зрения и изменения поля зрения была выше у пациентов, которые применяли прегабалин, сравнительно с пациентами из группы плацебо; частота возникновения изменений на глазном дне была выше у пациентов из группы плацебо(см. раздел "Фармакодинамика").
После выхода препарата на рынок также сообщалось о побочных реакциях со стороны органов зрения, включая потерю зрения, нечеткость зрения или другие изменения остроты зрения, много из которых были временными. После прекращения применения прегабалину эти симптомы со стороны органов зрения могут исчезнуть или уменьшиться.
Почечная недостаточность.
Сообщалось о случаях развития почечной недостаточности, которая иногда была оборотной после прекращения применения прегабалину.
Отмена сопутствующих противоэпилептических препаратов.
Теперь недостаточно данных относительно того, или можно отменять сопутствующие противоэпилептические препараты после того, как в результате добавления прегабалину к терапии будет достигнуто контроль судорог, чтобы перейти к монотерапии прегабалином.
Симптомы отмены.
У некоторых пациентов после прекращения краткосрочной или длительной терапии прегабалином наблюдались симптомы отмены препарата. Сообщалось о таких явлениях: бессонница, головная боль, тошнота, тревожность, диарея, гриппоподобный синдром, нервозность, депрессия, боль, судороги, гипергидроз и головокружения, которые указывают на физическую зависимость. Эту информацию следует сообщить пациенту перед началом терапии.
Судороги, в частности эпилептический статус и большие судорожные нападения, могут возникать во время терапии прегабалином или вскоре после его отмены.
Даны относительно отмены прегабалину после длительного приложения указывают на то, что частота возникновения и степень тяжести симптомов отмены могут зависеть от дозы.
Застойная сердечная недостаточность.
После выхода препарата на рынок сообщалось о застойной сердечной недостаточности у некоторых пациентов, которые принимали прегабалин. Такая реакция наблюдалась по большей части во время лечения прегабалином нейропатичного боли у пациентов пожилого возраста с уже существующими сердечно-сосудистыми нарушениями. Таким пациентам прегабалин следует применять с осторожностью. При прекращении применения прегабалину это явление может исчезнуть.
Лечение нейропатичного боли центрального происхождения в результате поражения спинного мозга.
Во время лечения нейропатичного боли центрального происхождения, вызванного поражением спинного мозга, увеличивалась частота побочных реакций в целом, а также побочных реакций со стороны центральной нервной системы и особенно сонливости. Это может быть связано с адитивной действием сопутствующих лекарственных средств(например, антиспастических препаратов), необходимых для лечения этого состояния. Это обстоятельство следует принимать во внимание, назначая прегабалин при таком состоянии.
Суїцидальне мышления и поведение.
Сообщалось о случаях суицидального мышления и поведения у пациентов, которые получали терапию противоэпилептическими препаратами за некоторыми показаниями. По результатам метаанализа данных, полученных в ходе рандомизированных, плацебо-контролируемых исследований противоэпилептических препаратов, также наблюдалось небольшое повышение риска появления суицидального мышления и поведения. Механизм возникновения этого риска неизвестен, а имеющиеся данные не исключают возможность существования повышенного риска при применении прегабалину.
В связи с этим необходимо тщательным образом наблюдать за пациентами для выявления признаков суицидального мышления и поведения и рассмотреть целесообразность назначения соответствующего лечения. В случае появления признаков суицидального мышления или поведения пациенты(но лица, которые присматривают за ними) должны обратиться за медицинской помощью.
Ухудшение функции нижних отделов желудочно-кишечного тракта.
После выхода препарата на рынок сообщалось о явлениях, связанных с ухудшением функции нижних отделов желудочно-кишечного тракта(такие как непроходимость кишечнику, паралитическая непроходимость кишечнику, запор), при применении прегабалину вместе с лекарственными средствами, которые могут вызывать запор, например опиоидними анальгетиками. При одновременном применении прегабалину и опиоида следует принять меры для профилактики запоров(особенно у женщин и пациентов пожилого возраста).
Неправильное приложение, злоупотребление или зависимость.
Сообщалось о случаях неправильного приложения, злоупотребления и зависимости. Следует с осторожностью применять препарат пациентам с злоупотреблением разными веществами в анамнезе; необходимо наблюдать за пациентом для выявления симптомов неправильного приложения, злоупотребления или зависимости от прегабалину(сообщалось о случаях развития привыкания, превышения назначенной дозы; поведения, направленного на получение препарата).
Энцефалопатия.
Сообщалось о случаях энцефалопатии, которые возникали преимущественно у пациентов с сопутствующими заболеваниями, которые могут спровоцировать энцефалопатию.
Непереносимость лактозы.
Препарат Лирика содержит лактозу. Пациентам с такими редкими наследственными заболеваниями, как непереносимость галактозы, лактазна недостаточность Лаппа или синдром мальабсорбции глюкозы и галактозы, не следует применять этот препарат.
Применение в период беременности или кормления груддю.
Женщины, способные забеременеть / средства контрацепции для женщин и мужчин.
Поскольку потенциальный риск для человека неизвестен, женщины, способные забеременеть, должны использовать эффективные средства контрацепции.
Беременность.
Надлежащие данные относительно применения прегабалину беременными женщинами отсутствуют.
В ходе исследований на животных была продемонстрирована репродуктивная токсичность. Потенциальный риск для человека неизвестен.
Препарат Лирика не следует применять в период беременности без неотложной надобности(когда польза для матери явно превышает возможный риск для плода).
Кормление груддю.
Небольшое количество прегабалину было выявлено в молоке женщин, которые кормят груддю. Следует сообщить женщинам, которые кормят груддю, что кормление груддю не рекомендуется во время применения прегабалину.
Фертильность.
Клинические данные относительно влияния прегабалину на фертильность женщин отсутствуют.
Во время клинического исследования из изучения влияния прегабалину на подвижность сперматозоидов здоровые добровольцы мужского пола применяли прегабалин в дозе 600 мг/сутки. После применения препарата в течение 3 месяцев ни одного влияния на подвижность сперматозоидов не выявлено.
В ходе исследования фертильности у самок крыс наблюдалось нежелательное влияние на репродуктивную функцию. В ходе исследования фертильности у самцов крыс наблюдалось нежелательное влияние на репродуктивную функцию и развитие. Клиническая значимость этих результатов неизвестна.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Лирика может оказывать незначительное или умеренное влияние на способность руководить транспортными средствами и работать с механизмами. Лирика может вызывать головокружение и сонливость и таким образом влиять на способность руководить транспортными средствами и работать с механизмами. В связи с этим пациентам следует рекомендовать воздерживаться от управления транспортными средствами, от работы со сложной техникой или от другой потенциально опасной деятельности, пока не станет известно, или влияет это лекарственное средство на их способность к такой деятельности.
Способ применения и дозы
Способ применения.
Препарат Лирика принимают независимо от приема еды.
Данное лекарственное средство предназначено исключительно для перорального приложения.
Дозы.
Диапазон доз препарата может изменяться в пределах 150-600 мг на сутки. Суточную дозу распределяют на 2 или 3 приемы.
Нейропатичний боль.
Терапию прегабалином можно начать с дозы 150 мг на сутки, распределенной на 2 или 3 приемы. В зависимости от индивидуального ответа и переносимости препарата пациентом дозу можно увеличить до 300 мг на сутки через 3-7 дни, а при необходимости - к максимальной дозе 600 мг на сутки еще после 7 дней.
Эпилепсия.
Терапию прегабалином можно начать с дозы 150 мг на сутки, распределенной на 2 или 3 приемы. В зависимости от индивидуального ответа и переносимости препарата пациентом дозу можно увеличить до 300 мг на сутки после первой недели лечения. Еще через одну неделю дозу можно увеличить к максимальной - 600 мг на сутки.
Генерализуемое тревожное расстройство.
Доза, которую распределяют на 2 или 3 приемы, может изменяться в пределах 150-600 мг на сутки. Периодически следует пересматривать необходимость продолжения терапии.
Терапию прегабалином можно начать с дозы 150 мг на сутки. В зависимости от индивидуального ответа и переносимости препарата пациентом дозу можно увеличить до 300 мг на сутки после первой недели лечения. После еще одной недели приема дозу можно увеличить до 450 мг на сутки. Еще через одну неделю дозу можно увеличить к максимальной - 600 мг на сутки.
Фибромиалгия.
Рекомендованная доза препарата для лечения фибромиалгии представляет от 300 до 450 мг на сутки. Лечение следует начинать из применения дозы 75 мг дважды на сутки(150 мг на сутки). В зависимости от эффективности и переносимости, дозу можно увеличивать до 150 мг дважды на сутки(300 мг на сутки) в течение одной недели. Для пациентов, для которых применение дозы 300 мг на сутки являются недостаточно эффективными, можно увеличить дозу до 225 мг дважды на сутки(450 мг на сутки). Хотя существует исследование применения дозы 600 мг на сутки, доказательств того, что применение этой дозы будет иметь дополнительное преимущество, нет; также такая доза имела худшую переносимость. Принимая во внимание дозозависимые побочные реакции, применения доз выше 450 мг на сутки не рекомендуется. Поскольку Лирика выводится главным образом почками, следует корректировать дозу препарата пациентам с нарушением функции почек.
Отмена прегабалину.
В соответствии с действующей клинической практикой, прекращать терапию прегабалином рекомендуется постепенно, в течение по меньшей мере одной недели, независимо от показаний(см. разделы "Особенности применения" и "Побочные реакции").
Нарушение функции почек.
Прегабалін выводится из системного кровотока в неизмененном виде, преимущественно почками. Поскольку клиренс прегабалину прямо пропорциональный клиренсу креатинина(см. раздел "Фармакокинетика"), уменьшать дозу пациентам с нарушением функции почек следует индивидуально как отмечено в таблице 1, в соответствии с клиренсом креатинина(CLcr), который определяют за формулой, :
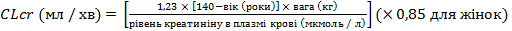
Прегабалін эффективно удаляется из плазмы крови с помощью гемодиализа(50 % препарату в течение 4 часов). Для пациентов на гемодиализе суточную дозу прегабалину следует корректировать в соответствии с функцией почек. Кроме суточной дозы, сразу после каждой 4-часовой процедуры гемодиализа необходимо применять дополнительную дозу препарата(см. таблицу 1).
Таблица 1. Коррекция дозы прегабалину в соответствии с функцией почек.
|
Клиренс креатинина(CLcr) (мл/хв) |
Общая суточная доза прегабалину * |
Режим дозирования |
|
|
Начальная доза(мг/сутки) |
Максимальная доза(мг/сутки) |
||
|
≥ 60 |
150 |
600 |
Дважды или трижды на сутки |
|
≥ 30 - < 60 |
75 |
300 |
Дважды или трижды на сутки |
|
≥ 15 - < 30 |
25-50 |
150 |
Раз или дважды на сутки |
|
< 15 |
25 |
75 |
Раз в сутки |
|
Дополнительная доза после гемодиализа(мг) |
|||
|
25 |
100 |
Однократная доза+ |
* Общую суточную дозу(мг/сутки) следует распределить на несколько приемов в соответствии с режимом дозирования, чтобы получить дозу для однократного приема(мг/дозу).
+ Дополнительная доза - это дополнительная однократная доза.
Печеночная недостаточность.
Для пациентов с нарушением функции печенки необходимости в коррекции дозы нет(см. раздел "Фармакокинетика").
Пациенты пожилого возраста.
Для пациентов пожилого возраста через ухудшение функции почек может понадобиться уменьшение дозы прегабалину(см. раздел "Особенности применения").
Деть.
Безопасность и эффективность препарата Лирика при его приложении детям в возрасте до 18 лет не установлены. Доступная на это время информация приведена в разделе "Побочные реакции", а также в разделах "Фармакодинамика" и "Фармакокинетика", однако, опираясь на их, невозможно предоставить никаких рекомендаций относительно дозирования этой категории пациентов.
Передозировка
После выхода препарата на рынок сообщалось, что самыми частыми побочными реакциями при передозировке прегабалину были сонливость, спутывание сознания, возбуждения и беспокойство. Также приходили сообщения о судорогах.
Редко сообщалось о случаях запятой.
Лечение передозировки прегабалину заключается в общих поддерживающих мероприятиях и при необходимости может включать гемодиализ(см. раздел "Способ применения и дозы", таблица 1).
Побочные реакции
В клинической программе из исследования прегабалину его получило свыше 8900 пациентов, из них 5600 - участники двойных слепых плацебо-контролируемых исследований. Самыми частыми зарегистрированными побочными реакциями были головокружение и сонливость. Побочные реакции обычно были легкой или умеренной степени. Во всех контролируемых исследованиях показатель отмены препарата через побочные реакции представлял 12 % среди пациентов, которые принимали прегабалин, и 5 % среди пациентов, которые получали плацебо. Самыми частыми побочными реакциями, которые приводили к прекращению применения препарата исследования в группе прегабалину были головокружение и сонливость.
Ниже приведены все побочные реакции, которые возникали чаще, чем при применении плацебо, и больше чем у одного пациента; эти побочные реакции перечислены за системами органов и за частотой: очень часто(≥ 1/10); часто(от ≥ 1/100 к < 1/10); нечасто(от ≥ 1/1000 к < 1/100); редко(от ≥ 1/10000 к < 1/1000); очень редко(< 1/10000); частота неизвестна(не может быть оценена на основе имеющихся данных). В каждой группе за частотой возникновения побочные эффекты представлены в порядке снижения степени их серьезности.
Отмеченные побочные реакции также могут быть связаны с течением основного заболевания и(или) сопутствующим применением других лекарственных средств.
Во время лечения нейропатичного боли центрального происхождения, вызванного поражением спинного мозга, увеличивалась частота побочных реакций в целом, частота побочных реакций со стороны ЦНС и особенно сонливость(см. раздел "Особенности применения").
Дополнительные побочные реакции, о которых сообщалось после выхода препарата на рынок, нижеприведены и обозначены курсивом.
Инфекции и инвазия.
Часто: назофарингит.
Нарушение со стороны крови и лимфатической системы.
Нечасто: нейтропения.
Нарушение со стороны иммунной системы.
Нечасто: гиперчувствительность.
Редко: ангионевротический отек, аллергические реакции, анафилактоидни реакции.
Нарушение обмена веществ, метаболизма.
Часто: повышение аппетита.
Нечасто: потеря аппетита, гипогликемия.
Со стороны психики.
Часто: эйфорическое настроение, спутывание сознания, раздражительность, дезориентация, бессонница, снижение либидо.
Нечасто: галлюцинации, панические атаки, беспокойство, возбуждение, депрессия, подавленное настроение, приподнятое настроение, агрессия, изменения настроения, деперсонализация, затрудненный отбор слов, патологические сновидения, усиления либидо, аноргазмия, апатия.
Редко: растормаживание.
Нарушение со стороны нервной системы.
Очень часто: головокружение, сонливость, головная боль.
Часто: атаксия, нарушение координации, тремор, дизартрия, амнезия, ухудшение памяти, нарушения внимания, парестезия, гипестезия, седативный эффект, нарушение равновесия, летаргия.
Нечасто: синкопе, ступор, миоклония, потеря сознания, психомоторная гиперактивность, дискинезия, постуральное головокружение, интенцийний тремор, нистагм, нарушение когнитивных функций, нарушения психики, расстройства вещания, гипорефлексия, гиперестезия, ощущение печиння, агевзия, общее недомогание, апатия, околоротовая парестезия, миоклонус.
Редко: судороги, паросмия, гипокинезия, дисфагия, гипалгезия, зависимость, мозочковий синдром, синдром зубчатого колеса, запятая, делирий, энцефалопатия, экстрапирамидный синдром, синдром Гієна-Барре, внутричерепная гипертензия, маниакальные реакции, параноидные реакции, расстройства сна.
Нарушение со стороны органов зрения.
Часто: нечеткость зрения, диплопия, конъюнктивит.
Нечасто: потеря периферического зрения, нарушения зрения, отек глаз, дефекты поля зрения, снижения остроты зрения, боль в глазах, астенопия, фотопсия, сухость в глазах, повышенное слезовиделение, раздражение глаз, блефарит, нарушение аккомодации, кровоизлияние в глаз, светобоязнь, отек сетчатки.
Редко: потеря зрения, кератит, осцилопсия, изменение зрительного восприятия глубины, мидриаз, страбизм, яркость зрения, анизокория, язвы роговицы, экзофтальм, паралич глазной мышцы, ирит, кератоконъюнктивит, миоз, ночная слепота, офтальмоплегия, атрофия зрительного нерва, отек диска зрительного нерва, птоз, увеит.
Нарушение со стороны органов слуха и равновесия.
Часто: вертиго.
Нечасто: гиперакузия.
Нарушение со стороны сердца.
Нечасто: тахикардия, атриовентрикулярная блокада первой степени, синусовая брадикардия, застойная сердечная недостаточность.
Редко: удлинение интервала QT, синусовая тахикардия, синусовая аритмия.
Нарушение со стороны сосудов.
Нечасто: артериальная гипотензия, артериальная гипертензия, приливы, гиперемия, ощущение холода в конечностях.
Нарушение со стороны дыхательной системы, грудной клетки и средостения.
Часто: фаринголарингеальний боль.
Нечасто: одышка, носовое кровотечение, кашель, заложенность носа, ринит, храп, сухость слизистой оболочки носа.
Редко: отек легких, сжатия в горле, ларингоспазм, апноэ, ателектаз, бронхиолит, икота, фиброз легких, зевоты.
Нарушение со стороны желудочно-кишечного тракта.
Часто: блюет, тошнота, запор, диарея, метеоризм, вздутие живота, сухость в рту, гастроэнтерит.
Нечасто: гастроезофагеальна рефлюксна болезнь, гиперсекреция слюны, гипестезия ротовой полости, холецистит, холелитиаз, колит, желудочно-кишечное кровотечение, мелена, отек языка, ректальное кровотечение.
Редко: асцит, панкреатит, отек языка, дисфагия, афтозный стоматит, язва пищевода, периодонтальный абсцесс.
Гепатобіліарні нарушения.
Нечасто: повышенный уровень печеночных ферментів*.
Редко: желтуха.
Очень редко: печеночная недостаточность, гепатит.
Нарушение со стороны кожи и подкожной ткани.
Часто: пролежни.
Нечасто: папулезное высыпание, крапивница, гипергидроз, зуд, аллопеция, сухость кожи, экзема, гирсутизм, язвы кожи, везикуло-бульозний сыпь.
Редко: синдром Стівенса-Джонсона, холодный пот, ексфолиативний дерматит, лихеноидний дерматит, меланоз, расстройства со стороны ногтей, петехиальний сыпь, пурпура, пустулярний сыпь, атрофия кожи, некроз кожи, кожные и подкожные узелки.
Нарушение со стороны опорно-двигательного аппарата и соединительной ткани.
Часто: мышечные судороги, артралгия, боль в спине, боль в конечностях, спазмы мышц шеи.
Нечасто: отек суставов, миалгия, посипування мышц, боль в шеи, скованность мышц.
Редко: рабдомиолиз.
Нарушение со стороны почек и мочевыводящих путей.
Нечасто: недержание мочи, дизурия, альбуминурия, гематурия, образование камней в почках, нефрит.
Редко: почечная недостаточность, олигурия, задержка мочи, острая почечная недостаточность, гломерулонефрит, пиелонефрит.
Нарушение половой системы и молочных желез.
Часто: эректильная дисфункция, импотенция.
Нечасто: половая дисфункция, задержка эякуляции, дисменорея, боль в молочных железах, лейкорея, меноррагия, метрорагия.
Редко: аменорея, выделение из молочных желез, увеличение молочных желез, гинекомастия, цервицит, баланит, эпидидимит.
Общие расстройства и реакции в месте введения.
Часто: периферический отек, отек, нарушение поступи, падения, ощущения опьянения, необычные ощущения, повышенная утомляемость.
Нечасто: генерализован отек, отек лица, скованность в груди, боль, жар, жажда, озноб, общая слабость, недомогание, абсцесс, воспаление жировой ткани, реакции фоточувствительности.
Редко: гранулема, преднамеренное причинение вреда, заочеревинний фиброз, шок.
Лабораторные исследования.
Часто: увеличение массы тела.
Нечасто: увеличение уровня креатинфосфокинази в крови, увеличение уровня глюкозы в крови, уменьшение количеству тромбоцитов, увеличения уровня креатинина в крови, уменьшение уровня калию у крови, уменьшения массы тела.
Редко: уменьшение уровня лейкоцитов в крови.
* Увеличение уровня аланинаминотрансферази(АЛТ) и аспартатаминотрансферази(АСТ).
У некоторых пациентов после прекращения краткосрочной или длительной терапии прегабалином наблюдались симптомы отмены препарата. Сообщалось о таких реакциях: бессонница, головная боль, тошнота, тревожность, диарея, гриппоподобный синдром, судороги, нервозность, депрессия, боль, гипергидроз и головокружения, которые указывают на физическую зависимость. Эту информацию следует сообщить пациенту перед началом терапии.
Даны относительно отмены прегабалину после длительного приложения указывают на то, что частота возникновения и степень тяжести симптомов отмены могут быть дозозависимыми.
Деть. Профиль безопасности прегабалину, установленный в ходе трех исследований, проведенных при участии педиатрических пациентов с парциальными судорожными нападениями со вторичным генерализованием или без нее(12-недельное исследование эффективности и безопасности у пациентов с парциальными судорожными нападениями, n=3D295; исследование фармакокинетики и переносимости препарата, n=3D65 и открытое исследование из изучения безопасности длительностью 1 год, n=3D54), был подобен профилю, который наблюдался в исследованиях у взрослых пациентов с эпилепсией. Наиболее распространенными побочными явлениями, которые наблюдались в 12-недельном исследовании терапии прегабалином, были сонливость, пирексия, инфекции верхних дыхательных путей, повышения аппетита, увеличения массы тела и назофарингит(см. разделы "Способ применения и дозы", "Фармакодинамика" и "Фармакокинетика").
Сообщение о подозреваемых побочных реакциях. Сообщение о подозреваемых побочных реакциях после регистрации лекарственного средства является важным. Это позволяет осуществлять непрерывный мониторинг соотношения пользы и риска при применении лекарственного средства.
Срок пригодности. 3 годы.
Условия хранения.
Не нуждается специальных условий хранения. Хранить в недоступном для детей месте.
Упаковка
Для капсул по 75 мг и 150 мг - по 14 или по 21 капсуле в блистере, по 1 или по 4 блистеры в картонной коробке.
Для капсул по 50 мг и 300 мг - по 21 капсуле в блистере, по 1 или по 4 блистеры в картонной коробке.
Категория отпуска
За рецептом.
Производитель
Пфайзер Менюфекчуринг Дойчленд ГмбХ/Pfizer Manufacturing Deutschland GmbH.
Местонахождение производителя и адрес места осуществления его деятельности
Бетрібштетте Фрайбург, Мусвальдаль 1, 79090 Фрайбург, Германия/
Betriebsstatte Freiburg, Mooswaldallee 1, 79090 Freiburg, Germany.
Другие медикаменты этого же производителя
Форма: лиофилизат для раствора для инъекций по 40 мг, 10 флаконы с лиофилизатом в картонной коробке
Форма: суспензия для инъекций, 150 мг/мл по 3,3 мл в флаконе; по 1 флакону в картонной коробке
Форма: лиофилизат для раствора для инъекций по 40 мг, 5 флаконы с лиофилизатом в комплекте с 5 ампулами растворителя по 2 мл(натрию хлорид, вода для инъекций) в картонной коробке
Форма: лиофилизат для раствора для инъекций по 100 мг; 1 флакон с лиофилизатом и 1 ампула с растворителем(спирт бензиловый, вода для инъекций) по 5 мл в картонной коробке
Форма: порошок и растворитель для раствора для инъекций по 500 мг, 1 флакон с порошком и 1 флакон с растворителем(спирт бензиловый(9 мг/мл), вода для инъекций), по 7,8 мл в картонной коробке