Новосевен®
Регистрационный номер: UA/5178/01/04
Импортёр: А/Т Ново Нордиск
Страна: ДанияАдреса импортёра: Ново Алле, ДК- 2880 Багсваерд, Данiя
Форма
порошок лиофилизированный для приготовления раствора для инъекций по 5 мг(250 КМО), 1 стеклянный флакон с лиофилизированным порошком в комплекте с 1 предварительно заполненным шприцем, который содержит 5 мл растворителя(гистидин, вода для инъекций), штоком поршня, переходником для флакона в индивидуальной упаковке в картонной коробке
Состав
1 флакон содержит 5 мг(250 КМО) ептакогу альфа(активированного)
Виробники препарату «Новосевен®»
Страна производителя: Дания
Адрес производителя: Ново Аллє, Багсваерд, 2880, Данiя(производитель действующего вещества, готового продукта и производитель, ответственный за выпуск серий готового продукта);
Страна производителя: Германия
Адрес производителя: Шутценштрасе, 87 и 99-101, 88212 Равенсбург, Германия(участок, на котором проводится изготовление растворителя в предварительно наполненном шприце и его первичная упаковка; участок производства, на котором проводится контроль/испытания растворителя в предварительно наполненном шприце);
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения препарата
НОВОСЕВЕН®
(NOVOSEVEN®)
Состав
действующее вещество: еptacog alfa(activated) (rFVIIa);
1 флакон содержит 2 мг(100 КMО) или 5 мг(250 КМО) ептакогу альфа(активированного);
вспомогательные вещества: натрию хлорид; кальцию хлорид, дигидрат; глицилглицин; полисорбат 80; метионин; сахароза; маннит(Е- 421).
После растворения 1 мл раствора содержит 10 мг сахарозы.
Растворитель: гистидин, вода для инъекций.
Врачебная форма. Порошок лиофилизированный и растворитель для приготовления раствора для инъекций.
Основные физико-химические свойства: лиофилизированный порошок белого цвета.
Фармакотерапевтична группа. Гемостатические средства. Факторы свертывания крови.
Код АТХ В02В D08.
Фармакологические свойства.
Фармакодинамика.
В состав препарата НовоСевен® входит активированный рекомбинантный VII фактор коагуляции с молекулярной массой ~50000 дальтон, выработанный методом генной инженерии с использованием как клетки-хозяина клеток почек новорожденных хомъячкив(ННХ-клітини). Механизм действия заключается в связывании фактора VІІа с тканевым фактором. Этот комплекс переводит факторы IX и Х в активную форму - ІХа и Ха, что вызывает превращение небольших количеств протромбина в тромбин. Тромбин в месте повреждения активирует тромбоциты, V и VIII факторы, которые вызывают превращение фибриногена в фибрин и образования гемостатического сгустку. Препарат НовоСевен® в фармакологических дозах независимо от тканевого фактора прямо активирует Х фактор непосредственно на поверхности активированных тромбоцитов, которые находятся в зоне повреждения. Это вызывает превращение большого количества протромбина в тромбин без участия тканевого фактора. Соответственно, фармакодинамична действие VIIа фактора заключается в локальном увеличении образования Ха фактора, тромбину и фибрину.
Теоретически нельзя полностью исключить генерализуемую активацию системы свертывания крови у больных, которые страдают заболеваниями, которые содействуют развитию дисеминованого внутрисосудистого свертывания(ДВЗ).
В неэкспериментальном реестре(F7HAEM - 3578), который включал случаи с врожденным дефицитом VII фактора, в 3 из 91 пациента, который прошел хирургическое вмешательство, были отмечены тромбоэмболические явления.
Фармакокинетика.
Здоровые добровольцыФармакокинетика препарата НовоСевен® исследовалась в 35 здоровых добровольцев европейской расы и японцев в ходе исследования с эскалацией дозы с использованием коагуляцийоного анализа FVII. Участники были стратифицированы за статью и этническим происхождением и получали дозы 40, 80 и 160 мкг препарату НовоСевен® на кг массы тела та/або плацебо(3 дозы). Фармакокінетичні профили были пропорциональными дозе. Фармакокинетика не зависела от пола и этнической группы. Средний объем распределения в равновесном состоянии колебался от 130 до 165 мл/кг, средние значения клиренса - от 33,3 до 37,2 мл/год х кг, а средний конечный период полувыведения - от 3,9 до 6 часов.
Гемофилия Но и В с наличием ингибиторовФармакокінетичні свойства препарата НовоСевен® с использованием FVII анализа исследовались в 12 детей(2-12 годы) и 5 взрослых пациентов при отсутствии кровотечения. Пропорциональность дозы изучалась у детей для исследуемых доз 90 и 180 мкг/кг массы тела в соответствии с полученными раньше данных при низших дозах(17,5-70 мкг/кг rFVIIa). Средний клиренс был приблизительно на 50 % выше у детей сравнительно с взрослыми(78 против 53 мл/год х кг), тогда как средний конечный период полувыведения был определен как 2,3 часы в обеих группах. Средний объем распределения в равновесном состоянии представлял 196 мл/кг у детей сравнительно с 159 мл/кг у взрослых. Очевидно, что клиренс связан с возрастом, потому у младших пациентов клиренс может расти больше чем на 50 %.
Дефицит фактора VIIФармакокинетика одноразового введения препарата НовоСевен® из расчета 15 и 30 мкг/кг массы тела существенно не различалась за значениями таких независимых от дозы показателей, как общий клиренс - 70,8-79,1 мл/год х кг, объем распределения в стационарном состоянии - 280 - 290 мл/кг, средняя длительность пребывания в кровотоци - 3,75-3,80 часы, время полувыведения - 2,82-3,11 часы. Среднее значение содержимого in vivo в плазме крови представляло ~ 20 % дозы, которая была введена.
Тромбастения ГланцманаФармакокинетику препарата НовоСевен® у больных тромбастенией Гланцмана не исследовали, однако можно допустить, что она существенно не отличается от фармакокинетики при гемофилии Но и В.
Даны из доклинической безопасности.
Все данные, полученные во время доклинических исследований из безопасности, были связаны с фармакологическим эффектом rFVIIa.
Потенциальный синергический эффект при комбинированном лечении с использованием rFXIII фактора и rFVIIa фактора был показан на экспериментальной сердечно-сосудистой модели у макак, что привело к значительному фармакологическому эффекту(тромбозу и смерти) при применении низших доз, чем при введении этих препаратов отдельно.
Клинические характеристики
Показание
Лечения кровотечений и их профилактика при хирургических вмешательствах или при других инвазивных процедурах у пациентов с такими заболеваниями:
· урожденная гемофилия с уровнем ингибиторов к факторам коагуляции VIII или IX > 5 BU;
· урожденная гемофилия с выраженной реакцией на введение факторов VIII или IX в анамнезе;
· приобретенная гемофилия;
· урожденный дефицит VII фактора;
· тромбастения Гланцмана с антителами к GP IIb - IIIa и/или HLA и резистентностью к переливанию тромбоцитов в прошлом или в данное время.
Противопоказание
Повышенная чувствительность к активному веществу или к любому вспомогательному веществу(см. раздел Состав(вспомогательные речевнини)), а также к белкам мышей, хомъячкив или коров.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Риск взаимодействия препарата НовоСевен® с концентратами факторов коагуляции неизвестен. Следует избегать одновременного применения концентратов протромбинового комплекса(активированного или неактивированного).
Введение антифибринолитикив больным гемофилией уменьшает кровопотерю при хирургических вмешательствах, особенно ортопедических или в участках с высокой фибринолитической активностью, например в ротовой полости. Однако опыт одновременного введения антифибринолитикив и препарата НовоСевен® ограничен.
В соответствии с данными доклиническими исследованиями(см. раздел "Даны из доклинической безопасности"), не рекомендуется совместимое применение VIIа фактора и фактора XIII.
Клинические данные относительно взаимодействия между VIIа фактором и фактором XIII отсутствуют.
Особенности применения
При патологических состояниях, когда тканевый фактор експресуеться более интенсивно, чем в норме, при введении препарата НовоСевен® может существовать потенциальный риск развития тромбоза или ДВЗ-синдрому. Подобная ситуация может возникнуть у больных с выраженным атеросклерозом, краш-синдромом, септицемией или ДВЗ синдромом.
Учитывая риск тромбоэмболических осложнений следует с осторожностью применять препарат НовоСевен® пациентам с ишемической болезнью сердца в анамнезе, заболеваниями печенки, после больших оперативных вмешательств, новорожденным или пациентам с риском тромбоэмболических феноменов или ДВЗ. В каждой из таких ситуаций потенциальная польза лечения препаратом НовоСевен® должна сравниваться с риском этих осложнений.
Поскольку препарат рекомбинантного фактора коагуляции VІІа НовоСевен® может содержать следы иммуноглобулинов G мышей и коров, а также других культуральных белков(сывороточные белки хомяков и коров), у больных, которые получают его, в отдаленный срок возникает опасность развития повышенной чувствительности к этим белкам. В таких случаях следует рассмотреть возможность внутривенного лечения антигистаминами.
При возникновении аллергических или анафилактических реакций следует немедленно прекратить применение препарата. При развитии шока следует прибегнуть к стандартному медицинскому лечению шока. Пациента следует проинформировать о ранних признаках реакций гиперчувствительности. При возникновении таких симптомов пациенту следует порекомендовать немедленно прекратить применение препарата и обратиться к врачу.
При тяжелых кровотечениях этот препарат следует вводить в лечебных учреждениях, которые специализируются на лечении больных гемофилией с наличием ингибиторов VIII или IX факторов, а при отсутствии такой возможности - в тесном сотрудничестве с врачом, который является специалистом по лечению гемофилии.
Если не удалось остановить кровотечение, больного обязательно госпитализируют. Больные или лица, которые оказывали им помощь, должны как можно быстрее информировать сотрудников лечебного учреждения обо всех инъекциях препарата НовоСевен®. У больных с дефицитом VII фактора перед и после введения препарата НовоСевен® следует определять протромбиновий время и активность VII фактора коагуляции. Если активность VIIа фактора не достигает ожидаемого уровня или введением доз, которые рекомендуются, не удается остановить кровотечение, можно допустить образование антител. В этих случаях необходимо определить их уровень.
Сообщалось о случаях тромбоза у больных с дефицитом VII фактора, что получали лечение препаратом НовоСевен® во время хирургических вмешательств, однако степень риска возникновения такого явления не выяснена(см. раздел "Фармакодинамика").
Пациентам с редкими наследственными проблемами непереносимости фруктозы, мальабсорбцией глюкозы или недостаточностью сахарозо-изомальтази не следует применять этот препарат.
Применение в период беременности или кормления груддю.
Беременность
Как предупредительного мероприятия рекомендуется избегать применение препарата НовоСевен® в течение беременности. Ограниченные даны о применении препарата в течение беременности за утвержденными показаниями свидетельствуют об отсутствии побочных влияний rFVIIа на ход беременности или на здоровье плода/новорожденного. На сегодня других соответствующих эпидемиологических данных нет. Исследования на животных свидетельствуют об отсутствии прямого или опосредствованного негативного влияния на беременность, развитие плода/эмбриона, роды или постнатальное развитие(см. раздел "Даны из доклинической безопасности").
Кормление груддю
Неизвестно, или попадает rFVIIа в грудное молоко человека. Экскреция rFVIIа в грудное молоко животных не исследовалась. Решение о продолжении/прекращения кормления груддю или терапии препаратом НовоСевен® следует принимать, учитывая преимущества кормления груддю для ребенка и терапии препаратом НовоСевен® для женщины.
Фертильность
Данные доклинических исследований, а также постмаркетинговые данные не свидетельствуют о негативном влиянии rFVIIa на фертильность мужчин или женщин.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Исследований эффекта препарата на способность влиять на скорость реакций при управлении автотранспортом или работе с другими механизмами не проводилось.
Способ применения и дозы
Лечение следует начинать под надзором врача, который имеет опыт лечения гемофилии та/або кровотечений.
Дозирование
Гемофилия А или В с наличием ингибиторов или приобретенная гемофилия
Доза
Препарат НовоСевен® следует вводить как можно быстрее после начала кровотечения. Начальную рекомендованную дозу вводят внутривенно(болюсно) из расчета 90 мкг(4,5 КМО) на кг массы тела.
После введения начальной дозы может возникнуть потребность в повторных введениях. Длительность лечения и интервалы между введениями варьируют в зависимости от тяжести кровотечению, виду инвазивной процедуры или оперативного вмешательства.
Дозирование для детей
Имеющийся клинический опыт свидетельствует об отсутствии в целом разницы между дозированием для взрослых и детей, хотя дети имеют более быстрый клиренс, чем взрослые. В связи с этим детям могут быть необходимы высшие дозы rFVIIa для достижения плазменной концентрации, подобной такой у взрослых пациентов(см. подразделение "Фармакокинетика").
Интервал между введениями
Сначала для достижения гемостазу препарат повторно вводят через 2-3 часы.
При необходимости продолжения лечения после достижения эффективного гемостазу введения повторяют через 4, 6, 8 или 12 часы столько, сколько будет нужно для лечения.
Легкие или умеренные кровотечения(в том числе при амбулаторном лечении)
В амбулаторных условиях раннее введение препарата оказывается эффективным при лечении слабых или умеренных кровоизлияний в суставах, мышцах, коже и слизистых оболочках. Можно рекомендовать две схемы введения препарата :
1) введение от двух до три дозы препарата из расчета 90 мкг/кг массы тела с интервалом в 3 часы и потом введения еще одной дозы для поддержки гемостазу;
2) введения одноразовой дозы препарата из расчета 270 мкг/кг массы тела.
Длительность амбулаторного лечения не должна превышать 24 часов.
Клинического опыта применения одноразовой дозы 270 мкг/кг массы тела пациентам пожилого возраста нет.
Тяжелые кровотечения
Рекомендуется вводить начальную дозу из расчета 90 мкг/кг массы тела во время транспортировки больной к больнице, где он обычно лечится. Величина следующих доз зависит от типа и тяжести кровотечения. Сначала препарат вводят каждый второй час к достижению улучшения клинического состояния больного. При необходимости продолжения лечения интервал между введениями увеличивают до 3 часов на 1-2 сутки. После этого на следующий период лечения интервал между введениями последовательно увеличивают до 4, 6, 8 или 12 часы. Тяжелые кровотечения иногда придется лечить в течение 2-3 недель и дольше(в зависимости от клинического состояния больного).
Инвазивные процедуры/оперативные вмешательства
Начальную дозу из расчета 90 мкг/кг массы тела вводят непосредственно перед вмешательством. Введения этой дозы повторяют через 2 часы, а потом в течение первых 24-48 часы - через 2-3 часы(в зависимости от объема вмешательства и клинического состояния больного). При больших хирургических вмешательствах препарат вводят через 2-4 часы в течение 6-7 суток. Дальше в течение 2 недель интервал между введениями увеличивают до 6-8 часов. Больных, которые перенесли большие оперативные вмешательства, лечат 2-3 недели к заживлению раны.
Приобретенная гемофилия
Доза и интервалы введения(в том числе при амбулаторном лечении)
НовоСевен® следует вводить как можно быстрее после начала кровотечения. Начальную рекомендованную дозу вводят внутривенно(болюсно) из расчета 90 мкг(4,5 КМО) на кг массы тела.
После введения начальной дозы может возникнуть потребность в повторных введениях. Длительность лечения и интервалы между введениями варьируют в зависимости от тяжести кровотечению, виду инвазивной процедуры или оперативного вмешательства.
Сначала препарат повторно вводят через 2-3 часы. При необходимости продолжения лечения после достижения эффективного гемостазу введения повторяют через 4, 6, 8 или 12 часы столько, сколько будет нужно для лечения.
Дефицит VII фактора
Доза, диапазон доз и интервалы введения
Диапазон рекомендованных доз для лечения кровотечений и их профилактика у больных, которой будут проводить оперативное вмешательство или инвазивные процедуры, представляет 15-30 мкг/кг массы тела каждые 4-6 часы к достижению гемостазу. Дозу и интервал введения подбирают индивидуально.
Тромбастения ГланцманаДоза, диапазон доз и интервалы введения
Диапазон рекомендованных доз для лечения кровотечений и их профилактика у больных, которой будут проводить оперативное вмешательство или инвазивные процедуры, представляет 90 мкг(от 80 до 120 мкг) /кг массы тела каждые 2 часы(1,5-2,5 часы). Для поддержания эффективного гемостазу следует ввести как минимум 3 дозы. Рекомендуется делать болюсни инъекции, поскольку медленное вливание может оказаться неэффективным. Для лечения тромбастении Гланцмана больным, которые не имеют резистентности, в первую очередь следует вводить тромбоциты.
Способ применения
Возобновляют раствор, как описано в инструкции для пользователя препарата НовоСевен®, и вводят в виде внутривенной болюсной инъекции в течение 2-5 минут.
Препарат НовоСевен® нельзя смешивать с инфузионными растворами или вводить крапельно.
Мониторинг лечения - лабораторные тестыПроведение мониторинга не является обязательным требованием, поскольку тяжесть кровотечения и клиническая реакция на введение препарата НовоСевен® определяют необходимость дальнейшего его введения.
После введения препарата НовоСевен® отмечено уменьшения значений протромбинового времени и активированного удельного тромбопластинового времени, однако при этом не были выявлены их корреляции с клинической эффективностью препарата.
НовоСевен®, инструкция для пользователя
Прежде чем использовать препарат НовоСевен®, внимательно прочитайте эту инструкцию
Препарат НовоСевен® поставляется в виде порошка. Перед инъекцией(введением) его необходимо развести растворителем, который добавляется в шприце. Растворитель - это раствор гистидина. Возобновленный препарат НовоСевен® должен быть введен в вену(внутривенная инъекция). Содержимое этой упаковки предназначено для разведения и введения препарата НовоСевен®.
Вам также понадобится инфузионный набор(трубка и игла-бабочка), спиртовые тампоны, марлевые салфетки и пластыре. Эти изделия медицинского назначения не входят в состав упаковки препарата НовоСевен®.
Не используйте оборудования без надлежащего инструктажа от врача или медсестры
Перед использованием всегда мойте руки и удостоверьтесь, что пространство вокруг вас чистое
Когда вы готовите и вводите лекарственное средство непосредственно в вену, очень важно
придерживаться правил асептики и антисептики. При неправильной технике вместе с инъекцией можно ввести микробов, которые могут инфицировать кровь.
Не открывайте оборудования, пока вы не готовы использовать его
Не используйте оборудования, если оно падало или повреждено Вместо этого используйте новую упаковку
Не используйте оборудования, если срок его пригодности закончился Вместо этого используйте новую упаковку Дата окончания срока пригодности напечатана после слов "Придатн к" на картонной коробке, на флаконе, переходнику для флакона и на предварительно заполненном шприце
Не используйте оборудования, если вы подозреваете, что оборудование загрязнено(контаминированный) Вместо этого используйте новую упаковку
Не выбрасывайте ни одной части набора, пока вы не ввели приготовленный раствор
Оборудование предназначено для одноразового использования
Содержимое
Эта упаковка содержит:
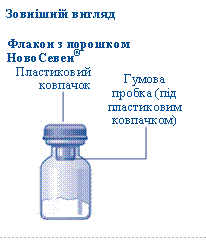
- 1 флакон с порошком НовоСевен®
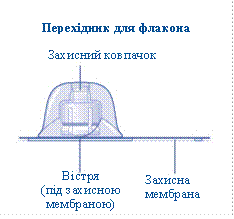
- 1 переходник для флакона
- 1 предварительно заполненный шприц с растворителем
- 1 шток поршня(находится под шприцем)
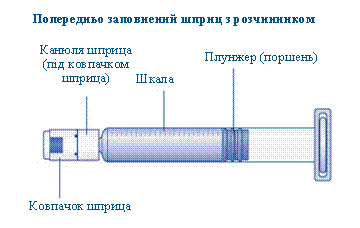

1 Подготовка флакона и шприца- Возьмите необходимое вам количество упаковок препарата НовоСевен®. - Проверьте срок пригодности. - Проверьте название, дозирование и цвет упаковки, чтобы убедиться, что вена содержит необходимый продукт. - Вымойте руки и высушите их чистым полотенцем или воздушной сушилкой. - Выньте флакон, переходник для флакона предварительно заполненный шприц из коробки. Оставьте шток поршня в коробке. - Нагрейте флакон и предварительно заполненный шприц к комнатной температуры(не выше 37° С). Вы можете сделать это держа их в руках, пока не почувствуете, что они такие же теплы, как и ваши руки. - Не используйте никакого другого способа подогрева флакона и предварительно заполненного шприца. |
|
|
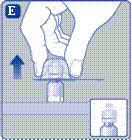
· Снимите пластиковый колпачок из флакона. Если пластиковый колпачок неплотно держится или отсутствует, не используйте флакон· Протрите спиртовым тампоном резиновую пробку и дайте ей высохнуть в течение нескольких секунд, прежде чем использовать, чтобы освободить ее от микроорганизмов, насколько это возможно. Не касайтесь резиновой пробки пальцами, поскольку это может привести к перенесению микроорганизмов |
|
· Снять защитную мембрану из переходника. Если герметичность защитной мембраны нарушена или она повреждена, не используйте переходник для флаконаНе вынимайте переходник для флакона из упаковки пальцами. Если вы коснетесь к острию переходника для флакона, это может привести к перенесению микроогранизмив из ваших пальцев. |
|
|
· Поставьте флакон на ровную и твердую поверхность. · Переверните защитный колпачок и под̓соединяйте переходник к флакону. · После присоединения не отсоединяйте переходник от флакона. |
|
но указательным пальцами, как показано на рисунке. Снимите защитный колпачок из переходника для флакона, но так, чтобы не вынуть переходник из флакона. |
|
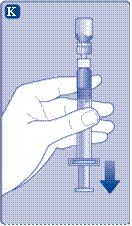
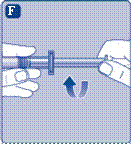
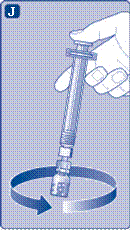
Возьмите шток шприца за широкий конец и выньте из коробки. Не касайтесь боковых поверхностей штока и переднего конца штока. Если вы коснетесь боковых поверхностей штока или переднего конца штока, это может привести к перенесению микроогранизмив из ваших пальцев. Сразу подсоедините шток поршня к поршню внутри предварительно заполненного шприца, возвращая его по часовой стрелке к упору. |
|
|
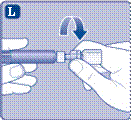
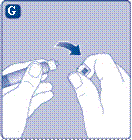
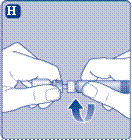
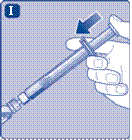
Удалите колпачок шприца из предварительно заполненного шприца сгибая его вниз, пока он не отломается за перфорацией. Не касайтесь канюле шприца под колпачком. Если вы коснетесь канюле шприца, это может привести к перенесению микроогранизмив из ваших пальцев. Если колпачок на шприце неплотно держится или отсутствует, не используйте этот предварительно заполненный шприц |
|
|
|
|
|
Не стряхивайте флакон - это приведет к образованию пены.
|
|
|
Используйте готовый раствор препарата НовоСевен® сразу, во избежание инфицирования. Не храните готовый раствор, не проконсультировавшись с врачом или медсестрой.
пока вы не получите необходимую вам дозу. |
|
|
|
Если вы коснетесь канюле шприца, это может привести к перенесению микроогранизмив из ваших пальцев. |
|
Введение препарата НовоСевен® из предварительно заполненного шприца через безголкове соединение для внутривенных катетеровПредостережение. Предварительно заполненный шприц изготовлен из стекла, и он есть совместимым со стандартным соединением "Луер-лок". Некоторые безголкови соединения с внутренним острием являются несовместимыми с предварительно заполненным шприцем. Эта несовместимость может привести до невозможности ввести препарат та/або к повреждению безголкового соединения. Следует придерживаться инструкции из использования безголкових соединений. При введении препарата с помощью безголкових соединений может быть необходимым вытянуть готовый раствор в стандартный одноразовый пластиковый шприц "Луер-лок" объемом 10 мл. Это необходимо выполнить сразу после шага J. |
|
|
5. Введение готового раствора Теперь препарат НовоСевен® готов для введения в виде внутривенной инъекции.
Инъекция раствора через центральный венозный катетер или подкожный порт :
|
|
|
Утилизация
|
|
Не разбирайте оборудования перед утилизациейНе используйте повторно оборудования. |
Деть.
Препарат применяют детям(см. раздел "Способ применения и дозы").
Передозировка
Дозолімітуюча токсичность препарата НовоСевен® в ходе клинических исследований не изучалась.
Об отдельных случаях передозировка сообщалась у пациентов с гемофилией. Единственным осложнением, о котором сообщалось в связи с передозировкой, было незначительное транзиторное повышение артериального давления у пациента возрастом 16 годы, который получил 24 мг rFVIIа вместо 5,5 мг.
О случаях передозировки у пациентов с приобретенной гемофилией или тромбастенией Гланцмана не сообщалось.
У пациентов с дефицитом фактора VII при рекомендованной дозе 15-30 мкг/кг rFVIIа один случай передозировки ассоциировал с тромботичним явлением(окципитальний инсульт) у пациента пожилого возраста(> 80 годы) мужского пола, который превысил рекомендованную дозу в 10-20 разы. Кроме того, формирование антител к препарату НовоСевену® и FVII было связано с передозировкой у одного пациента с дефицитом фактора VII.
Установленные дозы не должны превышать рекомендованные из-за отсутствия информации о возможном дополнительном риске.
Побочные реакции
Серьезные и несерьезные побочные реакции нижеприведены за системами классов органов и частотой.
Расстройства со стороны крови и лимфатической системы
Редко(≥ 1/10 000 к < 1/ 1000) - дисеминоване внутрисосудистое свертывание(ДВЗ) и связаны с этим лабораторные отклонения, включая повышение уровня D- димеру и снижение уровня АТ-ІІІ(см. раздел "Особенности применения"), коагулопатия.
Расстройства со стороны иммунной системы
Редко(≥ 1/10 000 к < 1/ 1000) - гиперчувствительность(см. разделы "Противопоказания" и "Особенности применения").
Частота неизвестна - анафилактические реакции.
Расстройства со стороны нервной системы
Редко(≥ 1/10 000 к < 1/1000) - головная боль.
Расстройства со стороны сосудистой системы
Редко(≥ 1/10 000 к < 1/1000) - артериальные тромбоэмболические явления(инфаркт миокарда, церебральный инфаркт, ишемия головного мозга, окклюзия сосудов головного мозга, инсульт, тромбоз артерии почки, ишемия периферических сосудов, периферический ишемический тромбоз и интестинальна ишемия), стенокардия.
Нечасто(≥ 1/1 000 к < 1/100) - венозные тромбоэмболические явления(тромбоз глубоких вен, тромбоз в месте внутривенного введения, легочная эмболия, тромбоэмболические явления печенки, включая тромбоз портальной вены, тромбоз вены почки, тромбофлебит, тромбофлебит поверхностных вен и интестинальна ишемия).
Частота неизвестна - тромбоз полостей сердца.
Расстройства со стороны желудочно-кишечного тракта
Редко(≥ 1/10 000 к < 1/1000) - тошнота.
Расстройства со стороны кожи и подкожных тканей
Нечасто(≥ 1/1 000 к < 1/100) - высыпание(включая аллергический дерматит и эритематозные высыпания), зуд и крапивница.
Частота неизвестна - приливы, ангионевротический отек.
Общие расстройства и состояние места введения
Нечасто(≥ 1/1 000 к < 1/100) - снижение терапевтического ответа*, лихорадка.
Редко(≥ 1/10 000 к < 1/1000) - реакции в месте инъекции, включая боль в месте инъекции.
Лабораторные исследования
Редко(≥ 1/10 000 к < 1/1000) - повышение уровня продуктов распада фибрина, повышения уровня аланинаминотрансферази, щелочной фосфатазы, лактатдегидрогенази, а также уровня протромбина.
В каждой группе частоты нежелательные эффекты представлены в порядке уменьшения их серьезности. Частота побочных эффектов, о которых сообщалось лишь в постмаркетинговом периоде(не в ходе клинических исследований), приводится как неизвестна.
* Сообщалось о случаях отсутствия эффекта или слабом влиянии препарата. Следует отметить, что важно придерживаться рекомендаций относительно дозирования, приведенных в разделе "Способ применения и дозы".
Тромбоэмболические явления могут приводить к остановке сердца.
Пациенты с приобретенной гемофилией.
Клинические исследования, проведенные при участии 61 пациента с приобретенной гемофилией(включали 100 эпизоды лечения), показали, что некоторые побочные реакции возникали чаще(1% от всех эпизодов лечения) : артериальные тромбоэмболические явления(окклюзия сосудов головного мозга, инсульт), венозные тромбоэмболические явления(легочная эмболия и тромбоз глубоких вен), стенокардия, тошнота, лихорадка, эритематозные высыпания, повышения уровня продуктов распада фибрина при лабораторных исследованиях.
Образование ингибуючих антител
По данным постмаркетинговых и клинических исследований, не было ни одного случая образования ингибуючих антител к препарату НовоСевен® или фактора VII у больных гемофилией В. ли В постмаркетинговых дослидженях сообщалось о случаях образования ингибуючих антител к препарату НовоСевен® у больных с урожденным дефицитом VII фактора.
Во время клинических исследований, проведенных при участии больных с дефицитом VII фактора, сообщалось только о такой побочной реакции, как образование антител к препарату НовоСевен® и фактора VII(часто: ≥ 1/100 к < 1/10). В некоторых случаях антитела в условиях in vitro вызывали ингибуючий эффект.
Факторы риска, которые могли способствовать образованию антител, включали предыдущее лечение человеческой плазмой та/або выделенной из нее VII фактором, тяжелые мутации гена фактора VII и передозировка препарата НовоСевен®. У больных с дефицитом VII фактора, что лечатся препаратом НовоСевен®, следует постоянно контролировать наличие антител к VII фактора(см. раздел "Особенности применения").
Тромбоэмболические явления
При применении препарата НовоСевен® за неутвержденными показаниями артериальные тромбоэмболические явления являются частыми(≥ 1/100 к < 1/10). Высший риск артериальных тромбоэмболических побочных явлений(см. выше "Расстройства со стороны сосудистой системы") (5,3 % у пациентов, которые лечились препаратом НовоСевен®, сравнительно с 2,8 % у пациентов, которые лечились плацебо) был продемонстрирован в метаанализе совокупных данных плацебо-контролируемых исследований, проведенных вне пределов утвержденных на данное время показаний в разных клинических группах, каждая из которых включала пациентов с разными характеристиками, а следовательно, и разный имеющийся профиль безопасности.
Безопасность и эффективность препарата НовоСевен® за пределами утвержденных показаний не установлены, потому в таких случаях препарат не рекомендуется.
Срок пригодности. 3 годы.
Условия хранения.
Хранить в недоступном для детей, защищенном от света месте, при температуре не выше 25 °С.
Не замораживать для предотвращения повреждения растворителя в шприце.
Доказана химическая и физическая стабильность растворенного препарата в течение 6 часов при 25 °С или 24 часов при 5 °С. С микробиологической точки зрения, продукт следует использовать сразу. Иначе за срок и условия хранения несет ответственность пользователь. Если растворение не проводилось в контролируемых и валидованих асептических условиях, срок хранения растворенного препарата не должен превышать 24 часы при 2-8 °С.
Несовместимость. НовоСевен® нельзя смешивать с инфузионными растворами или вводить крапельно.
Упаковка.
Каждая картонная коробка содержит 1 стеклянный флакон с белым порошком для приготовления раствора для инъекций, закрытый хлорбутиловой резиновой пробкой и закупорен алюминиевым колпачком с защитным съемным колпачком из полипропилена, и 1 предварительно заполненный шприц из стекла типа 1, что содержит 2 мл или 5 мл растворителя(гистидин, вода для инъекций).
Шприц закрыт с одной стороны колпачком из бромбутиловой резины и полипропилена, а из другого - поршнем из бромбутиловой резины и стопором из полипропилена. Также в комплекте к шприцу предоставляется шток поршня из полипропилена. Переходник для флакона в индивидуальной упаковке.
Категория отпуска. За рецептом.
Производитель.
А/Т Ново Нордіск/ Novo Nordisk A/S.
Местонахождение производителя и его адрес места осуществления деятельности
Ново Аллє, 2880 Багсваерд, Дания/ Novo Alle, 2880 Bagsvaerd, Denmark.
Другие медикаменты этого же производителя
Форма: суспензия для инъекций, 100 МО/мл по 10 мл в флаконе; по 1 флакону в картонной коробке
Форма: порошок лиофилизированный для приготовления раствора для инъекций по 5 мг(250 КМО), 1 стеклянный флакон с лиофилизированным порошком в комплекте с 1 предварительно заполненным шприцем, который содержит 5 мл растворителя(гистидин, вода для инъекций), штоком поршня, переходником для флакона в индивидуальной упаковке в картонной коробке
Форма: лиофилизат для раствора для инъекций по 1 мг(1 МО); 1 флакон с порошком в комплекте с растворителем(вода для инъекций по 1 мл в шприце № 1) в пластиковой коробке
Форма: таблетки по 2 мг по 15 таблетки в блистере; по 2 или 6 блистеры в картонной пачке
Форма: суспензия для инъекций, 100 МО/мл по 3 мл в картридже; по 1 картриджу в многодозовой одноразовой шприцевой ручке; по 1 или 5 шприцевые ручки в картонной коробке

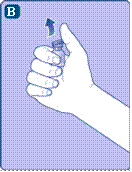
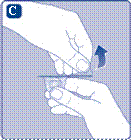
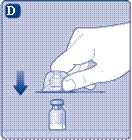
 Если необходима вам доза больше одного флакона, повторите шаги от А к J с дополнительными флаконами, переходниками для флаконов и предварительно заполненными шприцами
Если необходима вам доза больше одного флакона, повторите шаги от А к J с дополнительными флаконами, переходниками для флаконов и предварительно заполненными шприцами