Епайдра®
Регистрационный номер: UA/10240/01/01
- Состав
- Клинические характеристики
- Особенности применения
- Способ применения и дозы
- Передозировка
- Побочные реакции
- Несовместимость
- ИНСТРУКЦИЯ
- Инструкции относительно хранения
- Эксплуатация
- Стадия 1 Контроль инсулина
- Стадия 2 Присоединение иглы
- Стадия 4 Выбор дозы
- Стадия 5 Техника введения инъекции
- Стадия 6 Удаление и утилизация иглы
- Условия хранения
Импортёр: ООО "Санофи-Авентис Украина"
Страна: УкраинаАдреса импортёра: Украина, 01033, г. Киев, ул. Жилянская, 48-50А
Форма
раствор для инъекций, 100 ОТ/мл, № 5: по 3 мл в картридже; по 5 картриджи в блистерний упаковке в картонной коробке; № 5 : по 1 картриджу по 3 мл, вмонтированному в одноразовое устройство - шприц-ручку СолоСтар® (без игл для инъекций), по 5 шприцевые ручки в картонной коробке; № 1: по 10 мл в стеклянном флаконе; по 1 флакону в картонной коробке
Состав
1 мл раствора содержит инсулину глюлизину(продукту рекомбинантной ДНК-технологии с применением Escherichia coli) 100 единицы, что эквивалентно 3,49 мг; 1 картридж содержит 3 мл раствора для инъекций, что эквивалентно 300 Од. инсулину глюлизину; 1 шприц-ручка СолоСтар содержит 3 мл раствора для инъекций, что эквивалентно 300 Од. инсулину глюлизину; 1 флакон содержит 10 мл раствора для инъекций, что эквивалентно 1000 Од. инсулину глюлизину.
Виробники препарату «Епайдра®»
Страна производителя: Германия
Адрес производителя: Индустрипарк Хьохст-Брюнингштрассе 50, Н500, Н590, Н600, H785, H790, Франкфурт-на-Майни, Гессен, 65926, Германия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
ЕПАЙДРА®
(APIDRA®)
Состав
действующее вещество: инсулин глюлизин;
1 мл раствора содержит инсулину глюлизину(продукту рекомбинантной ДНК-технологии с применением Escherichia coli) 100 единицы, что эквивалентно 3,49 мг;
1 картридж содержит 3 мл раствора для инъекций, что эквивалентно 300 Од. инсулину глюлизину;
вспомогательные вещества: м-крезол, натрию хлорид, трометамин, полисорбат 20, кислота хлористоводородная концентрированная, натрию гидроксид, вода для инъекций.
Врачебная форма. Раствор для инъекций.
Основные физико-химические свойства: прозрачный бесцветный водный раствор.
Фармакотерапевтична группа. Противодиабетические средства. Инсулины и аналоги быстрого действия.
Код АТX А10А В06.
Фармакологические свойства.
Фармакодинамика. Инсулин глюлизин является рекомбинантным аналогом инсулина человека, что за своей силой действия подобный инсулину человека. Инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека.
Основное действие инсулинов и их аналогов, включая инсулин глюлизин, направленная на регулирование метаболизма глюкозы. Инсулины снижают уровень содержимого глюкозы в крови путем стимуляции периферийной утилизации глюкозы, особенно в скелетных мышцах и жировой ткани, и притеснение синтеза глюкозы в печенке. Инсулин предотвращает липолиз в адипоцитах, протеолизу и усиливает синтез протеина.
Исследования при участии здоровых добровольцев и больных сахарным диабетом продемонстрировали, что при подкожном введении инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека. Если инсулин глюлизин применяется в виде инъекции подкожно, снижение уровня глюкозы в крови начинается в течение 10-20 минут. При применении подкожно инсулина глюлизину и обычного инсулина человека в дозе 0,15 От/кг в разное время относительно 15-минутного стандартного приема еды было установлено, что при введении инсулина глюлизину при условии введения за 2 минуты до приема еды наблюдается постпрандиальний гликемичний контроль, подобный такому при введении обычного инсулина человека, который применялся за 30 минуты до приму еде. При сравнении гипогликемичних эффектов инсулина глюлизину и обычного инсулина человека при введенные за 2 минуты до приема еды инсулин глюлизин обеспечивал лучший постпрандиальний контроль, чем обычный инсулин человека. Применение инсулина глюлизину через 15 минуты после начала приема еды обеспечивает гликемичний контроль, подобный такому при применении обычного инсулина человека, который введен за 2 минуты до начала приема еды.
Ожирение.
Инсулин глюлизин сохраняет свои быстродействующие свойства в рпзи приложение пациентам с ожирением. Время до достижения 20 % общей AUC и показатель AUC(0-2 часы), который является показателями раннего действия инсулинов относительно снижения уровня глюкозы, равнялись соответственно 114 мин. и 427 мг/кг для инсулина глюлизину, 121 мин. и 354 мг/кг для инсулина лиспро, 150 мин. и 197 мг/кг для обычного инсулина человека.
Раса и пол.
В ходе контролируемых клинических исследований при участии взрослых пациентов инсулин глюлизин не продемонстрировал разницу в безопасности и эффективности в подгруппах, которые отличались за расой и статью.
Фармакокинетика.
Более быстрая абсорбция инсулина глюлизину обеспечивается заменой аминокислоты аспарагина в позиции В3 инсулина человека лизином и лизину в позиции В29 глютаминовой кислотой.
Абсорбция и биодоступность.
Фармакокінетичні профили у здоровых добровольцев и больных сахарным диабетом (И или
ІІ типа) продемонстрировали, что уровень абсорбции инсулина глюлизину был в два раза более высокий, а максимальная концентрация, приблизительно в два раза более высокая сравнительно с таким у обычного инсулина человека.
У больных сахарным диабетом И типа после подкожной инъекции в дозе 0,15 От/кг показатели Тмакс для инсулина глюлизину равнялись 55 мин. и Смакс был 82 ± 1,3 µОт/мл сравнительно с Тмакс, 82 мин. и Смакс 46 ± 1,3 µОт/мл для обычного инсулина человека. Среднее время наличия в организме инсулина глюлизину было короче(98 мин.), чем обычного инсулина человека(161 мин.).
У больных сахарным диабетом ІІ типа после подкожного применения инсулина глюлизину в дозе 0,2 От/кг Смакс представляет 91µОт/мл с интервалом достоверности от 78 до 104 µОт/мл.
При подкожной инъекции инсулина глюлизину в брюшную стенку, бедро или дельтообразную мышцу абсорбция препарата является более скорой при применении в участок стенки живота, чем в бедро. Абсорбция в месте инъекции в участке дельтообразной мышцы была средней между вышеупомянутыми показателями. Абсолютная биодоступность(70 %) инсулина глюлизину была подобной в вышеупомянутых местах инъекций и имела низкую индивидуальную вариативнисть(11 % CV). Внутривенное болюсне применение инсулина глюлизину было причиной большего системного влияния сравнительно с такими при подкожной инъекции, причем значение Сmax было приблизительно в 40 разы больше.
Распределение и выведение.
Распределение и выведение инсулина глюлизину и обычного человеческого инсулина после внутривенного введения является подобным, при этом объемы распределения представляют 13 л и 22 л, а периоды полувыведения - 13 хв и 18 хв соответственно.
После подкожного приложения инсулин глюлизин выводится быстрее, чем обычный инсулин человека, со средней длительностью периодов полувыведения 42 хв для инсулина глюлизину сравнительно с 86 хв для обычного инсулина. При анализе перекрестного исследования инсулина глюлизину при участии здоровых добровольцев или больных сахарным диабетом
И или ІІ типа средняя длительность периода полувыведения была от 37 до 75 минут(интервал достоверности).
Инсулин глюлизин, как и человеческий инсулин, плохо связывается с белками плазмы крови.
Особенности применения препарата специфическим группам пациентов
· Пациенты с нарушениями функции почек.
При нарушении функции почек потребность в инсулине может снижаться, однако способность инсулина глюлизину быстро действовать хранится.
· Пациенты с нарушениями функции печенки.
Фармакокінетичні свойства инсулина глюлизину не исследовались у пациентов с нарушением функции печенки.
· Пациенты пожилого возраста.
Относительно пациентов пожилого возраста, больных сахарным диабетом, существует очень ограниченная база данных относительно фармакокинетики препарата.
· Дети и подростки.
Фармакокінетичні и фармакодинамични свойства инсулина глюлизину у детей(7-11 годы) и подростков(12-16 годы), больных сахарным диабетом И типа, такие: инсулин глюлизин быстро усваивается у больных обеих возрастных групп и имеет такие же показатели Тмакс и Смакс, как и у взрослых. Введение инсулина глюлизину непосредственно перед приемом еды детям и подросткам обеспечивает лучший постпрандиальний гликемичний контроль сравнительно с обычным инсулином человека, как и у взрослых больных. Отклонение уровня глюкозы(AUC) представляет 641 мг/год/дл для инсулина глюлизину и 801 мг/год/дл для обычного инсулина человека.
Доклинические данные относительно безопасности применения
Доклинические данные не указывают на наличие токсичности(кроме той, которая связана с гипогликемией), которая бы отличалась от показателей обычного инсулина человека или была клинически значимой для людей.
Клинические характеристики
Показание.
Сахарный диабет, когда необходимое применение инсулина взрослым, подросткам и детям в возрасте от 6 лет и старше.
Противопоказание.
Гиперчувствительность к инсулину глюлизину или любого компонента препарата. Гипогликемия.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий.
Исследования относительно типов фармакокинетичних взаимодействий не проводились. Учитывая эмпирические знания относительно других подобных лекарственных средств, проявление клинически релевантных фармакокинетичних взаимодействий является маловероятным.
На метаболизм глюкозы влияет целый ряд веществ и лекарственных препаратов. Следовательно, это может нуждаться регулирования дозы инсулина глюлизину и особенно тщательного надзора за больным.
К веществам, которые могут усилить глюкозознижувальну активность и увеличить восприимчивость к гипогликемии, принадлежат пероральные антидиабетические средства, ингибиторы ангиотензинпревращающего фермента, дизопирамид, фибрати, флуоксетин, ингибиторы моноаминоксидази, пентоксифиллин, пропоксифен, салицилаты и сульфаниламидные антибиотики.
Вещества, которые могут привести к росту уровня глюкозы в крови, : кортикостероиды, даназол, диазоксид, диуретики, глюкагон, изониазид, производные фенотиазину, соматропин, симпатомиметические агенты(такие как, эпинефрин [адреналин], сальбутамол, тербуталин), тиреоидные гормоны, естрогени, прогестини(например, в составе пероральных контрацептивов), ингибиторы протеинази и антипсихотические лекарственные средства(в частности оланзапин и клозапин) атипизма.
Блокаторы Беты, клонидин, соли лития или алкоголь могут привести как к повышению, так и к снижению свойства инсулина уменьшать уровень глюкозы в крови. Пентамідин может вызывать развитие гипогликемии, которая иногда сопровождается гипергликемией.
Кроме того, под воздействием симпатолитичних лекарственных средств, таких как клонидин, гуанетидин, резерпин, и блокаторов беты признака адренергического обратного регулирования могут быть ослаблены или даже отсутствуют.
Особенности применения
Переход пациента на применение нового типа или препарата инсулина должно происходить под тщательным надзором врача. Изменения силы действия, типа препарату(производителя), вида препарата(обычный, НПХ, ленте, длительного действия и тому подобное), происхождения(животный, человеческий, аналог человеческого инсулина) та/або метода производства могут нуждаться изменения дозы. Также может возникать необходимость в регулировании схемы сопутствующего применения пероральных антидиабетических препаратов.
Гипергликемия.
Применение несоответственно доз или прекращение лечения, особенно у больных инсулинозависимым диабетом, может привести к развитию гипергликемии и диабетического кетоацидоза - состояниям, которые являются потенциально летальными.
Гипогликемия.
Гипогликемия возникает в зависимости от профиля действия инсулинов, которые применяются, и может изменяться при переходе на новый режим лечения.
Условия, которые могут сделать ранние предупредительные симптомы гипогликемии нетипичными или менее выраженными, включают значительную длительность заболевания на диабет, интенсивную инсулинотерапию, диабетическую нейропатию, применение лекарственных препаратов, таких как блокаторы беты, или переход из инсулина животного происхождения на инсулин человека. Потребность в коррекции дозы также может возникнуть, если пациенты повышают режим физической активности или изменяют свою обычную пищевую диету. Физические нагрузки сразу после еды повышают риск развития гипогликемии.
Гипогликемия после инъекции быстродействующих аналогов инсулина, как правило, возникает раньше, чем при применении растворимого инсулина человека.
Гипогликемические или гипергликемични реакции, если не предоставить пациенту соответствующей помощи, могут привести к потере сознания, запятой или летального следствия.
Потребность в инсулине может изменяться при наличии другой болезни или эмоциональных нарушений.
Приходили сообщения об ошибочном введении препаратов, когда вместо инсулина глюлизину случайно вводились другие инсулины, в частности инсулины длительного действия. Перед каждой инъекцией следует проверять информацию на этикетке картриджа, во избежание ошибочного введения вместо инсулина глюлизину других инсулинов.
Одна доза этого лекарственного средства содержит меньше чем 1 ммоль(23 мг) натрию, то есть он практически не содержит натрия.
Епайдра® содержит м-крезол, который может повлечь аллергические реакции.
Комбинация препарата Епайдра® из пиоглитазоном.
О случаях сердечной недостаточности сообщалось при применении пиоглитазону в сочетании из инсулином, особенно у пациентов, которые имеют риск развития сердечной недостаточности. Это нужно учитывать при рассмотрении возможности проведения лечения комбинацией пиоглитазону и препарату Епайдра®. При применении этой комбинации за пациентами нужно наблюдать относительно появления признаков и симптомов сердечной недостаточности, увеличения массы тела и отека. При любом ухудшении кардиологических симптомов применения пиоглитазону нужно прекратить.
Применение в период беременности или кормления груддю.
Беременность
Даны относительно применения инсулина глюлизину беременным женщинам отсутствуют или ограничены(меньше чем 300 результаты беременности).
В ходе исследований влияния на репродуктивную функцию, проведенных на животных, не было выявлено никаких отличий между применением инсулина глюлизину и инсулина человека относительно влияния на беременность, развитие эмбриона/плода, роды или постнатальное развитие(см. раздел "Фармакологические свойства").
Беременным женщинам этот препарат следует применять с осторожностью. Необходимо тщательным образом контролировать уровень глюкозы.
Пациентам с диагностированным или гестационным сахарным диабетом в период беременности следует поддерживать надлежащий метаболический контроль. Потребность организма в инсулине может уменьшаться в первом триместре беременности и, как правило, увеличивается в период второго и третьего триместров. Сразу после родов потребность организма в инсулине быстро уменьшается.
Кормление груддю
Неизвестно, или екскретуеться инсулин глюлизин в грудное молоко человека, однако обычно инсулин не проникает в грудное молоко и не абсорбируется после перорального приема.
Женщинам, которые кормят груддю, может быть необходимо откорректировать дозу инсулина и рацион питания.
Фертильность
В ходе исследований влияния інсулінy глюлізинy на репродуктивную функцию, проведенных на животных, не было выявлено никаких нежелательных влияний на фертильность.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Способность пациента концентрировать внимание и его реакция могут нарушаться вследствие развития гипогликемии или гипергликемии или, например, в результате нарушения зрения. Это может представлять риск в ситуациях, когда наличие таких симптомов является особенно важным(в частности, во время управления автомобилем или механизмами).
Пациентам следует рекомендовать быть осторожными и предотвращать развитие гипогликемии во время управления транспортом. Это особенно важно для тех, кто недостаточно поинформирован или вовсе не поинформирован относительно симптомов-предсказателей гипогликемии, и для тех больных, у кого часто возникают эпизоды гипогликемий. При этих обстоятельствах следует рассмотреть целесообразность управления транспортом.
Способ применения и дозы
Сила действия этого препарата выражается в единицах, которые используются исключительно для препарата Епайдра® и отличаются от МО или единиц, в которых выражается сила действия других аналогов инсулина.
Препарат Епайдра® можно применять в режимах инсулинотерапии, которые включают инсулин среднего или долговременного действия, или аналог базального инсулина, и можно применять одновременно с пероральными противодиабетическими средствами.
Дозу препарата Епайдра® подбирают и регулируют индивидуально.
Особенные категории пациентов.
Пациенты с нарушениями функции почек.
Фармакокінетичні свойства инсулина глюлизину в целом хранятся у пациентов с нарушением функции почек. Однако в случае нарушения функции почек потребность в инсулине может снижаться(см. раздел "Фармакокинетика").
Пациенты с нарушениями функции печенки.
Фармакокінетичні свойства инсулина глюлизину не изучались у пациентов со сниженной функцией печенки. У пациентов с нарушением функции печенки потребность в инсулине может быть меньшей через снижение глюконеогенеза и способности инсулина метаболизуватися.
Пациенты пожилого возраста.
Имеются даны из фармакокинетики инсулина у пациентов пожилого возраста, больных сахарным диабетом является недостаточными. Ухудшение функции почек может привести к снижению потребности в инсулине.
Дети и подростки.
Не существует достоверной клинической информации относительно применения препарата Епайдра® детям в возрасте до 6 лет.
Применение.
Препарат Епайдра® следует вводить путем подкожной инъекции незадолго до или сразу после приема еды или путем постоянной подкожной инфузии с помощью инсулинового насоса.
Препарат Епайдра® применяют подкожно в участке брюшной стенки, бедра или дельтообразной мышцы или путем непрерывной инфузии под кожу передней стенки живота. Места для инъекций или инфузий в зоне инъекции(передняя стенка брюшной полости, бедро или дельтообразная мышца) следует по очереди изменять. Степень абсорбции и, вероятно, начало и срок действия могут зависеть от определенного места инъекции, техники ее исполнения и других переменных показателей. Подкожная инъекция в брюшную стенку обеспечивает немного более быструю абсорбцию, чем введение препарата в другие места для инъекций.
Необходимо следить за тем, чтобы не повреждать кровеносные сосуды. После введения препарата не следует массажировать места инъекции.
Пациентов следует учить придерживаться правильной процедуры выполнения инъекции.
Епайдра®, раствор для инъекций в картриджах, предназначенный для использования с инсулиновыми шприцевыми ручками OптіПен, КлікСтар, Аутопен 24, Тактіпен или AllStarTM, в соответствии с рекомендациями, которые содержатся в инструкции производителя прибора. Картриджи нельзя применять в других шприцевых ручках многократного использования, поскольку точность дозирования была определена только для отмеченных шприцевых ручек.
Не все из этих шприцевых ручек могут быть имеются в вашей стране.
Следует четко придерживаться инструкций производителя относительно использования шприцевой ручки во время заправки картриджа, присоединения иглы и проведения инъекции инсулина. Перед использованием картридж нужно тщательным образом осмотреть. Он пригоден к применению, если раствор в нем прозрачен, бесцветен, не содержит видимых твердых частей. Картридж следует держать в течение 1-2 часов при комнатной температуре перед установлением его в шприц-ручку многократного использования. Волдырьки воздуха следует удалить из картриджа перед выполнением инъекции(см. инструкцию для использования шприцевой ручки). Пустые картриджи не позволяется заполнять повторно.
В случае неисправности шприцевой ручки(смотрите инструкцию из использования шприцевой ручки) раствор из картриджа можно набрать в шприц, который подходит для введения инсулина и рассчитан на 100 Од./мл, и сделать инъекцию. Если шприц-ручка для введения инсулина повреждена или не работает должным образом(через механические дефекты), ее следует уничтожить, а вместо нее использовать новую шприц-ручку.
С целью предотвращения инфицирования шприц-ручка для многократного использования используется лишь одним пациентом.
Перед каждой инъекцией следует проверять информацию, отмеченную на этикетке, во избежание ошибочного введения вместо инсулина глюлизину других инсулинов(см. раздел "Особенности применения").
Смешивание с другими инсулинами.
Препарат Епайдра®, который вводится в виде подкожной инъекции, запрещается смешивать с любыми другими лекарственными средствами, кроме человеческого инсулина НПХ(нейтрального протамина Хагедорна). При смешивании из НПХ - инсулином человека сначала следует набрать в шприц препарат Епайдра®. Инъекцию нужно делать сразу же после смешивания, поскольку надлежащих данных относительно стабильности смесей, приготовленных задолго до введения, нет.
Деть. Данных относительно клинического применения препарата Епайдра® детям в возрасте до 6 лет недостаточно.
Передозировка
Гипогликемия может возникать как следствие чрезмерного действия инсулина относительно объема принятой еды и расходов энергии.
Специфические данные относительно передозировки инсулина глюлизину отсутствуют. Однако гипогликемия может развиться постепенно.
Умеренные гипогликемические эпизоды могут лечиться путем перорального применения глюкозы или сахара. Таким образом, больному сахарным диабетом рекомендуется постоянно мать при себе несколько кусочков сахара, конфет, печенья или фруктового сока с сахаром. Цукрозамінники нельзя использовать для лечения гипогликемических состояний.
Тяжелые гипогликемические эпизоды, при которых пациент теряет сознание, можно устранять путем введения глюкагону(0,5-1 мг) внутримышечно или подкожно, что может сделать соответствующим образом проинструктированное лицо, или путем внутривенного введения глюкозы, которая должна выполнить медицинский работник. Глюкоза вводится внутривенно также в случае, если состояние пациента не улучшается в течение 10 или 15 хв после введения глюкагону.
Когда больной очнется, рекомендуется применить углеводы перорально с целью предотвращения рецидива гипогликемии.
После инъекции глюкагону пациента следует обследовать в больнице для выявления причины возникновения тяжелой гипогликемии и предотвращения возникновения подобных нападений.
Побочные реакции
Самым распространенным косвенным действием инсулинотерапии является гипогликемия, которая возникает как следствие применения значительно больше дозы инсулина, чем это нужно.
Соответствующие побочные реакции, продемонстрированные во время проведения клинических исследований, приводятся ниже за классами систем органов и в порядке уменьшения частоты возникновения : очень часто(≥ 1/10); часто(≥ 1/100 - < 1/10); нечасто(≥ 1/1 000 - < 1/100); редко(≥ 1/10 000 - < 1/1 000); очень редко(< 1/10 000), частота неизвестна(нельзя рассчитать по имеющимся данным).
В каждой из групп побочные явления представленные в порядке уменьшения степени их серьезности.
|
Класс органов и систем MedDRA |
Очень часто |
Часто |
Нечасто |
Редко |
|
Метаболические и алиментарные расстройства |
Гипогликемия |
|||
|
Расстройства со стороны кожи и подкожных тканей |
Реакции в месте инъекции местные реакции гиперчувствительности |
Липодистрофия |
||
|
Нарушение общего положения и реакции в месте введения |
Системные реакции гипер-чутливости |
Метаболические и алиментарные расстройства.
Симптомы гипогликемии, как правило, возникают внезапно. Они включают холодный пот, холодную бледную кожу, утомляемость, нервозность или тремор, ощущение беспокойства, необычную утомляемость или слабость, смущение, нарушение концентрации внимания, сонливость, сильное чувство голода, нарушения зрения, головную боль, тошноту и сильное сердцебиение. Гипогликемия может достичь значительной степени и привести к потере сознания та/або судорог и повлечь временное или постоянное нарушение функции мозга или даже стать причиной летального следствия.
Расстройства со стороны кожи и подкожных тканей.
Местные реакции гиперчувствительности(покраснение, отек и зуд в месте инъекции) возможны во время лечения с применением инсулина. Такие реакции, как правило, являются преходящими и обычно исчезают в случае продолжения лечения.
Липодистрофия может возникать в месте инъекции как следствие несоблюдения порядка изменения места инъекции.
Нарушение общего положения и реакции в месте введения.
Cистемні реакции гиперчувствительности могут включать крапивницу, сжатие в груди, одышку, аллергический дерматит и зуд. Тяжелые случаи включают генерализуемую аллергическую реакцию вместе с анафилактической реакцией, которая может угрожать жизни.
Срок пригодности. 2 годы.
Срок пригодности после первого использования - 4 недели.
Условия хранения.
Хранить в недоступном для детей месте. Хранить в холодильнике при температуре от +2 ºС до +8 ºС. Не замораживать. Хранить картридж во внешней картонной упаковке с целью защиты от действия света. Не допускать контакта со стенками холодильника.
Условия хранения во время пользования.
Начатые картриджи необходимо использовать в течение 4 недель.
Хранить при температуре не выше +25 ºС во внешней картонной упаковке с целью защиты от действия света. Перед установлением картриджа в шприц-ручку многократного использования картридж необходимо хранить при комнатной температуре в течение 1-2 часов.
Несовместимость
Препарат Епайдра® не следует смешивать с другими препаратами, отличными за составом от НПХ(нейтрального протамина Хагедорна) инсулина человека.
Упаковка. № 5: по 3 мл в картридже; по 5 картриджи в блистерний упаковке в картонной коробке.
Категория отпуска. За рецептом.
Производитель. Санофі-Авентіс Дойчланд ГмбХ, Германия/ Sanofi - Aventis Deutschland GmbH, Germany.
Местонахождение производителя и его адрес места осуществления деятельности.
Індустріпарк Хьохст-Брюнінгштрассе 50 H500, H590, Н600, Н785, Н790, Франкфурт-на-Майні, Гессен, 65926, Германия / Industriepark Hоеchst - Brueningstrasse 50 H500, H590, Н600, H785, H790, Frankfurt am Main, Hessen, 65926, Germany.
Заявитель. ООО "Санофі-Авентіс Украина", Украина/ Sanofi - Aventis Ukraine LLC, Ukraine.
ИНСТРУКЦИЯ
для медицинского применения лекарственного средства
ЕПАЙДРА®
(APIDRA®)
Состав
действующее вещество: инсулин глюлизин;
1 мл раствора содержит инсулину глюлизину(продукту рекомбинантной ДНК-технологии с применением Escherichia coli) 100 единицы, что эквивалентно 3,49 мг;
1 шприц-ручка СолоСтар® содержит 3 мл раствора для инъекций, что эквивалентно 300 Oд. инсулину глюлизину;
вспомогательные вещества: м-крезол, натрию хлорид, трометамин, полисорбат 20, кислота хлористоводородная концентрированная, натрию гидроксид, вода для инъекций.
Врачебная форма. Раствор для инъекций.
Основные физико-химические свойства: прозрачный бесцветный водный раствор.
Фармакотерапевтична группа. Противодиабетические средства. Инсулины и аналоги быстрого действия. Код АТС А10А В06.
Фармакологические свойства.
Фармакодинамика. Инсулин глюлизин является рекомбинантным аналогом инсулина человека, что за своей силой действия подобный инсулину человека. Инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека.
Основное действие инсулинов и их аналогов, включая инсулин глюлизин, направленная на регулирование метаболизма глюкозы. Инсулины снижают уровень содержимого глюкозы в крови путем стимуляции периферийной утилизации глюкозы, особенно в скелетных мышцах и жировой ткани, и притеснение синтеза глюкозы в печенке. Инсулин предотвращает липолиз в адипоцитах, протеолизу и усиливает синтез протеина.
Исследования при участии здоровых добровольцев и больных сахарным диабетом продемонстрировали, что при подкожном введении инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека. Если инсулин глюлизин применяется в виде инъекции подкожно, снижение уровня глюкозы в крови начинается в течение 10-20 минут. При применении подкожно инсулина глюлизину и обычного инсулина человека в дозе 0,15 От/кг в разное время относительно 15-минутного стандартного приема еды было установлено, что при введении инсулина глюлизину при условии введения за 2 минуты до приема еды наблюдается постпрандиальний гликемичний контроль, подобный такому при введении обычного инсулина человека, который применялся за 30 минуты до приму еде. При сравнении гипогликемичних эффектов инсулина глюлизину и обычного инсулина человека при введенные за 2 минуты до приема еды инсулин глюлизин обеспечивал лучший постпрандиальний контроль, чем обычный инсулин человека. Применение инсулина глюлизину через 15 минуты после начала приема еды обеспечивает гликемичний контроль, подобный такому при применении обычного инсулина человека, который введен за 2 минуты до начала приема еды.
Ожирение.
Инсулин глюлизин сохраняет свои быстродействующие свойства в рпзи приложение пациентам с ожирением. Время до достижения 20 % общей AUC и показатель AUC(0-2 часы), который является показателями раннего действия инсулинов относительно снижения уровня глюкозы, равнялись соответственно 114 мин. и 427 мг/кг для инсулина глюлизину, 121 мин. и 354 мг/кг для инсулина лиспро, 150 мин. и 197 мг/кг для обычного инсулина человека.
Раса и пол.
В ходе контролируемых клинических исследований при участии взрослых пациентов инсулин глюлизин не продемонстрировал разницу в безопасности и эффективности в подгруппах, которые отличались за расой и статью.
Фармакокинетика.
Более быстрая абсорбция инсулина глюлизину обеспечивается заменой аминокислоты аспарагина в позиции В3 инсулина человека лизином и лизину в позиции В29 глютаминовой кислотой.
Абсорбция и биодоступность.
Фармакокінетичні профили у здоровых добровольцев и больных сахарным диабетом (И или
ІІ типа) продемонстрировали, что уровень абсорбции инсулина глюлизину был в два раза более высокий, а максимальная концентрация, приблизительно в два раза более высокая сравнительно с таким у обычного инсулина человека.
У больных сахарным диабетом И типа после подкожной инъекции в дозе 0,15 От/кг показатели Тмакс для инсулина глюлизину равнялись 55 мин. и Смакс был 82 ± 1,3 µОт/мл сравнительно с Тмакс, 82 мин. и Смакс 46 ± 1,3 µОт/мл для обычного инсулина человека. Среднее время наличия в организме инсулина глюлизину было короче(98 мин.), чем обычного инсулина человека(161 мин.).
У больных сахарным диабетом ІІ типа после подкожного применения инсулина глюлизину в дозе 0,2 От/кг Смакс представляет 91µОт/мл с интервалом достоверности от 78 до 104 µОт/мл.
При подкожной инъекции инсулина глюлизину в брюшную стенку, бедро или дельтообразную мышцу абсорбция препарата является более скорой при применении в участок стенки живота, чем в бедро. Абсорбция в месте инъекции в участке дельтообразной мышцы была средней между вышеупомянутыми показателями. Абсолютная биодоступность(70 %) инсулина глюлизину была подобной в вышеупомянутых местах инъекций и имела низкую индивидуальную вариативнисть(11 % CV). Внутривенное болюсне применение инсулина глюлизину было причиной большего системного влияния сравнительно с такими при подкожной инъекции, причем значение Сmax было приблизительно в 40 разы больше.
Распределение и выведение.
Распределение и выведение инсулина глюлизину и обычного человеческого инсулина после внутривенного введения является подобным, при этом объемы распределения представляют 13 л и 22 л, а периоды полувыведения - 13 хв и 18 хв соответственно.
После подкожного приложения инсулин глюлизин выводится быстрее, чем обычный инсулин человека, со средней длительностью периодов полувыведения 42 хв для инсулина глюлизину сравнительно с 86 хв для обычного инсулина. При анализе перекрестного исследования инсулина глюлизину при участии здоровых добровольцев или больных сахарным диабетом
И или ІІ типа средняя длительность периода полувыведения была от 37 до 75 минут(интервал достоверности).
Инсулин глюлизин, как и человеческий инсулин, плохо связывается с белками плазмы крови.
Особенности применения препарата отдельным группам пациентов
· Пациенты с нарушениями функции почек.
При нарушении функции почек потребность в инсулине может снижаться, однако способность инсулина глюлизину быстро действовать хранится.
· Пациенты с нарушениями функции печенки.
Фармакокінетичні свойства инсулина глюлизину не исследовались у пациентов с нарушением функции печенки.
· Пациенты пожилого возраста.
Относительно пациентов пожилого возраста, больных сахарным диабетом, существует очень ограниченная база данных относительно фармакокинетики препарата.
· Дети и подростки.
Фармакокінетичні и фармакодинамични свойства инсулина глюлизину у детей(7-11 годы) и подростков(12-16 годы), больных сахарным диабетом И типа, такие: инсулин глюлизин быстро усваивается у больных обеих возрастных групп и имеет такие же показатели Тмакс и Смакс, как и у взрослых. Введение инсулина глюлизину непосредственно перед приемом еды детям и подросткам обеспечивает лучший постпрандиальний гликемичний контроль сравнительно с обычным инсулином человека, как и у взрослых больных. Отклонение уровня глюкозы(AUC) представляет 641 мг/год/дл для инсулина глюлизину и 801 мг/год/дл для обычного инсулина человека.
Доклинические данные относительно безопасности применения
Доклинические данные не указывают на наличие токсичности(кроме той, которая связана с гипогликемией), которая бы отличалась от показателей обычного инсулина человека или была клинически значимой для людей.
Клинические характеристики
Показание. Сахарный диабет, когда необходимое применение инсулина взрослым, подросткам и детям в возрасте от 6 лет и старше.
Противопоказание.
Гиперчувствительность к инсулину глюлизину или к любому компоненту препарата. Гипогликемия.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Исследования относительно типов фармакокинетичних взаимодействий не проводились. Учитывая эмпирические знания относительно других подобных лекарственных средств, проявление клинически релевантных фармакокинетичних взаимодействий является маловероятным.
На метаболизм глюкозы влияет целый ряд веществ и лекарственных препаратов. Следовательно, это может нуждаться регулирования дозы инсулина глюлизину и особенно тщательного надзора за больным.
К веществам, которые могут усилить глюкозознижувальну активность и увеличить восприимчивость к гипогликемии, принадлежат пероральные антидиабетические средства, ингибиторы ангиотензинпревращающего фермента, дизопирамид, фибрати, флуоксетин, ингибиторы моноаминоксидази, пентоксифиллин, пропоксифен, салицилаты и сульфаниламидные антибиотики.
Вещества, которые могут привести к росту уровня глюкозы в крови, : кортикостероиды, даназол, диазоксид, диуретики, глюкагон, изониазид, производные фенотиазину, соматропин, симпатомиметические агенты(такие как, эпинефрин [адреналин], сальбутамол, тербуталин), тиреоидные гормоны, естрогени, прогестини(например, в составе пероральных контрацептивов), ингибиторы протеинази и антипсихотические лекарственные средства(в частности, оланзапин и клозапин) атипизма.
Блокаторы Беты, клонидин, соли лития или алкоголь могут привести как к повышению, так и к снижению свойства инсулина уменьшать уровень глюкозы в крови. Пентамідин может вызывать развитие гипогликемии, которая иногда сопровождается гипергликемией.
Кроме того, под воздействием симпатолитичних лекарственных средств, таких как клонидин, гуанетидин, резерпин, и блокаторов беты признака адренергического обратного регулирования могут быть ослаблены или даже отсутствуют.
Особенности применения
Переход пациента на применение нового типа или препарата инсулина должно происходить под тщательным надзором врача. Изменения силы действия, типа препарату(производителя), вида препарата(обычный, НПХ, ленте, длительного действия и тому подобное), происхождения(животный, человеческий, аналог человеческого инсулина) та/або метода производства могут нуждаться изменения дозы. Также может возникать необходимость в регулировании схемы сопутствующего применения пероральных антидиабетических препаратов.
Гипергликемия.
Применение несоответственно доз или прекращение лечения, особенно у больных инсулинозависимым диабетом, может привести к развитию гипергликемии и диабетического кетоацидоза - состояниям, которые являются потенциально летальными.
Гипогликемия.
Гипогликемия возникает в зависимости от профиля действия инсулинов, которые применяются, и может, таким образом, изменяться при переходе на новый режим лечения.
Условия, которые могут сделать ранние предупредительные симптомы гипогликемии нетипичными или менее выраженными, включают значительную длительность заболевания на диабет, интенсивную инсулинотерапию, диабетическую нейропатию, применение лекарственных препаратов, таких как блокаторы беты, или переход из инсулина животного происхождения на инсулин человека. Потребность в коррекции дозы также может возникнуть, если пациенты повышают режим физической активности или изменяют свою обычную пищевую диету. Физические нагрузки сразу после еды повышают риск развития гипогликемии.
Гипогликемия после инъекции быстродействующих аналогов инсулина, как правило, возникает раньше, чем при применении растворимого инсулина человека. Гипогликемические или гипергликемични реакции, если не предоставить пациенту соответствующей помощи, могут привести к потере сознания, запятой или летального следствия.
Потребность в инсулине может изменяться при наличии другой болезни или эмоциональных нарушений.
Приходили сообщения об ошибочном введении препаратов, когда вместо инсулина глюлизину случайно вводились другие инсулины, в частности инсулины длительного действия. Перед каждой инъекцией следует проверять информацию на этикетке, во избежание ошибочного введения вместо инсулина глюлизину других инсулинов.
Одна доза этого лекарственного средства содержит меньше чем 1 ммоль(23 мг) натрию, то есть он практически не содержит натрия.
Епайдра® содержит м-крезол, который может повлечь аллергические реакции.
Комбинация препарата Епайдра® из пиоглитазоном.
О случаях сердечной недостаточности сообщалось при применении пиоглитазону в сочетании из инсулином, особенно у пациентов, которые имеют риск развития сердечной недостаточности. Это нужно учитывать при рассмотрении возможности проведения лечения комбинацией пиоглитазону и препарату Епайдра®. При применении этой комбинации за пациентами нужно наблюдать относительно появления признаков и симптомов сердечной недостаточности, увеличения массы тела и отека. При любом ухудшении кардиологических симптомов применения пиоглитазону нужно прекратить.
Применение в период беременности или кормления груддю.
Беременность
Даны относительно применения инсулина глюлизину беременным женщинам отсутствуют или ограничены(меньше чем 300 результаты беременности).
В ходе исследований влияния на репродуктивную функцию, проведенных на животных, не было выявлено никаких отличий между применением инсулина глюлизину и инсулина человека относительно влияния на беременность, развитие эмбриона/плода, роды или постнатальное развитие(см. раздел "Фармакологические свойства").
Беременным женщинам этот препарат следует применять с осторожностью. Необходимо тщательным образом контролировать уровень глюкозы.
Пациентам с диагностированным или гестационным сахарным диабетом в период беременности следует поддерживать надлежащий метаболический контроль. Потребность организма в инсулине может уменьшаться в первом триместре беременности и, как правило, увеличивается в период второго и третьего триместров. Сразу после родов потребность организма в инсулине быстро уменьшается.
Кормление груддю
Неизвестно, или екскретуеться инсулин глюлизин в грудное молоко человека, однако обычно инсулин не проникает в грудное молоко и не абсорбируется после перорального приема.
Женщинам, которые кормят груддю, может быть необходимо откорректировать дозу инсулина и рацион питания.
Фертильность
В ходе исследований влияния інсулінy глюлізинy на репродуктивную функцию, проведенных на животных, не было выявлено никаких нежелательных влияний на фертильность.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Способность пациента концентрировать внимание и его реакция могут нарушаться вследствие развития гипогликемии или гипергликемии или, например, в результате нарушения зрения. Это может представлять риск в ситуациях, когда наличие таких симптомов является особенно важным(в частности, во время управления автомобилем или механизмами).
Пациентам следует рекомендовать быть осторожными и предотвращать развитие гипогликемии во время управления транспортом. Это особенно важно для тех, кто недостаточно поинформирован или вовсе не поинформирован относительно симптомов-предсказателей гипогликемии, и для тех больных, у кого часто возникают эпизоды гипогликемии. При этих обстоятельствах следует рассмотреть целесообразность управления транспортом.
Способ применения и дозы
Сила действия этого препарата выражается в единицах, которые применяются исключительно для препарата Епайдра® и отличаются от МО или единиц, в которых выражается сила действия других аналогов инсулина.
Препарат Епайдра® применяют в режимах инсулинотерапии, которые включают инсулин среднего или долговременного действия, или аналог базального инсулина и можно использовать одновременно с пероральными гипогликемическими средствами.
Дозу препарата Епайдра® подбирают и регулируют индивидуально.
Особенные категории пациентов.
Пациенты с нарушениями функции почек.
Фармакокінетичні свойства инсулина глюлизину в целом хранятся у пациентов с нарушением функции почек. Однако в случае нарушения функции почек потребность в инсулине может снижаться(см. раздел "Фармакокинетика").
Пациенты с нарушениями функции печенки.
Фармакокінетичні свойства инсулина глюлизину не изучались у пациентов со сниженной функцией печенки. У пациентов с нарушением функции печенки потребность в инсулине может быть меньшей через снижение глюконеогенеза и способности инсулина метаболизуватися.
Пациенты пожилого возраста.
Имеются даны из фармакокинетики инсулина у пациентов пожилого возраста, больных сахарным диабетом, является недостаточными. Ухудшение функции почек может привести к снижению потребности в инсулине.
Дети и подростки.
Не существует достоверной клинической информации относительно применения препарата Епайдра® детям в возрасте до 6 лет.
Применение.
Препарат Епайдра® следует вводить путем подкожной инъекции незадолго до или сразу после приема еды или путем постоянной подкожной инфузии с помощью инсулинового насоса.
Препарат Епайдра® применяют подкожно в участок брюшной стенки, бедра или дельтообразной мышцы, или путем непрерывной инфузии под кожу передней стенки живота. Места для инъекций или инфузий в зоне инъекции(передняя стенка брюшной полости, бедро или дельтообразная мышца) следует по очереди изменять. Степень абсорбции и, вероятно, начало и срок действия могут зависеть от определенного места инъекции, техники ее исполнения и других переменных показателей. Подкожная инъекция в брюшную стенку обеспечивает немного более быструю абсорбцию, чем введение препарата в другие места для инъекций.
Необходимо следить за тем, чтобы не повреждать кровеносные сосуды. После введения препарата не следует массажировать место инъекции. Пациентов следует учить придерживаться правильной процедуры выполнения инъекций.
Смешивание с другими инсулинами.
Инсулин глюлизин не следует смешивать с другими лекарственными средствами, кроме человеческого инсулина НПХ(нейтрального протамина Хагедорна).
ИНСТРУКЦИЯ
из использования шприцевой ручки CолоСтар®
Перед первым приложением шприц-ручку следует выдержать при комнатной температуре в течение 1-2 часов.
Проверьте картридж перед его использованием. Его можно применять лишь тогда, когда раствор в нем является прозрачным, бесцветным, без видимых твердых частиц и имеет такую же консистенцию, как и вода. Поскольку Епайдра® является раствором, она не нуждается ресуспендування перед применением.
Пустые шприцевые ручки нельзя использовать опять, их нужно должным образом уничтожить.
Чтобы предотвратить инфицирование, каждая предварительно наполненная шприц-ручка должна использоваться лишь одним лицом.
Перед каждой инъекцией следует проверять информацию на этикетке, во избежание ошибочного введения вместо инсулина глюлизину других инсулинов(см. раздел "Особенности применения").
Схематическое изображение шприцевой ручки СолоСтар®
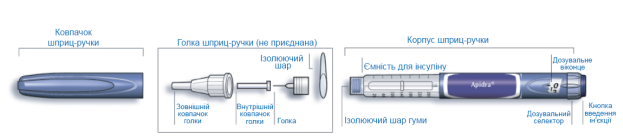
Важная информация для использования шприцевой ручки СолоСтар®:
- Для каждой инъекции используйте новую иглу, совместимую исключительно с шприцевой ручкой СолоСтар®. Не избирайте дозу и не нажимайте кнопку введения, если игла не присоединена к шприцевой ручке.
- Тест на безопасность выполняйте перед каждой инъекцией.
- Шприц-ручка назначен лично Вам, и не следует передавать ее другим лицам.
- Если инъекцию Вам вводит другое лицо, это лицо должен принимать специальные меры безопасности для предотвращения несчастных случаев, связанных с применением иглы и перенесением инфекции.
- Не используйте шприц-ручку СолоСтар® в случае повреждения или при наличии сомнений относительно правильности ее функционирования.
- Всегда необходимо иметь запасную шприц-ручку СолоСтар® на случай потери или повреждения.
Инструкции относительно хранения
Внимательно ознакомьтесь с информацией относительно хранения шприцевой ручки СолоСтар®.
Если Ваша шприц-ручка СолоСтар® хранится в холодильнике, выньте ее оттуда за
1-2 часы перед введением препарата, чтобы он нагрелся к комнатной температуре. Инъекционное введение охлажденного инсулина является более болезненным.
Использованная шприц-ручка СолоСтар® подлежит уничтожению согласно установленным правилам.
Эксплуатация
Оберегайте шприц-ручку СолоСтар® от пыли и грязи.
Очистить внешне шприц-ручку СолоСтар® можно, протирая ее влажной тканью.
Не окунайте в жидкость, не промывайте и не смазывайте шприц-ручку, поскольку этим Вы можете повредить ее.
СолоСтар® предназначен для аккуратной и безопасной работы.
Его необходимо использовать с осторожностью. Избегайте ситуаций, при которых возможное повреждение шприцевой ручки СолоСтар®. Если Вы подозреваете, что шприц-ручка СолоСтар® повреждена, используйте новую шприц-ручку.
Стадия 1 Контроль инсулина
A. Внимательно прочитайте информацию на этикетке шприцевой ручки СолоСтар® для того, чтобы убедиться в введении соответствующего инсулина. Шприц-ручка СолоСтар® из Епайдрою® синего цвета, кнопка для введения препарата - темно-синего цвета с рельефным кольцом в верхней части.
B. Снимите колпачок шприцевой ручки.
C. Проконтролируйте внешний вид инсулина. Епайдра® является прозрачным инсулином. Не используйте шприц-ручку СолоСтар®, если инсулин мутен, окрашен или имеет посторонние части.
Стадия 2 Присоединение иглы
Для каждой инъекции всегда применяйте новую стерильную иглу. Это поможет предотвратить загрязнение, а также возможное засорение иглы.
А. Снимите защитную этикетку из контейнера иглы.
В. Установите иглу на одной линии с шприцевой ручкой, а потом содержите на одной прямой к ее присоединению(навинчивают или насаждают в зависимости от типа иглы).
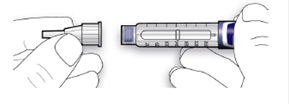
· Если игла не находится на одной линии с шприцевой ручкой в момент присоединения, это может привести к нарушению изолирующего слоя резины и повлечь истекание жидкости или перелом иглы.
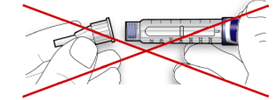
Стадия 3 Выполнение теста на безопасность
Во всех случаях выполняйте тест на безопасность перед каждой инъекцией. Этим Вы обеспечиваете получение точной дозы благодаря:
· проверке того, что шприц-ручка и игла функционируют нормально;
· удалению волдырьков воздуха.
A. Отмеряйте дозу, которая равняется 2 единицам, возвращая дозировочный селектор.
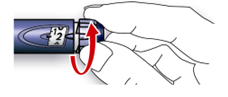
B. Снимите внешний колпачок из иглы и храните его, чтобы потом поместить у него использованную после введения инъекции иглу. Снимите внутренний колпачок из иглы и выбросьте его.
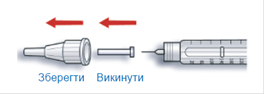
C. Разместите шприц-ручку иглой вверх.
D. Кончиками пальцев постучите осторожно по емкости для инсулина, чтобы все волдырьки воздуха поднялись вверх в направлении иглы.
E. Нажмите на кнопку введение инъекции к упору. Проверьте, или появляется инсулин на кончике иглы.
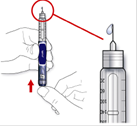
Вы можете провести испытание на безопасность несколько раз, пока не появится инсулин.
· Если инсулин не появился, проведите контроль наличия волдырьков воздуха и повторно проведите испытание на безопасность больше два раза к их удалению.
· Если появления инсулина не наблюдается, это может быть вызвано блокированием иглы. Снимите иглу и повторите испытание.
· Если появления инсулина не наблюдается потом замены иглы, Ваша шприц-ручка СолоСтар® может быть испорчена. Не используйте ее.
Стадия 4 Выбор дозы
Вы можете установить дозу с точностью до 1 единицы(от минимальной дозы 1 единица к максимальной дозе 80 единицы). Если Вам необходимо ввести дозу, которая превышает 80 единицы, нужно ввести 2 или больше инъекции.
A. Проверьте, чтобы дозировочное окошко показывало "0" по завершению испытания на безопасность.
B. Выберите необходимую Вам дозу (на нижеследующем примере избранная доза представляет
30 единицы). Если Вы установили дозу, которая превышает необходимую, следует повернуть дозировочный селектор в начальное положение.
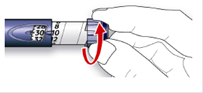
· Не нажимайте на кнопку введения инъекции во время вращения селектора, иначе инсулин вытечет.
· Вы не сможете повернуть дозировочный селектор к числу единиц, которое превышает количество, которое осталось в шприцевой ручке. Не пытайтесь силой повернуть дозировочный селектор. В этом случае Вы должны или ввести остаток инсулина и дополнить необходимую Вам дозу с помощью новой шприцевой ручки СолоСтар®, или использовать новую шприц-ручку СолоСтар® для введения полной дозы.
Стадия 5 Техника введения инъекции
А. Придерживайтесь техники введения инъекции, с которой Вас ознакомил врач.
В. Введите иглу в кожу.
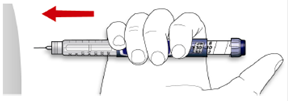
С. Введите дозу с помощью нажатия на кнопку введения инъекции к упору в одном направлении. После введения инъекции в дозировочном окошке должен установиться "0".

Д. Оставьте кнопку введения инъекции в нажатом положении. Медленно считайте к
10 перед вытягиванием иглы из кожи. При этом обеспечивается введение полной дозы.
Стадия 6 Удаление и утилизация иглы
Во всех случаях удаляйте иглу после каждой инъекции и храните шприц-ручку без прикрепленной иглы. Этим обеспечивается профилактика:
· загрязнение та/або попадание инфекции;
· попадание воздуха к емкости для инсулина и истекания инсулина, который может привести к неправильному дозированию.
A. Насадите внешний колпачок иглы обратно на иглу и используйте его для свинчивания иглы из шприцевой ручки. Для снижения риска несчастных случаев, связанных с применением иглы, никогда не насаждайте назад внутренний колпачок иглы.
· Если введение препарата было осуществлено другим лицом, специальные меры безопасности при удалении и утилизации иглы употребляются этим же лицом. Придерживайтесь рекомендованных мер безопасности для удаления и утилизации игл(например техники насаждания колпачка одной рукой) для снижения риска несчастных случаев, связанных с применением иглы, а также перенесения инфекционных заболеваний.
B. Осторожно выбросьте иглу(согласно инструкциям врача).
C. Во всех случаях помещайте колпачок обратно на шприц-ручку и храните шприц-ручку к следующей инъекции.
Деть. Данных относительно клинического применения препарата Епайдра® детям в возрасте до 6 лет недостаточно.
Передозировка
Гипогликемия может возникать как следствие чрезмерного действия инсулина относительно объема употребленной еды и расходов энергии.
Специфические данные относительно передозировки инсулина глюлизину отсутствуют. Однако гипогликемия может развиться постепенно.
Умеренные гипогликемические эпизоды можно лечить путем перорального применения глюкозы или сахара. Поэтому больному сахарным диабетом рекомендуется постоянно мать при себе несколько кусочков сахара, конфет, печенья или фруктового сока с сахаром.
Цукрозамінники нельзя применять для лечения гипогликемических состояний!
Тяжелые гипогликемические эпизоды, при которых пациент теряет сознание, можно устранить с помощью введения глюкагону(0,5-1 мг) внутримышечно или подкожно, что может сделать соответствующим образом проинструктированное лицо, или с помощью внутривенного введения глюкозы, что должен выполнить медицинский работник. Глюкозу вводят внутривенно также в случае, если состояние пациента не улучшается в течение 10-15 хв после введения глюкагону.
Когда больной очнется, рекомендуется применение углеводов перорально с целью предотвращения рецидива гипогликемии.
После инъекции глюкагону пациента следует обследовать в больнице для выявления причины возникновения тяжелой гипогликемии и предотвращения возникновения подобных нападений.
Побочные реакции
Самым распространенным косвенным действием инсулинотерапии является гипогликемия, которая возникает как следствие применения большей дозы инсулина, чем это нужно.
Соответствующие побочные реакции, продемонстрированные во время проведения клинических исследований, приводятся ниже за классами систем органов и в порядке уменьшения частоты возникновения : очень часто(≥ 1/10); часто(≥ 1/100 - < 1/10); нечасто(≥ 1/1 000 - < 1/100); редко(≥ 1/10 000 - < 1/1 000); очень редко(< 1/10 000), частота неизвестна(нельзя рассчитать по имеющимся данным).
В каждой из групп побочные явления представленные в порядке уменьшения степени их серьезности.
|
Класс органов и систем MedDRA |
Очень часто |
Часто |
Нечасто |
Редко |
|
Метаболические и алиментарные расстройства |
Гипогликемия |
|||
|
Расстройства со стороны кожи и подкожных тканей |
Реакции в месте инъекции местные реакции гиперчувствительности |
Липодистрофия |
||
|
Нарушение общего положения и реакции в месте введения |
Системные реакции гиперчувствительности |
Метаболические и алиментарные расстройства.
Симптомы гипогликемии, как правило, возникают внезапно. Они включают холодный пот, холодную бледную кожу, утомляемость, нервозность или тремор, ощущение беспокойства, необычную утомляемость или слабость, смущение, нарушение концентрации внимания, сонливость, сильное чувство голода, нарушения зрения, головную боль, тошноту и сильное сердцебиение. Гипогликемия может достичь значительной степени и привести к потере сознания та/або судорог и повлечь временное или постоянное нарушение функции мозга или даже стать причиной летального следствия.
Расстройства со стороны кожи и подкожных тканей.
Местные реакции гиперчувствительности(покраснение, отек и зуд в месте инъекции) возможны во время лечения с применением инсулина. Такие реакции, как правило, являются преходящими и обычно исчезают в случае продолжения лечения.
Липодистрофия может возникать в месте инъекции как следствие несоблюдения порядка изменения места инъекции.
Нарушение общего положения и реакции в месте введения.
Cистемні реакции гиперчувствительности могут включать крапивницу, сжатие в груди, одышку, аллергический дерматит и зуд. Тяжелые случаи включают генерализуемую аллергическую реакцию вместе с анафилактической реакцией, которая может угрожать жизни.
Срок пригодности. 2 годы.
Срок пригодности после первого приложения - 4 недели.
Условия хранения
Хранить в недоступном для детей месте.
Хранить в холодильнике при температуре от +2 ºС до +8 ºС. Не замораживать. Хранить шприц-ручку во внешней картонной упаковке с целью защиты от действия света.
Не допускать контакта со стенками холодильника.
Условия хранения во время пользования.
После начала применения шприц-ручку(с насаженным колпачком) необходимо использовать в течение 4 недель. Хранить при температуре не выше +25 ºС во внешней картонной упаковке с целью защиты от действия света. Перед первым использованием шприц-ручку необходимо хранить при комнатной температуре в течение 1-2 часов.
Несовместимость
Епайдру® не следует смешивать с другими препаратами, отличными за составом от НПХ(нейтрального протамина Хагедорна) инсулина человека.
Упаковка. № 5: по 1 картриджу по 3 мл, вмонтированному в одноразовое устройство - шприц-ручку СолоСтар® (без игл для инъекций), по 5 шприцевые ручки в картонной коробке.
Категория отпуска. За рецептом.
Производитель. Санофі-Авентіс Дойчланд ГмбХ, Германия/ Sanofi - Aventis Deutschland GmbH, Germany.
Местонахождение производителя и его адрес места осуществления деятельности.
Індустріпарк Хьохст-Брюнінгштрассе 50 H500, H590, Н600, Н785, Н790, Франкфурт-на-Майні, Гессен, 65926, Германия / Industriepark Hоеchst - Brueningstrasse 50 H500, H590, Н600, H785, H790, Frankfurt am Main, Hessen, 65926, Germany.
Заявитель. ООО "Санофі-Авентіс Украина", Украина/ Sanofi - Aventis Ukraine LLC, Ukraine.
ИНСТРУКЦИЯ
для медицинского применения лекарственного средства
ЕПАЙДРА®
(APIDRA®)
Состав
действующее вещество: инсулин глюлизин;
1 мл раствора содержит инсулину глюлизину(продукту рекомбинантной ДНК-технологии с применением Escherichia coli) 100 единицы, что эквивалентно 3,49 мг;
1 флакон содержит 10 мл раствора для инъекций, что эквивалентно 1000 Од. инсулину глюлизину;
вспомогательные вещества: м-крезол, натрию хлорид, трометамин, полисорбат 20, кислота хлористоводородная концентрированная, натрию гидроксид, вода для инъекций.
Врачебная форма. Раствор для инъекций.
Основные физико-химические свойства: прозрачный бесцветный водный раствор.
Фармакотерапевтична группа. Противодиабетические средства. Инсулины и аналоги быстрого действия.
Код АТХ А10А В06.
Фармакологические свойства.
Фармакодинамика. Инсулин глюлизин является рекомбинантным аналогом инсулина человека, что за своей силой действия подобный инсулину человека. Инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека.
Основное действие инсулинов и их аналогов, включая инсулин глюлизин, направленная на регулирование метаболизма глюкозы. Инсулины снижают уровень содержимого глюкозы в крови путем стимуляции периферийной утилизации глюкозы, особенно в скелетных мышцах и жировой ткани, и притеснение синтеза глюкозы в печенке. Инсулин предотвращает липолиз в адипоцитах, протеолизу и усиливает синтез протеина.
Исследования при участии здоровых добровольцев и больных сахарным диабетом продемонстрировали, что при подкожном введении инсулин глюлизин действует быстрее и имеет меньшую длительность действия, чем обычный инсулин человека. Если инсулин глюлизин применяется в виде инъекции подкожно, снижение уровня глюкозы в крови начинается в течение 10-20 минут. При применении подкожно инсулина глюлизину и обычного инсулина человека в дозе 0,15 От/кг в разное время относительно 15-минутного стандартного приема еды было установлено, что при введении инсулина глюлизину при условии введения за 2 минуты до приема еды наблюдается постпрандиальний гликемичний контроль, подобный такому при введении обычного инсулина человека, который применялся за 30 минуты до приму еде. При сравнении гипогликемичних эффектов инсулина глюлизину и обычного инсулина человека при введенные за 2 минуты до приема еды инсулин глюлизин обеспечивал лучший постпрандиальний контроль, чем обычный инсулин человека. Применение инсулина глюлизину через 15 минуты после начала приема еды обеспечивает гликемичний контроль, подобный такому при применении обычного инсулина человека, который введен за 2 минуты до начала приема еды.
Ожирение.
Инсулин глюлизин сохраняет свои быстродействующие свойства в рпзи приложение пациентам с ожирением. Время до достижения 20 % общей AUC и показатель AUC(0-2 часы), который является показателями раннего действия инсулинов относительно снижения уровня глюкозы, равнялись соответственно 114 мин. и 427 мг/кг для инсулина глюлизину, 121 мин. и 354 мг/кг для инсулина лиспро, 150 мин. и 197 мг/кг для обычного инсулина человека.
Раса и пол.
В ходе контролируемых клинических исследований при участии взрослых пациентов инсулин глюлизин не продемонстрировал разницу в безопасности и эффективности в подгруппах, которые отличались за расой и статью.
Фармакокинетика.
Более быстрая абсорбция инсулина глюлизину обеспечивается заменой аминокислоты аспарагина в позиции В3 инсулина человека лизином и лизину в позиции В29 глютаминовой кислотой.
Абсорбция и биодоступность.
Фармакокінетичні профили у здоровых добровольцев и больных сахарным диабетом (И или
ІІ типа) продемонстрировали, что уровень абсорбции инсулина глюлизину был в два раза более высокий, а максимальная концентрация, приблизительно в два раза более высокая сравнительно с таким у обычного инсулина человека.
У больных сахарным диабетом И типа после подкожной инъекции в дозе 0,15 От/кг показатели Тмакс для инсулина глюлизину равнялись 55 мин. и Смакс был 82 ± 1,3 µОт/мл сравнительно с Тмакс, 82 мин. и Смакс 46 ± 1,3 µОт/мл для обычного инсулина человека. Среднее время наличия в организме инсулина глюлизину было короче(98 мин.), чем обычного инсулина человека(161 мин.).
У больных сахарным диабетом ІІ типа после подкожного применения инсулина глюлизину в дозе 0,2 От/кг Смакс представляет 91µОт/мл с интервалом достоверности от 78 до 104 µОт/мл.
При подкожной инъекции инсулина глюлизину в брюшную стенку, бедро или дельтообразную мышцу абсорбция препарата является более скорой при применении в участок стенки живота, чем в бедро. Абсорбция в месте инъекции в участке дельтообразной мышцы была средней между вышеупомянутыми показателями. Абсолютная биодоступность(70 %) инсулина глюлизину была подобной в вышеупомянутых местах инъекций и имела низкую индивидуальную вариативнисть(11 % CV). Внутривенное болюсне применение инсулина глюлизину было причиной большего системного влияния сравнительно с такими при подкожной инъекции, причем значение Сmax было приблизительно в 40 разы больше.
Распределение и выведение.
Распределение и выведение инсулина глюлизину и обычного человеческого инсулина после внутривенного введения является подобным, при этом объемы распределения представляют 13 л и 22 л, а периоды полувыведения - 13 хв и 18 хв соответственно.
После подкожного приложения инсулин глюлизин выводится быстрее, чем обычный инсулин человека, со средней длительностью периодов полувыведения 42 хв для инсулина глюлизину сравнительно с 86 хв для обычного инсулина. При анализе перекрестного исследования инсулина глюлизину при участии здоровых добровольцев или больных сахарным диабетом
И или ІІ типа средняя длительность периода полувыведения была от 37 до 75 минут(интервал достоверности).
Инсулин глюлизин, как и человеческий инсулин, плохо связывается с белками плазмы крови.
Особенности применения препарата специфическим группам пациентов
· Пациенты с нарушениями функции почек.
При нарушении функции почек потребность в инсулине может снижаться, однако способность инсулина глюлизину быстро действовать хранится.
· Пациенты с нарушениями функции печенки.
Фармакокінетичні свойства инсулина глюлизину не исследовались у пациентов с нарушением функции печенки.
· Пациенты пожилого возраста.
Относительно пациентов пожилого возраста, больных сахарным диабетом, существует очень ограниченная база данных относительно фармакокинетики препарата.
· Дети и подростки.
Фармакокінетичні и фармакодинамични свойства инсулина глюлизину у детей(7-11 годы) и подростков(12-16 годы), больных сахарным диабетом И типа, такие: инсулин глюлизин быстро усваивается у больных обеих возрастных групп и имеет такие же показатели Тмакс и Смакс, как и у взрослых. Введение инсулина глюлизину непосредственно перед приемом еды детям и подросткам обеспечивает лучший постпрандиальний гликемичний контроль сравнительно с обычным инсулином человека, как и у взрослых больных. Отклонение уровня глюкозы(AUC) представляет 641 мг/год/дл для инсулина глюлизину и 801 мг/год/дл для обычного инсулина человека.
Доклинические данные относительно безопасности применения
Доклинические данные не указывают на наличие токсичности(кроме той, которая связана с гипогликемией), которая бы отличалась от показателей обычного инсулина человека или была клинически значимой для людей.
Клинические характеристики
Показание.
Сахарный диабет, когда необходимое применение инсулина взрослым, подросткам и детям в возрасте от 6 лет и старше.
Противопоказание.
Гиперчувствительность к инсулину глюлизину или любого компонента препарата. Гипогликемия.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий.
Исследования относительно типов фармакокинетичних взаимодействий не проводились. Учитывая эмпирические знания относительно других подобных лекарственных средств, проявление клинически релевантных фармакокинетичних взаимодействий является маловероятным.
На метаболизм глюкозы влияет целый ряд веществ и лекарственных препаратов. Следовательно, это может нуждаться регулирования дозы инсулина глюлизину и особенно тщательного надзора за больным.
К веществам, которые могут усилить глюкозознижувальну активность и увеличить восприимчивость к гипогликемии, принадлежат пероральные антидиабетические средства, ингибиторы ангиотензинперетворювалего фермента, дизопирамид, фибрати, флуоксетин, ингибиторы моноаминоксидази, пентоксифиллин, пропоксифен, салицилаты и сульфаниламидные антибиотики.
Вещества, которые могут привести к росту уровня глюкозы в крови, : кортикостероиды, даназол, диазоксид, диуретики, глюкагон, изониазид, производные фенотиазину, соматропин, симпатомиметические агенты(такие как, эпинефрин [адреналин], сальбутамол, тербуталин), тиреоидные гормоны, естрогени, прогестини(например, в составе пероральных контрацептивов), ингибиторы протеинази и антипсихотические лекарственные средства(в частности, оланзапин и клозапин) атипизма.
Блокаторы Беты, клонидин, соли лития или алкоголь могут привести как к повышению, так и к снижению свойства инсулина уменьшать уровень глюкозы в крови. Пентамідин может вызывать развитие гипогликемии, которая иногда сопровождается гипергликемией.
Кроме того, под воздействием симпатолитичних лекарственных средств, таких как клонидин, гуанетидин, резерпин, и блокаторов беты признака адренергического обратного регулирования могут быть ослаблены или даже отсутствуют.
Особенности применения
Переход пациента на применение нового типа или другой торговой марки препарата инсулина должно происходить под тщательным надзором врача. Изменения силы действия, торговой марки(производителя), типа препарата(обычный, НПХ [нейтральный протамин Хагедорна], ленте, длительного действия и тому подобное), происхождения(животный, человеческий, аналог человеческого инсулина) та/або метода производства могут обусловливать возникновение потребности в изменении дозы. Также может возникать необходимость во внесении изменений к схеме сопутствующего применения пероральных противодиабетических препаратов.
Гипергликемия
Применение несоответственно доз или прекращение лечения, особенно у больных инсулинозависимым диабетом, может привести к развитию гипергликемии и диабетического кетоацидоза - состояниям, которые являются потенциально летальными.
Гипогликемия
Время развития гипогликемии зависит от профиля действия используемых инсулинов и, таким образом, может изменяться после изменения схемы лечения.
Условия, которые могут сделать ранние предупредительные симптомы гипогликемии нетипичными или менее выраженными, включают значительную длительность заболевания на диабет, интенсивную инсулинотерапию, диабетическую нейропатию, применение лекарственных препаратов, таких как блокаторы беты, или переход из инсулина животного происхождения на инсулин человека.
Потребность в коррекции дозы также может возникнуть, если пациенты увеличивают свою физическую активность или изменяют свой обычный рацион питания. Физические нагрузки сразу после приема еды могут повышать риск развития гипогликемии.
Гипогликемия после введения быстродействующих аналогов инсулина может возникать раньше, чем при применении растворимого инсулина человека.
Если не предоставить пациенту соответствующей помощи, гипогликемические или гипергликемични реакции могут привести к потере сознания, запятой или летального следствия.
Потребность в инсулине может изменяться при наличии другой болезни или эмоциональных нарушений.
Ошибочное введение другого препарата
Приходили сообщения об ошибочном введении препаратов, когда вместо инсулина глюлизину случайно вводились другие инсулины, в частности инсулины длительного действия. Перед каждой инъекцией следует проверять информацию на этикетке препарата, во избежание ошибочного введения вместо инсулина глюлизину других инсулинов.
Непрерывная подкожная инфузия инсулина
Неисправность инсулинового насоса или системы для инфузионного введения или неправильное обращение с ними может приводить к быстрому развитию гипергликемии, кетоза или диабетического кетоацидоза. В таких случаях необходимо быстрое определение и устранение причины гипергликемии, кетоза или диабетического кетоацидоза.
Сообщалось о случаях развития диабетического кетоацидоза при введении препарата Епайдра® путем непрерывной подкожной инфузии инсулина с помощью насосных систем. Большинство из этих случаев было связано с неправильным обращением с насосными системами или с их неисправностями.
Может быть нужно временное введение препарата Епайдра® путем подкожных инъекций. Пациентов, которые получают инсулинотерапию путем непрерывной подкожной инфузии инсулина с помощью насосных систем, необходимо научить вводить инсулин с помощью инъекций. Такие пациенты должны иметь наготове другое средство введения инсулина на случай неисправности насосной системы(см. разделы "Особенности применения " и "Побочные реакции").
Вспомогательные вещества
Одна доза этого лекарственного средства содержит меньше чем 1 ммоль(23 мг) натрию, то есть он практически не содержит натрия.
Епайдра® содержит м-крезол, который может повлечь аллергические реакции.
Комбинация препарата Епайдра из пиоглитазоном
Сообщалось о случаях сердечной недостаточности при применении пиоглитазону в сочетании из инсулином, особенно у пациентов, которые имеют факторы риска развития сердечной недостаточности. Это нужно учитывать при рассмотрении возможности проведения лечения комбинацией пиоглитазону и препарату Епайдра®. При применении этой комбинации за пациентами нужно наблюдать относительно появления признаков и симптомов сердечной недостаточности, увеличения массы тела и появления отеков.
При любом ухудшении кардиологических симптомов применения пиоглитазону нужно прекратить.
Применение в период беременности или кормления груддю.
Беременность
Даны относительно применения инсулина глюлизину беременным женщинам отсутствуют или ограничены(меньше чем 300 результаты беременности).
В ходе исследований влияния на репродуктивную функцию, проведенных на животных, не было выявлено никаких отличий между применением инсулина глюлизину и инсулина человека относительно влияния на беременность, развитие эмбриона/плода, роды или постнатальное развитие(см. раздел "Фармакологические свойства").
Беременным женщинам этот препарат следует применять с осторожностью. Необходимо тщательным образом контролировать уровень глюкозы.
Пациентам с диагностированным или гестационным сахарным диабетом в период беременности следует поддерживать надлежащий метаболический контроль. Потребность организма в инсулине может уменьшаться в первом триместре беременности и, как правило, увеличивается в период второго и третьего триместров. Сразу после родов потребность организма в инсулине быстро уменьшается.
Кормление груддю
Неизвестно, или екскретуеться инсулин глюлизин в грудное молоко человека, однако обычно инсулин не проникает в грудное молоко и не абсорбируется после перорального приема.
Женщинам, которые кормят груддю, может быть необходимо откорректировать дозу инсулина и рацион питания.
Фертильность
В ходе исследований влияния інсулінy глюлізинy на репродуктивную функцию, проведенных на животных, не было выявлено никаких нежелательных влияний на фертильность.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Способность пациента концентрировать внимание и его реакция могут нарушаться вследствие развития гипогликемии или гипергликемии или, например, в результате нарушения зрения. Это может представлять риск в ситуациях, когда наличие таких симптомов является особенно важным(в частности, во время управления автомобилем или механизмами).
Пациентам следует рекомендовать быть осторожными и предотвращать развитие гипогликемии во время управления транспортом. Это особенно важно для тех, кто недостаточно поинформирован или вовсе не поинформирован относительно симптомов-предсказателей гипогликемии, и для тех больных, у кого часто возникают эпизоды гипогликемий. При этих обстоятельствах следует рассмотреть целесообразность управления транспортом.
Способ применения и дозы
Сила действия этого препарата выражается в единицах. Эти единицы используются исключительно для препарата Епайдра® и отличаются от МО или единиц, в которых выражается сила действия других аналогов инсулина.
Препарат Епайдра® можно применять в режимах инсулинотерапии, которые включают инсулин среднего или долговременного действия, или аналог базального инсулина, и можно применять одновременно с пероральными противодиабетическими средствами.
Дозу препарата Епайдра® подбирают и регулируют индивидуально.
Особенные категории пациентов
Пациенты с нарушениями функции почек
Фармакокінетичні свойства инсулина глюлизину в целом хранятся у пациентов с нарушением функции почек. Однако в случае нарушения функции почек потребность в инсулине может снижаться(см. раздел "Фармакокинетика").
Пациенты с нарушениями функции печенки
Фармакокінетичні свойства инсулина глюлизину не изучались у пациентов со сниженной функцией печенки. У пациентов с нарушением функции печенки потребность в инсулине может быть меньшей через снижение глюконеогенеза и способности инсулина метаболизуватися.
Пациенты пожилого возраста
Имеются даны из фармакокинетики инсулина у пациентов пожилого возраста, больных сахарным диабетом, является недостаточными. Ухудшение функции почек может привести к уменьшению потребности в инсулине.
Дети и подростки
Не существует достоверной клинической информации относительно применения препарата Епайдра® у детей в возрасте до 6 лет.
Применение.
Препарат Епайдра® следует вводить путем подкожной инъекции незадолго до или сразу после приема еды или путем постоянной подкожной инфузии с помощью инсулинового насоса.
Препарат Епайдра® нужно вводить подкожно в участок передней стенки живота, бедра или дельтообразной мышцы или путем непрерывной инфузии под кожу передней стенки живота. Места для инъекций или инфузий в зоне инъекции(передняя стенка живота, бедро или дельтообразная мышца) следует по очереди изменять. Степень абсорбции и, вероятно, начало и срок действия могут зависеть от определенного места инъекции, техники ее исполнения и других переменных показателей. Подкожная инъекция в переднюю стенку живота обеспечивает несколько более быструю абсорбцию, чем введение препарата в другие места для инъекций.
Следует соблюдать осторожность, чтобы исключить введение препарата непосредственно в кровеносный сосуд. После введения препарата не следует массажировать место инъекции.
Пациентов следует учить придерживаться правильной процедуры выполнения инъекций.
Смешивание с другими инсулинами
Препарат Епайдра®, который вводится в виде подкожной инъекции, запрещается смешивать с любыми другими лекарственными средствами, кроме человеческого инсулина НПХ(нейтрального протамина Хагедорна). При смешивании из НПХ(нейтральным протамином Хагердона) инсулином человека сначала следует набрать в шприц препарат Епайдра®. Инъекцию нужно делать сразу же после смешивания, поскольку надлежащих данных относительно стабильности смесей, приготовленных задолго до введения, нет.
Непрерывная подкожная инфузия инсулина
Препарат Епайдра® можно применять для непрерывной подкожной инфузии инсулина(CSII) через насосные системы, предназначенные для проведения инфузии инсулина и укомплектованы соответствующими катетерами и резервуарами. Пациентов, которые пользуются CSII, нужно тщательным образом проинструктировать относительно применения насосных систем.
Систему инфузионного введения и резервуар, которые используются для введения препарата Епайдра®, нужно менять по крайней мере каждые 48 часы с соблюдением правил асептики. Эти инструкции могут отличаться от общих инструкций из использования насосных систем. Важно, чтобы при применении препарата Епайдра® пациенты придерживались специфических инструкций относительно этого препарата. Несоблюдение специфических инструкций относительно препарата Епайдра® может привести к серьезным нежелательным явлениям.
При подкожном введении с помощью инсулинового инфузионного насоса препарат Епайдра® запрещается смешивать с растворителями или любым другим инсулином.
Пациенты, которые применяют препарат Епайдра® с помощью CSII, должны дополнительно мать другое средство введения инсулина на случай неисправности насосной системы(см. разделы "Особенности применения " и "Побочные реакции").
Деть. Данных относительно клинического применения препарата Епайдра® детям в возрасте до 6 лет недостаточно.
Передозировка
Гипогликемия может возникать как следствие чрезмерного действия инсулина относительно к объему принятой еды и расходов энергии.
Специфические данные относительно передозировки инсулина глюлизину отсутствуют. Однако гипогликемия может развиться постепенно.
Умеренные гипогликемические эпизоды могут лечиться путем перорального применения глюкозы или сахара. Таким образом, больному сахарным диабетом рекомендуется постоянно мать при себе несколько кусочков сахара, конфет, печенья или фруктового сока с сахаром. Цукрозамінники нельзя использовать для лечения гипогликемических состояний.
Тяжелые гипогликемические эпизоды, при которых пациент теряет сознание, можно устранять путем введения глюкагону(0,5-1 мг) внутримышечно или подкожно, что может сделать соответствующим образом проинструктированное лицо, или путем внутривенного введения глюкозы, которая должна выполнить медицинский работник. Глюкоза вводится внутривенно также в случае, если состояние пациента не улучшается в течение 10 или 15 минуты после введения глюкагону.
Когда больной очнется, рекомендуется применить углеводы перорально с целью предотвращения рецидива гипогликемии.
После инъекции глюкагону пациента следует обследовать в больнице для выявления причины возникновения тяжелой гипогликемии и предотвращения возникновения подобных нападений.
Побочные реакции
Самым распространенным косвенным действием инсулинотерапии является гипогликемия, которая возникает как следствие применения значительно больше дозы инсулина, чем это нужно.
Соответствующие побочные реакции, продемонстрированные во время проведения клинических исследований, приводятся ниже за классами систем органов и в порядке уменьшения частоты возникновения : очень часто(≥ 1/10); часто(≥ 1/100 - < 1/10); нечасто(≥ 1/1 000 - < 1/100); редко(≥ 1/10 000 - < 1/1 000); очень редко(< 1/10 000), частота неизвестна(нельзя рассчитать по имеющимся данным).
В каждой из групп побочные явления представленные в порядке уменьшения степени их серьезности.
|
Классы систем органов за MedDRA |
Очень часто |
Часто |
Нечасто |
Редко |
Частота неизвестна |
|
Метаболические и алиментарные расстройства |
Гипогликемия |
Гипергликемия(что потенциально может приводить к диабетическому кетоацидозу(1)) |
|||
|
Расстройства со стороны кожи и подкожной клетчатки |
Реакции в месте инъекции. |
Ліпо-дистрофія |
|||
|
Общие расстройства и реакции в месте применения |
Системные реакции гиперчутли-вости |
( 1) Большинство из этих случаев была связана с неправильным обращением с насосной системой или ее неисправностями при применении препарата Епайдра® с помощью CSII.
Описание отдельных нежелательных реакций
Метаболические и алиментарные расстройства.
Симптомы гипогликемии, как правило, возникают внезапно. Они включают холодный пот, холодную бледную кожу, утомляемость, нервозность или тремор, ощущение беспокойства, необычную утомляемость или слабость, смущение, нарушение концентрации внимания, сонливость, сильное чувство голода, нарушения зрения, головную боль, тошноту и сильное сердцебиение. Гипогликемия может достичь значительной степени и привести к потере сознания та/або судорог и повлечь временное или постоянное нарушение функции мозга или даже стать причиной летального следствия.
Сообщалось о случаях развития гипергликемии при применении препарата Епайдра® с помощью CSII(см. раздел "Особенности применения"), которые приводили к возникновению диабетического кетоацидоза(ДКА); большинство из этих случаев было связано с неправильным обращением с насосной системой или ее неисправностями. Пациент должен всегда придерживаться специфических инструкций из введения препарата Епайдра® и обязательно мать наготове другое средство введения инсулина на случай неисправности насосной системы.
Расстройства со стороны кожи и подкожных тканей.
Местные реакции гиперчувствительности(покраснение, отек и зуд в месте инъекции) возможны во время лечения с применением инсулина. Такие реакции, как правило, являются преходящими и обычно исчезают в случае продолжения лечения.
Липодистрофия может возникать в месте инъекции как следствие несоблюдения порядка изменения места инъекции.
Нарушение общего положения и реакции в месте введения.
Cистемні реакции гиперчувствительности могут включать крапивницу, сжатие в груди, одышку, аллергический дерматит и зуд. Тяжелые случаи включают генерализуемую аллергическую реакцию вместе с анафилактической реакцией, которая может угрожать жизни.
Срок пригодности. 2 годы.
Срок пригодности после первого использования - 4 недели.
Условия хранения.
Хранить в недоступном для детей месте. Хранить в холодильнике при температуре от +2ºС до +8ºС. Не замораживать. Хранить флакон во внешней картонной коробке с целью защиты от действия света. Предотвращать контакт со стенками холодильника.
Условия хранения после открытия флакона.
Открытые флаконы необходимо использовать в течение 4 недель. Хранить при температуре не выше +25 ºС во внешней картонной коробке с целью защиты от действия света.
Несовместимость
Подкожное введение.
Препарат Епайдра® не следует смешивать с другими препаратами, отличными за составом от НПХ(нейтрального протамина Хагедорна) инсулина человека.
При подкожном введении с помощью инсулинового инфузионного насосу препарат Епайдра® запрещается смешивать с другими лекарственными средствами.
Упаковка. № 1: по 10 мл в флаконе; по 1 флакону в картонной коробке.
Категория отпуска. За рецептом.
Производитель. Санофі-Авентіс Дойчланд ГмбХ, Германия/ Sanofi - Aventis Deutschland GmbH, Germany.
Местонахождение производителя и его адрес места осуществления деятельности.
Індустріпарк Хьохст-Брюнінгштрассе 50 H500, H590, Н600, Н785, Н790, Франкфурт-на-Майні, Гессен, 65926, Германия / Industriepark Hоеchst - Brueningstrasse 50 H500, H590, Н600, H785, H790, Frankfurt am Main, Hessen, 65926, Germany.
Заявитель. ООО "Санофі-Авентіс Украина", Украина/ Sanofi - Aventis Ukraine LLC, Ukraine.
Другие медикаменты этого же производителя
Форма: раствор для перорального приложения, 100 мг/мл № 1(по 60 мл в флаконе, по 1 флакону в картонной коробке); в картонную коробку вложенный шприц для дозирования
Форма: таблетки, покрытые оболочкой, по 3 000 000 МО № 10(10х1) : по 10 таблетки в блистере, по 1 блистеру в картонной коробке
Форма: концентрат для раствора для инфузий по 12 мг/1,2 мл № 1: по 1,2 мл в флаконе, по 1 флакону в картонной коробке
Форма: таблетки, покрытые пленочной оболочкой, по 10 мг № 30(15х2), № 90(15х6) : по 15 таблетки в блистере, по 2 или 6 блистеры в картонной коробке
Форма: капсулы по 300 мг № 56(7х8) в блистерах