Генотропин®
Регистрационный номер: UA/11798/01/02
- Состав
- Клинические характеристики
- Показание
- Противопоказание
- Особенности применения
- Способ применения и дозы
- Кончик держателя картриджа
- Черная кнопка фиксатора
- Налаживание и применение новой ручки
- Шаг 1 Прикрепление иглы(рис 1)
- Шаг 2 Смешивание препарата(рис 2)
- Паз
- Шаг 3 Удаление воздуха
- Шаг 5 Подготовка ручки к работе
- Внутренний футляр иглы Выбросить
- Внешний футляр иглы Сохранить
- Серый диск
- Предохранитель
- иглы
- Предохранитель иглы
- Вытянуть
- Шаг 6 Установление дозы
- Шаг 7 Набор дозы
- Запобіж-
- поникал иглы
- кнопка
- Белый указатель
- Шаг 9a С предохранителем иглы
- Шаг 9b Без предохранителя иглы
- Внешний футляр иглы
- 5 секунды
- Без предохранителя иглы
- Экран иглы
- С предохранителем иглы
- Кончик держателя
- картриджа
- 8 Сделайте инъекцию
- 9 Удалите иглу
- Хранение
- Поведение
- Иглы
- Общие положения
- Вопрос
- Ответ
- Передозировка
- Побочные реакции
Импортёр: Пфайзер Інк.
Страна: СШААдреса импортёра: 235 Ист 42-га Стрит, Нью-Йорк, НЙ 10017-5755, США
Форма
порошок лиофилизированный и растворитель для раствора для инъекций по 36 МО(12 мг); 1 или 5 предварительно наполненных ручек, которые содержат 1 двухкамерный картридж(передняя камера с порошком и задняя камера с растворителем по 1,13 мл(м-крезол, маннит(E 421), вода для инъекций)) каждая, в картонной коробке; 1 или 5 предварительно наполненных ручек, которые содержат 1 двухкамерный картридж(передняя камера с порошком и задняя камера с растворителем по 1,13 мл(м-крезол, маннит(E 421), вода для инъекций)) каждая, в картонной коробке из стикером
Состав
передняя камера: соматропин 13,8 мг; 1 мл возобновленного раствора содержит соматропину 36 МО(12 мг)
Виробники препарату «Генотропин®»
Страна производителя: Бельгия
Адрес производителя: Рейксвег 12, Пуурс, В- 2870, Бельгия
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
ГЕНОТРОПІН®
(GENOTROPIN®)
Состав
действующее вещество: соматропин;
передняя камера: соматропин 6,1 мг или 13,8 мг;
1 мл возобновленного раствора содержит соматропину 16 МО(5,3 мг) или 36 МО(12 мг);
вспомогательные вещества: глицин, маннит(E 421), натрию дигидрофосфат безводный, натрию гидрофосфат(додекагидрат);
задняя камера(растворитель) : м-крезол, маннит(E 421), вода для инъекций.
Врачебная форма. Порошок лиофилизированный и растворитель для раствора для инъекций.
Основные физико-химические свойства: лиофилизированное гомогенное вещество белого цвета. Растворитель должен быть практически свободным от механических включений.
Фармакотерапевтична группа. Гормоны передней части гипофиза и их аналоги. Соматропін и агонисты соматропину. Соматропін. Код АТХ H01A C01.
Фармакологические свойства.
Фармакодинамика.
Соматропін - сильный метаболический гормон, который играет важную роль в метаболизме липидов, углеводов и белков. У детей с недостаточностью эндогенного гормона роста соматропин убыстряет линейный рост скелета и скорость роста. Как у взрослых, так и у детей соматропин поддерживает нормальное телосложение благодаря повышению усвоения нитрогена, ускорению роста скелетных мышц и мобилизации жира в организме. К соматропину особенно чувствительная висцеральна жировая ткань. Кроме стимуляции липолиза, соматропин уменьшает поступление триглицеридов в жировые депо. Концентрации ІФР- 1(инсулиноподобного фактора роста, тип 1) и ІФРЗБ- 3(связывающего белка инсулиноподобного фактора роста, тип 3) в сыворотке крови повышаются под воздействием соматропину.
Метаболизм липидов. Соматропін стимулирует рецепторы холестерина липопротеина низкой плотности(ЛПНЩ) в печенке и влияет на профиль липидов и липопротеина в сыворотке крови. В целом применение соматропину у пациентов с дефицитом гормона роста приводит к снижению концентрации ЛПНЩ и аполипопротеину B. Также возможное снижение уровня общего холестерина.
Метаболизм углеводов. Соматропін повышает уровень инсулина, однако уровень глюкозы натощак обычно не изменяется. У детей с гипопитуитаризмом может отмечаться гипогликемия натощак. Соматропін инвертирует это состояние.
Водно-солевой обмен. Дефицит гормона роста связан со снижением объемов плазмы крови и тканевой жидкости. Оба этих показателя быстро растут после лечения соматропином. Соматропін способствует задержке в организме натрия, калия и фосфора.
Костный метаболизм. Соматропін стимулирует обновление костной ткани скелета. У пациентов с дефицитом гормона роста и остеопорозом длительное лечение соматропином приводит к повышению минерального состава и плотности костей на опорных участках.
Физическая работоспособность. Длительное лечение соматропином повышает силу мышц и физическую выносливость. Соматропін также увеличивает сердечные выбросы, однако механизм этого эффекта еще не выяснен. Определенную роль в этом может играть уменьшение периферического сосудистого сопротивления.
В ходе клинических исследований с участием детей низкого роста, которые родились малыми для своего гестационного возраста, применяли дозы от 0,033 до 0,067 мг/кг массы тела на сутки до достижения окончательного роста. В 56 пациентов, которых постоянно лечили и которые достигли(почти достигли) окончательного роста, величина стандартного отклонения(ВСВ) для среднего изменения роста от начала лечения представляла +1,90 ВСВ для дозы 0,033 мг/кг на сутки и +2,19 ВСВ для дозы 0,067 мг/кг на сутки. Опубликованные даны относительно детей, которые родились малыми для своего гестационного возраста и которые не получали лечения и не смогли спонтанно достичь нормального роста, допускают поздний рост в пределах 0,5 ВСВ.
Фармакокинетика.
Абсорбция. Биодоступность соматропину, введенного подкожно, представляет приблизительно 80 % как у здоровых добровольцев, так и у пациентов с дефицитом гормона роста. Доза 0,035 мг/кг соматропину, введенного подкожно, приводит к таким диапазонам значений Cmax и tmax в плазме крови : 13-35 нг/мл и 3-6 часы соответственно.
Выведение. Среднее время полувыведения после внутривенного применения соматропину взрослым с дефицитом гормона роста представляет приблизительно 0,4 часы. Однако после подкожного приложения время полувыведения может представлять до 2-3 часов. Разница, которая наблюдалась, возможно, вызванная медленной абсорбцией с места инъекции после подкожного приложения.
Субпопуляции. Абсолютная биодоступность соматропину при подкожном введении является одинаковой у лиц мужского и женского пола.
Информация относительно фармакокинетики соматропину у пациентов пожилого возраста, у детей, у пациентов разных рас и у пациентов с нарушением функций почек и печенки или сердечной недостаточностью отсутствующая или неполная.
Доклинические данные из безопасности.
В ходе исследований общей токсичности, местной переносимости и репродуктивной токсичности ни одного клинически релевантного действия не наблюдалось. In vitro и in vivo исследования генотоксичности относительно генных мутаций и индукции хромосомных абераций имели негативный результат.
В ходе одного исследования in vitro на лимфоцитах, взятых у пациентов после длительного лечения соматропином и дальнейшего применения дополнительного радиомиметического препарата блеомицину, наблюдалась повышенная ломкость хромосом. Клиническое значение этого факта не понятно.
В ходе другого исследования в лимфоцитах, взятых у пациентов после длительного лечения соматропином, не было выявлено хромосомных аномалий.
Клинические характеристики
Показание
Деть.
Нарушение роста через недостаточную секрецию гормона роста(дефицит гормона роста).
Нарушение роста, связанное с синдромом Тернера или хронической почечной недостаточностью.
Нарушение роста(величина стандартного отклонения текущего роста меньше - 2,5 и величина стандартного отклонения генетически предопределенного роста меньше - 1) у детей низкого роста, которые родились меньше нормы для своего гестационного возраста, со стандартным отклонением в массе та/або длине тела меньше - 2 и не смогли достичь вековой нормы роста(величина стандартного отклонения скорости роста менее 0 в течение последнего года) к достижению ими 4 годов и больше.
Синдром Прадера-Віллі с целью улучшения роста и телосложения. Диагноз синдрома Прадера-Віллі следует подтвердить соответствующими генетическими тестами.
Взрослые.
Заместительная терапия для взрослых с выраженным дефицитом гормона роста.
Возникновение дефицита гормона роста во взрослом возрасте. Пациенты с дефицитом гормона роста тяжелой степени, связанным с множественным гормональным дефицитом в результате известной патологии гипоталамуса или гипофиза, а также пациенты, которые имеют дефицит хотя бы одного из гормонов гипофиза, за исключением пролактину. Этим пациентам следует провести соответствующий динамический тест для установления наличия или отсутствия дефицита гормона роста.
Возникновение дефицита гормона роста в детском возрасте. Пациенты, в которых возник дефицит гормона роста в детском возрасте в результате наследственных, генетических, приобретенных или неизвестных причин. Для пациентов с дефицитом гормона роста, который возник в детском возрасте, следует провести повторный тест на способность секреции гормона после окончания продольного роста. Для пациентов с высокой вероятностью постоянного дефицита гормона роста(например, по наследственным причинам или вторичному дефициту гормона роста в результате гипоталамо-гипофизарного заболевания или инсульта) величина среднего отклонения инсулиноподобного фактора роста, тип 1(ІФР- 1) меньше - 2 без лечения гормоном роста в течение по крайней мере 4 недель должен считаться достаточным основанием для диагностики дефицита гормона роста.
Для всех других пациентов необходимо провести анализ ІФР- 1 и один тест стимуляции гормона роста.
Противопоказание
Повышенная чувствительность к действующему веществу или к любому вспомогательному веществу.
Соматропін запрещено назначать при наличии любых признаков активности опухоли. Внутричерепные опухоли должны быть неактивные, а также перед началом терапии гормоном роста нужно закончить противоопухолевую терапию. При наличии любых признаков опухолевого роста лечения следует прекратить.
Генотропін® не следует применять для стимуляции росту детям с закрытыми эпифизарными зонами роста.
Лечение препаратом Генотропін® противопоказано пациентам, которые находятся в остром критическом состоянии в результате осложнения операции на открытом сердце, на брюшной полости, в результате множественной травмы, острой дыхательной недостаточности или других подобных состояний(информацию относительно пациентов, которые получают заместительное лечение, см. в разделе "Особенности применения").
Соматропін противопоказанный больным активной пролиферативной или тяжелой непролиферативной диабетической ретинопатией.
Соматропін противопоказанный детям с синдромом Прадера-Віллі, которые страдают ожирением тяжелой степени или имеют тяжелые нарушения со стороны дыхательных путей.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Одновременное приложение с глюкокортикоидами подавляет стимулирующее влияние препаратов соматропину на скорость роста. Пациентам с дефицитом адренокортикотропного гормона следует внимательно подбирать заместительную терапию глюкокортикоидами, во избежание любого пригничувального влиянию на рост.
Поэтому необходимо тщательным образом контролировать рост пациентов, которые получают лечение глюкокортикоидами, чтобы иметь возможность оценить потенциальное влияние применения глюкокортикоидов на рост.
Гормон роста уменьшает превращение кортизону в кортизол и может привести к проявлению ранее не диагностированной центральной гипофункции надпочечников или сделать неэффективным применение низких доз глюкокортикоидов для заместительной терапии(см. раздел "Особенности применения").
Данные, полученные во время исследования взаимодействия лекарственных препаратов, проведенного с участием взрослых пациентов с дефицитом гормона роста, свидетельствуют о том, что применение соматропину может повышать клиренс соединений, какие метаболизуються с помощью изоферментов цитохрома Р450. Клиренс соединений, какие метаболизуються с помощью цитохрома Р450 3А4(таких как половые стероидные гормоны, кортикостероиды, противосудорожные препараты и циклоспорин), может быть слишком повышенным, приводя к уменьшению концентрации этих веществ в плазме крови. Клиническое значение этого факта неизвестно.
Дополнительную информацию относительно сахарного диабета и дисфункции щитовидной железы см. в разделе "Особенности применения".
Женщинам, которые получают заміcну терапию эстрогеном перорально, для достижения цели лечения может быть нужна высшая доза гормона роста(см. раздел "Особенности применения").
Особенности применения
Ставить диагноз, начинать терапию препаратом Генотропін® и проводить дальнейший контроль должны квалифицированные врачи, которые имеют опыт диагностики и лечения пациентов в соответствии с показаниями для применения.
Миозит - очень редкий побочный эффект, который может быть вызван действием консерванта м-крезола, который входит в состав препарата. В случае миалгии или повышенной болезненности в месте инъекции следует допускать возникновение миозита. В случае его подтверждения необходимо применять форму препарата соматропину, что не содержит м-крезола.
Не следует превышать максимальную рекомендованную суточную дозу(см. раздел "Способ применения и дозы").
Чувствительность к инсулину.
Соматропін может снижать чувствительность к инсулину. Для пациентов с сахарным диабетом после начала терапии соматропином может быть нужная коррекция дозы инсулина. В течение терапии соматропином следует контролировать состояние пациентов с диабетом, непереносимостью глюкозы или дополнительными факторами риска развития диабета.
Редко терапия соматропином может вызывать значительную непереносимость глюкозы, которая отвечает диагностическим критериям сахарного диабета 2-го типа.
Риск развития диабета во время лечения соматропином более высок у пациентов с другими факторами риска возникновения сахарного диабета 2-го типа, такими как ожирение, диабет в семейном анамнезе, лечение стероидами или предварительно ослабленная переносимость глюкозы. Пациентам с существующим сахарным диабетом может быть нужная корректировка противодиабетической терапии после назначения лечения соматропином.
Функция щитовидной железы.
Гормон роста убыстряет периферическое превращение Т4 в Т3, что может повлечь снижение сывороточной концентрации Т4 и рост сывороточной концентрации Т3. В то время как периферические концентрации гормонов щитовидной железы остаются в норме в большинстве здоровых добровольцев, теоретически возможное развитие гипотиреоза у пациентов с субклинической формой гипотиреоза. Следовательно, для всех пациентов следует проводить контроль функций щитовидной железы. У пациентов с гипопитуитаризмом, которые получают стандартную заместительную терапию, необходимо тщательным образом контролировать возможное влияние терапии гормоном роста на функцию щитовидной железы.
Гипофункция надпочечников.
Ввод лечения соматропином может привести к притеснению 11βHSD - 1 и снижение концентрации кортизола в сыворотке крови. У пациентов, которые получали соматропин, может проявиться раньше не диагностирована центральная(вторичная) гипофункция надпочечников, и им может быть нужна заместительная терапия глюкокортикоидами. Кроме того, пациенты, которые получали заместительную терапию глюкокортикоидами в виду предварительно диагностированной гипофункции надпочечников, могут нуждаться увеличения пидтримуючих или повышенных доз после начала лечения соматропином(см. раздел "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
Совместимое приложение с пероральной терапией эстрогеном.
Если женщина, которая применяет соматропин, начинает пероральную терапию эстрогеном, возможно, нужно будет увеличить ей дозу соматропину, чтобы поддерживать уровни ІФР- 1 в сыворотке крови в пределах вековой нормы. И наоборот, если женщина, которая применяет соматропин, прекращает пероральную терапию эстрогеном, возможно, нужно будет уменьшение дозы соматропину, во избежание излишка гормона роста та/або побочных эффектов(см. раздел "Взаимодействие с другими лекарственными средствами и другие виды взаимодействий").
В случае вторичного дефицита гормона роста в результате лечения злокачественных заболеваний, рекомендуется обращать внимание на признаки рецидива злокачественного новообразования. Относительно лиц с перенесенным злокачественным новообразованием в детстве сообщалось о повышенном риске развития вторичного новообразования у пациентов, которые получали лечение соматропином после первичного новообразования.
Самыми частыми такими вторичными новообразованиями у пациентов, которые получали лучевое лечение участка председателя по поводу первичного новообразования, были внутричерепные опухоли, в частности менингиомы.
У пациентов с эндокринными расстройствами, в частности с дефицитом гормона роста, могут возникать вывихи головки бедра чаще, чем в человеческой популяции в целом. Деть, которые хромают во время терапии соматропином, должны быть клинически обследованы.
Доброкачественная внутричерепная гипертензия.
В случае тяжелой или частой головной боли, нарушений зрения, тошноты та/або блюет рекомендуется провести офтальмоскопию относительно выявления отека диска зрительного нерва. Если наличие отека диска зрительного нерва подтверждается, следует рассмотреть диагноз доброкачественной внутричерепной гипертензии и при необходимости прекратить лечение гормоном роста. На данное время недостаточно сведения, на основании которых можно сформулировать рекомендации относительно продолжения терапии гормоном роста для пациентов после исчезновения внутричерепной гипертензии. После возобновления терапии гормоном роста нужно проводить тщательный контроль симптомов внутричерепной гипертензии.
Лейкемия.
Сообщалось о случаях лейкемии у небольшого количества пациентов с дефицитом гормона роста, некоторые из которых получали терапию соматропином. Однако отсутствующие доказательства повышения частоты развития лейкемии у пациентов, которые получают гормон роста и не имеют склонности к этому заболеванию.
Антитела.
Как и в случае со всеми препаратами соматропину, у небольшой части пациентов могут образовываться антитела к препарату Генотропін® (приблизительно у 1 % пациента). Эти антитела характеризуются слабой связывающей способностью и не влияют на скорость роста. У любого пациента с недостаточным ответом на лечение(какую невозможно объяснить другими причинами) следует провести тест на наличие антител к соматропину.
Пациенты пожилого возраста.
Опыт применения пациентам в возрасте от 80 лет ограничен. Пациенты пожилого возраста могут быть чувствительнее к действию препарата Генотропін®, а следовательно, более склонными к развитию побочных реакций.
Острые критические состояния.
Эффективность препарата Генотропін® во время выздоровления изучали в ходе двух плацебо-контролируемых исследований с участием 522 пациентов, которые находились в критическом состоянии в результате осложнения операции на открытом сердце, на брюшной полости, в результате множественной травмы или острой дыхательной недостаточности. Летальность среди пациентов, которые получали 5,3 или 8 мг препарата Генотропін® на сутки, была более высока, чем в группе плацебо : 42 % сравнительно с 19 %. Согласно данной информации пациентов этого типа не следует лечить препаратом Генотропін®. Поскольку отсутствующая информация относительно безопасности проведения заместительной терапии гормоном роста пациентам с острыми критическими состояниями, для данной ситуации следует взвесить пользу от продолжения лечения и связанные потенциальные риски.
Для всех пациентов, в которых возник другой или подобное острое критическое состояние, необходимо взвесить возможную пользу лечения препаратом Генотропін® и связанный потенциальный риск.
Синдром Прадера-Віллі.
Лечение пациентов с синдромом Прадера-Віллі следует всегда сочетать с низкокалорийной диетой.
Сообщалось о летальных последствиях, связанных с применением гормона роста детям с синдромом Прадера-Віллі, которые имели один или больше факторы риска : тяжелое ожирение(пациенты с соотношением массы тела к росту, которое превышает 200 %), наличие в анамнезе дыхательной недостаточности или апноэ во время сна или неидентифицированная респираторная инфекция. Пациенты с одним или несколькими приведенными факторами могут принадлежать к группе повышенного риска.
Перед началом лечения соматропином у пациентов с синдромом Прадера-Віллі необходимо выявить признаки обструкции верхних дыхательных путей, апноэ во время сна или респираторных инфекций.
Если во время оценки проходности верхних дыхательных путей получены данные о наличии патологии, ребенка нужно направить к отоларингологу на лечение и устранение респираторного расстройства к началу лечения гормоном роста.
Апноэ во время сна следует выявить к началу терапии гормоном роста с помощью стандартных методов полисомнографии или ночной оксиметрии и контролировать в случае возможности его развития.
Если в течение лечения соматропином у пациентов возникают симптомы обструкции верхних дыхательных путей(в частности появление и увеличение храпа), лечения следует прервать и провести новое обследование ЛОР-органів.
В случае возможности развития апноэ во время сна следует контролировать всех пациентов с синдромом Прадера-Віллі.
Пациентов следует проверять относительно признаков респираторных инфекций, которые необходимо диагностировать как можно раньше и активно лечить.
У всех пациентов с синдромом Прадера-Віллі следует также тщательным образом контролировать массу тела к началу и в течение лечения гормоном роста.
У пациентов с синдромом Прадера-Віллі часто возникает сколиоз. У некоторых детей в связи с быстрым ростом сколиоз может прогрессировать. Во время лечения следует контролировать признаки сколиоза.
Опыт длительного применения гормона роста для лечения взрослых и пациентов с синдромом Прадера-Віллі ограничен.
Деть, которые родились малыми для своего гестационного возраста.
Перед началом лечения детей, которые родились малыми для своего гестационного возраста, следует исключить возможность влияния других медицинских причин или средств лечения на нарушение роста.
Перед началом лечения детей, которые родились малыми для своего гестационного возраста, рекомендуется определить уровни инсулина и глюкозы в крови натощак и ежегодно повторять это исследование. Пациентам с высоким риском возникновения сахарного диабета(например, при наличии в семейном анамнезе диабета, ожирения, выраженной резистентности к инсулину, черному акантозу) следует провести пероральный тест переносимости глюкозы. Если диагностируется наличие диабета, то гормон роста не следует применять.
Перед началом лечения детей, которые родились малыми для своего гестационного возраста, рекомендуется измерять уровни ІФР- 1 и дважды на год повторять это исследование. Если после повторного измерения стандартное отклонение уровней ІФР- 1 превышает +2 ВСВ сравнительно с вековой нормой и половым дозреванием, то для решения вопроса о необходимости коррекции дозы следует учитывать соотношение ІФР- 1/ІФРЗБ- 3.
Опыт лечения непосредственно перед началом полового дозревания детей, которые родились малыми для своего гестационного возраста, ограниченный. Поэтому не рекомендуется начинать лечения непосредственно перед началом полового дозревания. Опыт лечения пациентов с синдромом Сільвера-Расселла ограничен.
Успехи, полученные в ходе лечения детей, которые родились малыми для своего гестационного возраста, гормоном роста, могут быть потерянными, если лечение прекратить к достижению ими окончательного роста.
Хроническая почечная недостаточность.
В случае хронической почечной недостаточности функция почек к началу лечения должна быть более низкая 50 % от нормы. Для подтверждения признаков нарушений роста следует отслеживать рост на протяжении года к началу терапии. Во время этого периода нужно начать консервативное лечение нарушений функций почек(что включает контроль ацидоза, гиперпаратироидизму и питание) и проводить его в течение терапии гормоном роста. Лечение следует прекратить в случае трансплантации почки.
На данное время отсутствующие даны относительно достижения окончательного роста пациентами с хроническими нарушениями функций почек, для лечения которых применяли препарат Генотропін®.
Новообразование.
Пациенты с существующими опухолями или дефицитом гормона роста, что возникли в результате внутричерепных поражений, должны регулярно обследоваться относительно прогресса или рецидива основного патологического процесса. По клиническим данным, у детей не выявлено ни одной связи между заместительной терапией соматропином и рецидивом опухолей центральной нервной системы(ЦНС) или возникновением новых екстракраниальних опухолей. Однако среди детей с раком, которые выжили, сообщалось об увеличенном риске возникновения второго новообразования у пациентов, которые получали соматропин после лечения первого новообразования. Внутричерепные опухоли, в частности менингиомы, являются самыми распространенными вторичными новообразованиями у пациентов, которые проходили курс лечения облучением председателя в течение первого новообразования.
Неизвестно, или есть связь между заместительной терапией соматропином и рецидивом опухолей ЦНС у взрослых пациентов.
Пациенты должны находиться под тщательным надзором относительно возникновения любой злокачественной трансформации кожных поражений.
Гипопитуитаризм.
Заместительную терапию следует тщательным образом контролировать у пациентов с гипопитуитаризмом во время лечения соматропином.
Вывих головки бедренной кости у детей.
Вывих головки бедренной кости чаще возникает у пациентов с эндокринными расстройствами(в том числе дефицит гормона роста и синдром Тернера) или у швидкозростаючих пациентов. Любой педиатрический пациент, который начал хромать или жаловаться на тазобедренную или коленную боль во время терапии соматропином, должен быть тщательным образом обследован.
Отит и кардиоваскулярные нарушения у пациентов с синдромом Тернера.
Состояние пациентов с синдромом Тернера следует тщательным образом оценить относительно возникновения среднего отита и других заболеваний уха, поскольку эти пациенты имеют повышенный риск развития таких заболеваний и расстройств слуха. Лечение соматропином может привести к увеличению риска возникновения среднего отита у пациентов с синдромом Тернера. Кроме того, у пациентов с синдромом Тернера нужно тщательным образом контролировать состояние сердечно-сосудистой системы, поскольку такие пациенты имеют повышенный риск возникновения сердечно-сосудистых заболеваний, таких как инсульт, аневризма/расслоения аорты, гипертония.
Системные и местные реакции.
Может возникнуть атрофия тканей при введении соматропину подкожно в одно и то же место в течение длительного времени.
Как и с любым белком, могут возникать местные или системные аллергические реакции. Пациенты или их родители должны быть проинформированы, что такие реакции возможны и что в случае возникновения аллергических реакций, необходимо быстрое медицинское вмешательство.
Панкреатит
Сообщалось об одиночных случаях возникновения панкреатита у детей и взрослых, которые получают лечение соматропином, с некоторыми доказательствами, которые подтверждают высший риск у детей сравнительно с взрослыми. Существуют данные, что девушки с синдромом Тернера склонны к большему риску, чем другие деть, которых лечили соматропином. Хотя и изредка, но следует рассматривать возможность возникновения панкреатита у любого пациента, который проходит лечение соматропином, особенно у детей с прогрессирующей стойкой сильной болью в животе.
Изменения лабораторных показателей
В сыворотке крови может увеличиться уровень неорганического фосфора, щелочной фосфатазы, паратиреоидного гормона(ПТГ) и инсулиноподобного фактора роста(IФР - I) во время терапии соматотропином.
Применение в период беременности или кормления груддю.
Клинические исследования относительно применения препарата Генотропін® в период беременности отсутствуют. Поэтому препараты, которые содержат соматропин, не рекомендуется назначать беременным и женщинам репродуктивного возраста, которые не используют средства для контрацепции.
Клинические исследования относительно применения препаратов соматропину женщинам, которые кормят груддю, не проводились. Неизвестно, или проникает соматропин в грудное молоко человека, но абсорбция интактного белка из желудочно-кишечного тракта младенца является чрезвычайно маловероятной. Поэтому препараты соматропину следует применять с осторожностью женщинам, которые кормят груддю.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Генотропін® не влияет на скорость реакции во время управления автотранспортом или на работу с другими механизмами.
Способ применения и дозы
Дозирование и режим применения следует подбирать индивидуально.
Инъекцию следует выполнять подкожно и изменять место введения для предотвращения липоатрофии.
Задержка роста через недостаточную секрецию гормона роста у детей. Обычно рекомендуется доза 0,025-0,035 мг/кг массы тела на сутки или 0,7-1,0 мг/м² площади поверхности тела на сутки. Существует опыт применения даже высших доз.
Если дефицит гормона роста возник в детском возрасте и хранится в подростковом возрасте, следует продолжить лечение к достижению полного соматического развития(то есть телосложения, массы костей). Как контроль использовали одну из терапевтических целей в течение переходного периода: достижения нормального пика массы костей, которая определяется как величина показателя Т>- 1(то есть стандартизирован к среднему пика массы костей взрослого, измеренного с помощью двоенергетичной рентгеновской абсорбциометрии, с учетом пола и этнической принадлежности пациента). Инструкции относительно дозирования для взрослых описаны ниже.
Синдром Прадера-Віллі, с целью улучшения роста и телосложения у детей. Обычно следует назначать по 0,035 мг/кг массы тела на сутки(1,0 мг/м2 площади поверхности тела на сутки). Не следует превышать суточную дозу 2,7 мг. Лечения не следует применять детям со скоростью роста менее 1 см на год и в возрасте, когда начинается закрытие эпифизарных зон роста.
Задержка роста через синдром Тернера. Рекомендованная доза представляет 0,045-0,050 мг/кг массы тела на сутки или 1,4 мг/м² площади поверхности тела на сутки.
Задержка роста у пациентов с хронической почечной недостаточностью. Рекомендованная доза представляет 0,045-0,050 мг/кг массы тела на сутки(1,4 мг/м² площади поверхности тела на сутки). Недостаточная скорость роста может требовать назначения высшей дозы. Коррекция дозы может быть нужна через 6 месяцы лечения.
Задержка роста у низких детей, которые родились малыми для своего гестационного возраста. Обычно рекомендуется доза 0,035 мг/кг массы тела на сутки(1 мг/м² площади поверхности тела на сутки) до достижения окончательного роста(см. раздел "Фармакологические свойства").
Лечение следует прекратить после первого года, если величина стандартного отклонения для скорости роста представляет менее +1. Лечение следует прекратить, если скорость роста менее 2 см на год и(при необходимости подтверждения) костный возраст представляет больше 14 лет для девочек или больше 16 лет для мальчиков, что отвечает возраста закрытия ростковых зон в эпифизах костей.
Таблица 1.
Рекомендации относительно дозирования детям
|
Показание |
мг/кг массы тела |
мг/м2 площади поверхности тела |
|
суточная доза |
||
|
Дефицит гормона роста |
0,025-0,035 |
0,7 - 1,0 |
|
Синдром Прадера-Віллі |
0,035 |
1,0 |
|
Синдром Тернера |
0,045-0,050 |
1,4 |
|
Хроническая почечная недостаточность |
0,045-0,050 |
1,4 |
|
Задержка роста у детей, которые родились малыми для своего гестационного возраста |
0,035 |
1,0 |
Взрослые пациенты с дефицитом гормона роста. Для пациентов, которые продолжают терапию гормоном роста после возникновения дефицита гормона роста в детском возрасте, рекомендованная доза представляет 0,2-0,5 мг на сутки. Дозу нужно постепенно увеличивать или уменьшать в зависимости от индивидуальных потребностей пациента, который определяется концентрацией ІФР- 1.
Для пациентов, в которых дефицит гормона роста возник во взрослом возрасте, терапию следует начинать с низкой дозы: 0,15-0,3 мг на сутки. Дозу следует постепенно увеличивать в зависимости от индивидуальных потребностей пациента, который определяется концентрацией ІФР- 1.
В обоих случаях целью лечения является достижение концентрации ІФР- 1 в пределах величины стандартного отклонения от средней вековой нормы, которая представляет 2. Пациентам с концентрацией ІФР- 1 в пределах нормы в начале курса лечения следует применять гормон роста в дозе, нужной для увеличения концентрации ІФР- 1 к верхним пределам нормы, но не больше величина стандартного отклонения, которое представляет 2. Подбирая дозу, можно также принимать во внимание клинический эффект и побочные реакции. Известно, что у некоторых пациентов с дефицитом гормона роста, невзирая на надлежащий клинический ответ, не нормализуются уровни ІФР- 1; таким пациентам не нужно повышать дозу. Ежедневная пидтримуюча доза лишь изредка превышает 1,0 мг на сутки. Для женщин может быть нужное применение высших доз, чем для мужчин, поскольку у мужчин со временем отмечается высшая чувствительность к ІФР- 1. Это значит, что у женщин, особенно тех, кто получает пероральную естрогензамисну терапию, существует риск развития недостаточного клинического эффекта, а у мужчин - избыточного. Поэтому каждые 6 месяцы следует контролировать точность дозы гормона роста. Поскольку с возрастом происходит физиологичное уменьшение продуцирования гормону роста, можно уменьшить дозу препарата. У пациентов в возрасте от 60 лет терапию нужно начинать с дозы 0,1-0,2 мг на сутки, и дозу следует медленно повышать в зависимости от индивидуальных потребностей пациента. Следует применять минимальные эффективные дозы. Ежедневная пидтримуюча доза для этих пациентов лишь изредка превышает 0,5 мг на сутки.
Информация для пациента
Инструкция относительно применения предварительно наполненной ручки для инъекций для дозирования 5,3 мг или 12 мг
Лекарственное средство Генотропін® применяется с помощью многодозовой шприцевой ручки для инъекций одноразовой(в ручке не допускается замены картриджей), что содержит 5,3 мг или 12 мг соматропину. Препарат в ручке смешивается лишь один раз перед началом применения новой ручки. После смешивания одну ручку можно применять до 28 суток. Менять картриджи не нужно. После того как препарат в ручке был использован, начинают применения новой ручки.
Ручка имеет свойство запоминать дозу. Дозу устанавливают один раз в начале применения. После этого ручка вводит одинаковую дозу во время каждой инъекции. Возможное использование ручки с дополнительным предохранителем иглы или без него(в комплект шприцевой ручки не входит).
Перед применением ручки пациентам нужно:
- получить практические навыки под руководством медперсонала;
- получить информацию о назначенной дозе; выучить составные части ручки;
- убедиться, что для применения взято ручка с соответствующим дозированием: с синей инъекционной кнопкой(5,3 мг) или пурпуровой(12 мг).
Препарат Генотропін® в дозировании 5,3 мг выпускается в предварительно наполненной ручке с инъекционной кнопкой, логотипом и надписями синего цвета, в дозировании 12 мг - пурпурового.
Ниже приведено детальное описание последовательности применения ручки для дозирования 5,3 мг. Для дозирования 12 мг нужно выполнять аналогичные действия.
|
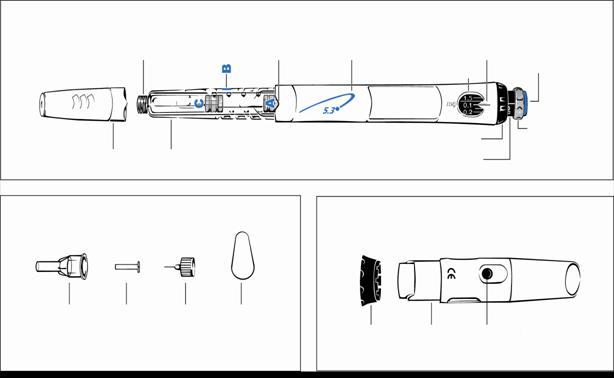
|
Внешний вид и комплектация иглы может отличаться.
Налаживание и применение новой ручки
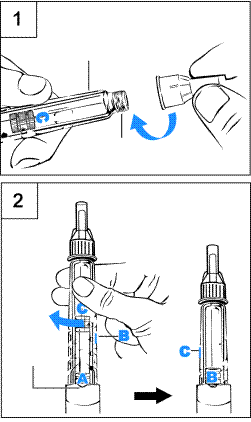
Шаг 1 Прикрепление иглы(рис 1)a. Снимите быстрым движением белый колпачок из ручки. b. Освободите от защитной пленки новую иглу. c. Крепко возьмите держателя картриджа. d. Прижмите иглу к кончику держателя картриджа. e. Аккуратно нагвинтить иглу на ручку. Не затягивайте слишком сильно. f. Оставьте оба футляра на игле. Шаг 2 Смешивание препарата(рис 2)a. Держите ручку концом иглы кверху, чтобы A было расположено перед Вашим лицом. b. Плотно вкрутите держателя картриджа в ручку к фиксации B в пазу. · Осторожно наклоните ручку со стороны в сторону. Не трясите ручку. Стряхивание может повредить гормон роста. c. Убедитесь, что жидкость в картридже является прозрачной. Весь порошок должен быть растворенным. · Если нет, осторожно наклоните ручку со стороны в сторону еще несколько раз. d. Проверьте жидкость еще раз. Убедитесь, что она является прозрачной. · Если жидкость является прозрачной, перейдите к шагу 3. · Если жидкость все еще является мутной или Вы видите порошок, применяйте новую ручку. |
|
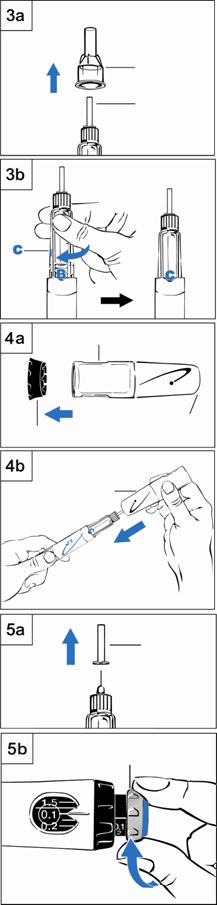
Шаг 3 Удаление воздухаa. Снимите внешний футляр из иглы(при наличии). Сохраните его, чтобы повторно закрыть иглу(рис. 3a). b. Оставьте внутренний футляр иглы на месте. c. Держите ручку кончиком иглы кверху(рис. 3b). d. Осторожно постучите по держателю картриджа, чтобы переместить пузырьки воздуха вверх. e. Плотно вкручивайте держателя картриджа в ручку, пока часть C не щелкнет в пазу. · Может появиться небольшое количество жидкости вокруг внутреннего футляра иглы. Шаг 4 Присоединение предохранителя иглы(при наличии)a. Вытяните черный колпачок из предохранителя иглы(рис. 4a). · Если экран иглы выдвигается наружу, вталкивайте его назад в предохранитель иглы, пока он не зафиксуеться на месте. b. Держите ручку в одной руке ниже синего логотипа. Второй рукой держите предохранитель иглы ниже екрана иглы(рис. 4b). c. Уровняйте черный логотип на предохранителе иглы с синим логотипом на ручке. Осторожно натягивайте предохранитель иглы на ручку, пока он не станет на место. Шаг 5 Подготовка ручки к работеa. Снимите внутренний футляр иглы(при наличии). Выбросьте его(рис. 5a). b. Убедитесь, что в окошке памяти установлено 0,1 мг. c. Возвращайте серый диск в направлении, куда указывают стрелки, пока он не прекратит щелкать(рис. 5b). |
|
|
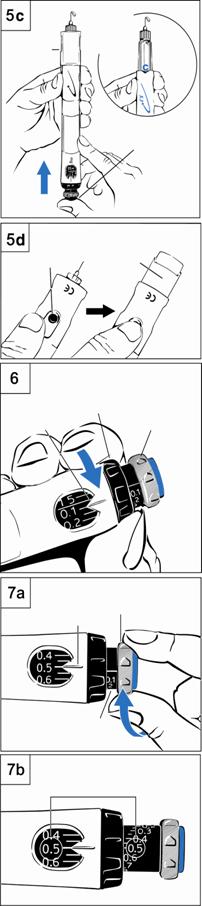
d. Держите ручку иглой кверху(рис. 5c) (с предохранителем иглы и без него). e. Жмите на синюю инъекционную кнопку, пока не появится жидкость. f. Если жидкость не появится во время шага "e", повторите этапы b - e, приведенные в данном разделе, еще не больше два раза. g. Если жидкость все равно не появляется, не используйте эту ручку. · В разделе "Вопроса/Ответ" ниже приведен более детальную информацию. h. Если Вы используете предохранитель иглы, нажмите черную кнопку фиксатора, чтобы вытянуть экран иглы(рис. 5d). Шаг 6 Установление дозы· С помощью черного кольца установите дозу. Будьте осторожные, чтобы не повернуть серый диск, устанавливая дозу. a. Держите черное кольцо, как показано на рис. 6. b. Возвращайте черное кольцо, пока доза не сравнится с белым указателем. О необходимой Вам дозе должен сообщить медперсонал. c. Если Вы повернули дозу дальше белого указателя, просто поверните черное кольцо назад, чтобы установить правильную дозу. d. После установления Вашей дозы не изменяйте ее, если только медперсонал не скажет Вам это сделать. Примечание. Если Вы не можете повернуть черное кольцо, нажмите на синюю инъекционную кнопку, пока она не прекратит щелкать. Потом продолжайте устанавливать дозу с помощью черного кольца(более детальная информация также приведена в разделе "Вопроса/Ответ" ниже). Шаг 7 Набор дозыa. Возвращайте серый диск в направлении стрелки, пока не прекратится щелкание(рис. 7a). b. Ваша доза на черном цилиндре должна уравняться с белым указателем. c. Убедитесь, что набрана Вами доза на черном цилиндре равняется дозе, которую Вы установили в окошке памяти. На рис. 7b приводится пример. d. Если дозы не сбегаются, убедитесь, что Вы повернули серый диск в направлении стрелки к прекращению щелкания. |
|
|
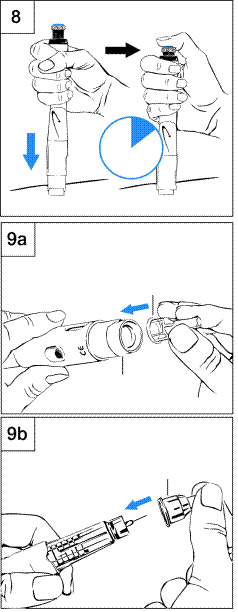
Шаг 8. Осуществление инъекции a. Подготовьте место введения в соответствии с указаниями медперсонала. b. Держите ручку над местом введения. c. Прижмите ручку, чтобы ввести иглу в кожу. d. Большим пальцем притискивайте синюю инъекционную кнопку, пока она не прекратит щелкать(рис. 8). · Отчислите 5 секунды, прежде чем вытянуть иглу из кожи. Продолжайте легко жать на кнопку большим пальцем, пока считаете. e. Вытяните ручку быстрым движением из кожи. Шаг 9 Завершение использования ручки снять иглу; ручку закрыть колпачком и положить на хранениеШаг 9a С предохранителем иглыa. Поместите внешний футляр иглы в кончик екрана иглы(рис. 9a). b. С помощью футляра иглы подтолкните экран иглы внутрь к его фиксации на месте. c. С помощью футляра иглы отвинтите иглу и положите ее в надлежащий контейнер для использованных игл. d. Оставьте предохранитель иглы на ручке. e. Наденьте черный колпачок на предохранитель иглы. Храните ручку в холодильнике. Шаг 9b Без предохранителя иглыa. Не касайтесь иглы. b. Осторожно наденьте внешний футляр на иглу(рис. 9b). c. С помощью футляра иглы отвинтите иглу и положите ее в надлежащий контейнер для использованных игл. d. Наденьте белый колпачок на ручку. Храните ручку в холодильнике. |
|
 Регулярное применение ручки
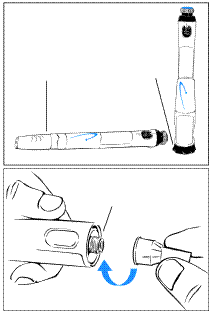
Регулярное применение ручки
|
|
|
- С предохранителем иглы :
- Если экран иглы выдвигается, втолкните его обратно на место.
- Присоедините новую иглу к кончику держателя картриджа.
|
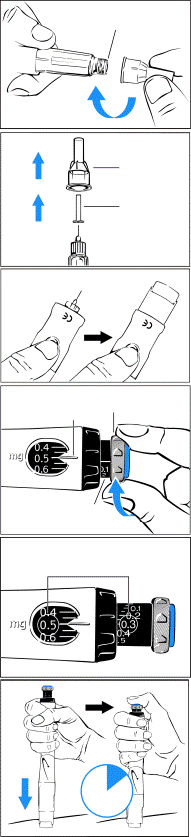
· Без предохранителя иглы : · Присоедините новую иглу к кончику держателя картриджа. 3 Снимите оба футляра иглы Сохраните внешний футляр иглы4 В случае применения предохранителя иглы нажмите черную кнопку фиксатора, чтобы выпустить экран иглы5 Чтобы набрать дозу, возвращайте серый диск, пока он не прекратит щелкать6 Убедитесь, что набранная доза равняется дозе, которая установлена в окошке памяти· Если набранная доза является меньшей, то ручка содержит неполную дозу препарата Генотропін®. · Придерживайтесь указаний медперсонала, если ручка содержит неполную дозу препарата. 7 Подготовьте место введения в соответствии с указаниями медперсонала8 Сделайте инъекцию· Прижмите ручку вниз, чтобы ввести иглу в кожу. · Нажимайте синюю инъекционную кнопку, пока она не прекратит щелкать. · Отчислите 5 секунды, прежде чем вытянуть иглу из кожи. Продолжайте легко жать на кнопку большим пальцем, пока считаете. · Вытяните ручку быстрым движением из кожи. |
|
9 Удалите иглу· С предохранителем иглы · С помощью внешнего футляра иглы вталкивайте экран иглы, пока он не станет на место. · Без предохранителя иглы · Осторожно наденьте внешний футляр на иглу. · С помощью внешнего футляра иглы выкрутите иглу. Поместите иглу в надлежащий контейнер для использованных игл. 10 Закройте колпачком предохранитель иглы или непосредственно ручку и храните ее в холодильнике |

|
Дополнительная информация
Хранение
- Через 4 недели нужно выбросить ручку, даже если некоторое количество лекарственного средства еще осталось.
- Не замораживайте ручку для инъекций и не пиддавайте влияния мороза.
Поведение
- Не смешивайте порошок и жидкость в предварительно наполненной ручке, если на ней нет иглы.
- Не храните ручку с присоединенной иглой, потому что препарат Генотропін® может выливаться из ручки, а в картридже могут образовываться воздушные пузырьки. Всегда удаляйте иглу и присоединяйте колпачок шприцевой ручки перед хранением.
- Избегайте падения ручки. Если ручка упала, необходимо опять выполнить подготовку к работе, как описано в шаге 5 подразделения "Налаживания и применения новой ручки". Но если любая часть ручки выглядит сломанной или поврежденной, не применяйте эту ручку.
- Очищайте ручку и предохранитель иглы сухой тряпкой. Не погружайте ручку в воду.
Иглы
- Всегда используйте новую иглу для каждой инъекции.
- Кладите все использованные иглы в соответствующие контейнеры для острых предметов.
- Никому не давайте для применения Вашу ручку или иглы.
Общие положения
- Цифры и линии на держателе картриджа могут помочь оценить, сколько препаратов остались в ручке.
- Если во время шага 6 регулярного использования в ручке нет полной дозы препарата Генотропін®, шкала на черном цилиндре указывает на количество лекарственного средства, которое осталось в ручке.
- Незрячие пациенты или те, кто плохо видит, должны использовать ручку только с помощью лица, которая умеет пользоваться ручкой.
- Придерживайтесь указаний медперсонала для очистки рук и кожи, когда готовитесь к проведению и осуществляете инъекцию.
Вопрос |
Ответ |
|
Что делать в случае, когда на игле после инъекции видно большее количество жидкости, чем маленькая капля? |
Во время следующей инъекции нужно подождать 5 секунды до конца, прежде чем вынимать иглу из кожи. Если Вы все еще видите какую-то жидкость после вынимания иглы, в следующий раз подождите еще немного больше. |
|
Считается ли проблемой, когда видно пузырьки воздуха в картридже? |
Нет, небольшое количество воздуха может присутствовать в картридже во время нормального приложения. |
|
Что делать, когда видно, что препарат Генотропін® вытекает из шприцевой ручки? |
Если препарат вытекает из ручки, нужно убедиться, что игла была прикреплена правильно. |
|
Что делать, если шприц-ручка, которую используют, не была положена на ночь в холодильник? |
Ручку нужно выбросить и использовать новую предварительно наполненную ручку. |
|
Что делать, если невозможно повернуть черное кольцо? |
Вероятно, что случайно был возвращен серый диск. Если серый диск возвращен, ручка не даст возвращать черное кольцо, чтобы Ваша доза не изменялась в течение инъекции. Чтобы высвободить черное кольцо, нажмите на синюю(или пурпуровую) инъекционную кнопку, пока она не остановится. Обратите внимание, что жидкость будет выходить из иглы. Потом продолжайте устанавливать дозу с помощью черного кольца. |
|
Что делать, если врач изменяет дозу после того, как уже началось лечение с помощью шприцевой ручки? |
Установить новую дозу поворотом черного кольца. |
|
Что делать, если введена неправильная доза? |
Нужно немедленно обратиться к врачу и выполнить его советы. |
|
Что делать, если шприц-ручка не будет подготовлена к работе(то есть если жидкость не появилась на шаге 5g)? |
Нужно немедленно обратиться к врачу и выполнить его советы. |
|
Какие дозы могут быть введены с помощью шприцевой ручки? |
С помощью ручки 5,3 мг можно вводить дозы от 0,10 мг до 1,5 мг препарата Генотропін®. Каждое щелкание черного кольца изменяет дозу на 0,05 мг. С помощью ручки 12 мг можно вводить дозы от 0,30 мг до 4,5 мг препарата Генотропін®. Каждое щелкание черного кольца изменяет дозу на 0,15 мг. |
Деть.
Препарат можно применять в педиатрической практике.
Передозировка
Симптомы. Острая передозировка может привести сначала к гипогликемии и впоследствии к гипергликемии. Долговременная передозировка может привести к признакам и симптомам, которые отвечают известным эффектам излишка гормона роста человека. Лечение симптоматическое.
Побочные реакции
Для пациентов с дефицитом гормона роста характерный дефицит внеклеточной жидкости. После начала лечения соматропином происходит быстрая компенсация этого дефицита жидкости. У взрослых пациентов часто возникают такие побочные реакции, связанные с задержкой жидкости, : периферический отек, скованность конечностей, артралгия, миалгия и парестезия. В целом эти побочные реакции слабо или умеренно выражены, возникают в течение первых месяцев лечения и исчезают спонтанно или после снижения дозы.
Частота этих побочных эффектов зависит от дозы препарата, возраста пациента и, возможно, обратно пропорциональная возраста, в котором возникла недостаточность гормона роста. У детей такие побочные эффекты возникают нечасто.
Наиболее серйозниб та/або самые частые а побочные реакции во время лечения соматропином :
· бвнутришнечерепни опухоли, в частности менингиомы, у подростков/молодежи, которые в детстве проходили курс лечения облучением злокачественных опухолей председателя одновременно с терапией соматропином;
· браптовий летальное следствие у детей с синдромом Прадера-Віллі с такими факторами риска, как ожирение тяжелой степени, обструкция верхних дыхательных путей или апноэ во сне и неидентифицированные респираторные инфекции в анамнезе;
· а, бпорушення толерантности к глюкозе, в том числе нарушенная гликемия натощак, а также явный сахарный диабет;
· бвиражена диабетическая ретинопатия;
· бпрогресування сколиозу у детей;
· авиявлення латентного центрального гипотиреоза;
· алипоатрофия(а также жидкие генерализуемые реакции гиперчувствительности);
· бпанкреатит(см. раздел "Особенности применения").
Генотропін® вызывает образование антител у приблизительно 1 % пациента. Эти антитела характеризуются слабой связывающей способностью, а их образование не приводило к любым клиническим изменениям.
Перечень подозреваемых побочных реакций.
Ниже поданный перечень побочных реакций за частотой: очень часто(≥1/10); часто(от ≥1/100 к <1/10); нечасто(от ≥1/1000 к <1/100); редко(от ≥1/10 000 к <1/1000); очень редко(<1/10000); частота неизвестна(не может быть установлена на основании имеющихся данных) для каждого отмеченного состояния.
Клинические исследования при участии детей с дефицитом гормона роста.
Долговременное лечение детей с задержкой росту через недостаточную секрецию гормона роста.
Доброкачественные, злокачественные и неспецифические новообразования(включая кисты и полипы). Нечасто: лейкемия†.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Частота неизвестна: парестезия*, доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Нечасто: артралгия*; частота неизвестна: миалгия*, скованность кінцівок*.
Общие расстройства и реакции в месте введения. Очень часто: реакция в месте инъекции$, частота неизвестна: периферический набряк*.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
Клинические исследования при участии детей с синдромом Тернера.
Долговременное лечение детей с задержкой росту, предопределенной синдромом Тернера.
Доброкачественные, злокачественные и неспецифические новообразования(включая кисты и полипы). Частота неизвестна: лейкемия†.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Частота неизвестна: парестезия*, доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Очень часто: артралгия*, частота неизвестна: миалгия*, скованность кінцівок*.
Общие расстройства и реакции в месте введения. Частота неизвестна: периферический отек*, реакция в месте инъекции$.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
Клинические исследования при участии детей с хронической почечной недостаточностью.
Долговременное лечение детей с задержкой росту, предопределенной хронической почечной недостаточностью.
Доброкачественные, злокачественные и неспецифические новообразования(включая кисты и полипы). Частота неизвестна: лейкемия†.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Частота неизвестна: парестезия*, доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Частота неизвестна: артралгия*, миалгия*, скованность кінцівок*.
Общие расстройства и реакции в месте введения. Часто: реакция в месте инъекции$; частота неизвестна: периферический набряк*.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
Клинические исследования при участии детей, которые родились малыми для своего гестационного возраста.
Долговременное лечение детей с задержкой росту, которые родились малыми для своего гестационного возраста.
Доброкачественные, злокачественные и неспецифические новообразования(включая кисты и полипы). Частота неизвестна: лейкемия†.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Частота неизвестна: парестезия*, доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Нечасто: артралгия*; частота неизвестна: миалгия*, скованность кінцівок*.
Общие расстройства и реакции в месте введения. Часто: реакция в месте инъекции$; частота неизвестна: периферический набряк*.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
Клинические исследования при участии детей с синдромом Прадера-Віллі.
Долговременное лечение с целью улучшения телосложения у детей с задержкой росту, предопределенной синдромом Прадера-Віллі.
Доброкачественные, злокачественные и неспецифические новообразования(включая кисты и полипы). Частота неизвестна: лейкемия†.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Часто: парестезия*, доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Часто: артралгия*, миалгия*; частота неизвестна: скованность кінцівок*.
Общие расстройства и реакции в месте введения. Часто: периферический отек*; частота неизвестна: реакция в месте инъекции$.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
Клинические исследования у взрослых с дефицитом гормона роста.
Заместительная терапия для взрослых с дефицитом гормона роста.
Со стороны обмена веществ, метаболизма. Частота неизвестна: сахарный диабет 2-го типа.
Со стороны нервной системы. Часто: парестезия*, синдром карпального канала; частота неизвестна: доброкачественная внутричерепная гипертензия.
Со стороны опорно-двигательного аппарата и соединительной ткани. Очень часто: артралгия*; часто: миалгия*, скованность кінцівок*.
Общие расстройства и реакции в месте введения. Очень часто: периферический отек*; частота неизвестна: реакция в месте инъекции$.
Обследование. Частота неизвестна: снижение уровня кортизола в крови‡.
* В целом эти побочные реакции слабо или умеренно выражены, возникают в течение первых месяцев лечения и исчезают спонтанно или после снижения дозы. Частота этих побочных реакций зависит от дозы препарата и возраста пациента. Возможно, частота обратно пропорциональна возраста пациента, когда возникла недостаточность гормона роста.
$ У детей сообщалось о кратковременных реакциях в месте инъекции.
‡ Клиническая значимость неизвестна.
† Сообщалось о возникновении данной реакции у детей с дефицитом гормона роста, которые получали лечение соматропином, но похоже, что частота ее возникновения не отличается от такой среди детей, которые не имеют дефицита гормона роста.
Во время клинических исследований дополнительно сообщалось о нижеозначенных побочных реакциях.
У детей с дефицитом гормона роста : реакции в месте инъекции, включая боль или печиння после инъекции, фиброз, нервные узлы, сыпь, воспаление, пигментацию или кровотечение; головная боль; гематурия; гипотиреоз; гипергликемия легкой степени тяжести.
У детей с синдромом Прадера-Віллі : агрессивность, выпадение волос, головная боль.
У детей с синдромом Тернера : респираторные заболевания(тонзиллит, отит, синусит, грипп), инфекции мочевыводящего тракта.
У детей из идеопатичним малым ростом: тонзиллит, назофарингит, грипп, гастроэнтерит, головная боль, увеличение аппетита, лихорадка, переломы, изменения настроения.
У взрослых с дефицитом гормона роста : гипоестезия, головная боль, боль и скованность в конечностях, боль в спине, слабость.
Дополнительно в течение надлежащего применения соматропину у детей наблюдалась гинекомастия.
Снижение уровней кортизола в сыворотке крови.
Сообщалось, что соматропин снижает уровни кортизола в сыворотке крови, возможно, за счет влияния на транспортные белки или за счет увеличения печеночного клиренса. Клиническое значение этих полученных данных может быть ограничено. Невзирая на это, следует оптимизировать заместительную терапию кортикостероидами к началу терапии препаратом Генотропін®.
Синдром Прадера-Віллі.
В постмаркетинговом периоде сообщалось об одиночных случаях внезапного летального следствия среди пациентов с синдромом Прадера-Віллі, которые получали лечение соматропином, но причинная связь с лечением не была продемонстрирована.
Лейкемия.
У детей с дефицитом гормона роста, некоторые из которых получали лечение соматропином, сообщалось о случаях лейкемии(редко или очень редко), которые наблюдались также во время постмаркетингового периода. Однако нет свидетельств повышения риска развития лейкемии без содействующих факторов, таких как лучевое облучение мозга или председателя.
Вывих головки бедренной кости или болезнь Легга-Кальве-Пертеса.
Сообщалось о вывихе головки бедренной кости и болезни Легга-Кальве-Пертеса у детей, которые получали лечение гормоном роста. Вывих головки бедренной кости чаще всего возникает при эндокринных расстройствах, а болезнь Легга-Кальве-Пертеса чаще всего наблюдается при низком росте. Однако неизвестно, или эти две патологии чаще наблюдаются при лечении соматропином. Возможность этого диагноза следует рассмотреть у ребенка с дискомфортом или болью в участке бедра или колена.
Другие побочные реакции на лекарственное средство.
Другие побочные реакции на лекарственное средство, которые могут считаться эффектами класса препаратов, к которым принадлежит соматропин, включают, в частности, возможную гипергликемию, вызванную снижением чувствительности к инсулину, снижение уровня свободного тироксина и доброкачественную внутричерепную гипертензию.
Отчетность о подозреваемых побочных реакциях.
Отчетность о подозреваемых побочных реакциях после регистрации лекарственного средства имеет важное значение. Это дает возможность осуществлять непрерывный мониторинг соотношения пользы и рисков, связанных с применением лекарственного средства.
Срок пригодности. 3 годы.
Условия хранения. Хранить при температуре 2-8 °С в оригинальной упаковке для защиты от света.
Возобновленный раствор может храниться при температуре 2-8 °С в течение 28 дней в оригинальной упаковке для защиты от света.
Хранить в недоступном для детей месте.
Несовместимость. Поскольку исследования несовместимости не проводились, данный препарат запрещено смешивать с другими лекарственными средствами.
Упаковка. 5,3 мг: 1 предварительно наполненная ручка, которая содержит 1 двухкамерный картридж(передняя камера с порошком и задняя камера с растворителем) в картонной коробке.
12 мг: 1 или 5 предварительно наполненных ручек, которые содержат 1 двухкамерный картридж(передняя камера с порошком и задняя камера с растворителем) каждая, в картонной коробке.
Категория отпуска. за рецептом.
Производитель.
Пфайзер Менюфекчуринг Бельгия НВ/Pfizer Manufacturing Belgium NV.
Местонахождение производителя и его адрес места осуществления деятельности
Рейксвег 12, Пуурс, В- 2870, Бельгия/Rijksweg 12, Puurs, В- 2870, Belgium.
Другие медикаменты этого же производителя
Форма: таблетки, покрытые пленочной оболочкой, по 5 мг по 10 таблетки в блистере, по 3 или по 6 или по 10 блистеры в пачке из картона, по 14 таблетки в блистере, по 2 блистеры в пачке из картона
Форма: порошок для раствора для инъекций по 1000 мг/1000 мг, по 2 г(1000 мг/1000 мг) порошка в флаконе; по 1, или по 5, или по 10 флаконы в картонной коробке
Форма: таблетки, покрытые пленочной оболочкой, по 50 мг по 10 таблетки в блистере; по 1 блистеру в картонной коробке
Форма: раствор для инъекций 2500 МО(анти-Ха) /0,2 мл; по 0,2 мл в одноразовом шприце; по 5 шприцы в блистере; по 2 блистеры в картонной коробке
Форма: капсулы по 300 мг по 8 капсулы в блистере; по 2 блистеры в картонной коробке