Онбрез Бризхайлер
Реєстраційний номер: UA/11706/01/02
- Склад
- Клінічні характеристики
- Показання
- Протипоказання
- Особливості застосування
- Спосіб застосування та дози
- Зняти ковпачок
- Відкрити інгалятор
- Підготовка капсули
- Проколоти капсулу
- Робіть це тільки 1 раз
- Видихнути
- Не дути у мундштук
- Вдихнути лікарський засіб
- Примітка
- Додаткова інформація
- Якщо пацієнт не чує дзижчання
- Затримка дихання
- Передозування
- Побічні реакції
- Таблиця 1 Побічні реакції
Імпортер: Новартіс Фарма АГ
Країна: ШвейцаріяАдреса імпортера: Ліхтштрассе 35, 4056 Базель, Швейцарія
Форма
порошок для інгаляцій, тверді капсули по 300 мкг № 10 (10х1), № 30 (10х3) у блістерах з 1 інгалятором
Склад
1 капсула містить індакатеролу малеату еквівалентно 300 мкг індакатеролу, що відповідає 240 мкг цільової дози, яка вивільняється;
Виробники препарату «Онбрез Бризхайлер»
Країна: Швейцарія
Адреса: Шаффхаусерштрассе, 4332 Штейн, Швейцарія
Країна: Швейцарія
Адреса: вул. Балестра, 6600 Локарно, Швейцарія
Країна: Іспанія
Адреса: Ронда де Санта Марія 158, 08210 Барбера дель Валлес, Барселона, Іспанія
Країна: Швейцарія
Адреса: Ім Ванненбоден 16, 4133 Праттельн, Швейцарія
Інструкція по застосуванню
для медичного застосування лікарського засобу
ОНБРЕЗ БРИЗХАЙЛЕР
(ONBREZ® BREEZHALER®)
Склад
діюча речовина: indacaterol maleate;
1 капсула містить індакатеролу| малеату| еквівалентно 150 мкг або 300 мкг індакатеролу, що відповідає 120 мкг або 240 мкг цільової дози, яка вивільняється;
допоміжні речовини: лактози моногідрат, желатин.
Лікарська форма. Порошок для інгаляцій, тверді капсули.
Основні фізико-хімічні властивості:
природньо прозорі
(безбарвні)|безколірні| капсули розміром 3 з
нанесеним|із| чорним кольором знаком
«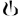 » під чорною смугою на кришці
та нанесеним |надписом|чорним кольором написом
«IDL| 150» над |цвітучорною
смугою на корпусі, містять порошок від білого до практично
білого кольору|цвіту|;
» під чорною смугою на кришці
та нанесеним |надписом|чорним кольором написом
«IDL| 150» над |цвітучорною
смугою на корпусі, містять порошок від білого до практично
білого кольору|цвіту|;
природньо прозорі
(безбарвні)|безколірні| капсули розміром 3 з
нанесеним|із| синім кольором знаком
«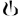 » під синьою смугою на кришці
та нанесеним |надписом|синім кольором написом
«IDL| 300» над |цвітусиньою
смугою на корпусі, містять порошок від білого до практично
білого кольору|цвіту|.
» під синьою смугою на кришці
та нанесеним |надписом|синім кольором написом
«IDL| 300» над |цвітусиньою
смугою на корпусі, містять порошок від білого до практично
білого кольору|цвіту|.
Фармакотерапевтична група. Адренергічні препарати для інгаляційного застосування. Селективні агоністи бета2-адренорецепторів.
Код АТХ R03A C18.
Фармакологічні властивості.
Фармакодинаміка.
Механізм дії
Фармакологічні ефекти агоністів бета2-адренорецепторів принаймні частково зумовлені стимуляцією внутрішньоклітинної аденілциклази, ферменту, що каталізує перетворення аденозинтрифосфату (АТФ) у циклічний-3',5'-аденозинмонофосфат (циклічний монофосфат). Підвищений рівень циклічного АМФ призводить до розслаблення гладких м'язів бронхів. Дослідження in vitro показали, що індакатерол має активність агоніста бета2-рецепторів тривалої дії, що у 24 рази вища від активності до бета1-рецепторів і в 20 разів вища від активності до бета3-рецепторів. Після інгаляції індакатерол діє місцево в легенях як бронходилататор. Індакатерол є частковим агоністом бета2-адренорецепторів людини з наномолярною активністю. В ізольованому бронху людини індакатерол продемонстрував швидкий початок та тривалість дії.
Хоча бета2-рецептори переважають серед адренорецепторів у гладких м'язах бронхів, а бета1-рецептори переважають серед рецепторів у серці людини, в людському серці також є бета2-адренорецептори, що становлять 10-50 % від загального числа адренорецепторів. Точна функція бета2-адренорецепторів у серці людини невідома, але їх присутність підвищує імовірність впливу високо селективних агоністів бета2-адренорецепторів на функцію серця.
Фармакодинамічні ефекти
Онбрез Бризхайлер, який слід приймати 1 раз на добу в дозах 150 мкг та 300 мкг, забезпечував постійне значуще покращення функції легенів (ОФВ1) протягом 24 годин під час ряду клінічних фармакодинамічних досліджень і досліджень ефективності застосування препарату. Спостерігався швидкий початок дії, протягом 5 хвилин після інгаляції препарату Онбрез Бризхайлер, з підвищенням ОФВ1 відносно початкового показника на 110-160 мл, порівняно зі швидкодіючим агоністом бета2-адренорецепторів сальбутамолом 200 мкг, і статистично значно швидший початок дії порівняно з сальметеролом/флутиказоном 50/500 мкг. Максимальний ефект препарату Онбрез Бризхайлер на ОФВ1 відносно початкового показника становив 250-330 мл у рівноважному стані. Бронхолітичний ефект не залежав від часу введення дози (вранці або ввечері).
Онбрез Бризхайлер скорочував перерозтягнення легенів як динамічне, так і в стані спокою, що призводило до збільшення дихальної ємності порівняно з плацебо.
Вплив на електрофізіологію серця
Результати подвійного сліпого, плацебо- та активно (моксифлоксацин)-контрольованого дослідження, що проводилося протягом 2 тижнів з участю 404 здорових добровольців, продемонстрували максимальне середнє (90 % довірчі інтервали) подовження інтервалу QTcF (у мс) - 2,66 (0,55, 4,77), 2,98 (1,02, 4,93) і 3,34 (0,86, 5,82) після застосування багаторазових доз препарату (150 мкг, 300 мкг і 600 мкг відповідно). Таким чином, це вказує на відсутність ризику щодо проаритмічного потенціалу, пов'язаного з подовженням інтервалу QT при застосуванні рекомендованих терапевтичних доз препарату або доз, що в два рази перевищують максимальну рекомендовану дозу. Даних щодо зв'язку концентрації препарату з дельта QTc в діапазоні оцінюваних доз отримано не було.
Як було продемонстровано в 26-тижневому подвійному сліпому плацебо-контрольованому дослідженні фази III з участю 605 пацієнтів з ХОЗЛ, клінічно значуща відмінність у розвитку явищ аритмії при 24-годинному моніторингу на початковому рівні і тричі протягом 26-тижневого лікування не спостерігалася між пацієнтами, які отримували рекомендовані дози препарату Онбрез Бризхайлер, і пацієнтами, які отримували плацебо або тіотропій.
Клінічна ефективність і безпека
Програма клінічних досліджень включала одне 12-тижневе дослідження, два 6-місячних дослідження (одне з яких було подовжено до одного року для оцінки безпеки застосування і переносимості препарату) і одне однорічне рандомізоване контрольоване дослідження з участю пацієнтів з клінічним діагнозом ХОЗЛ. Ці дослідження включали такі критерії оцінювання функції легень і стану здоров'я як задишка, загострення захворювання і пов'язана зі здоров'ям якість життя.
Функція легень
При застосуванні препарату Онбрез Бризхайлер в дозах 150 мкг і 300 мкг 1 раз на добу, наявне клінічно значуще покращення функції легень. У 12-тижневій первинній кінцевій точці
(24-годинний мінімальний ОФВ1) застосування препарату в дозі 150 мкг призвело до збільшення показника на 130-180 мл порівняно із застосуванням плацебо (p<0,001) і до збільшення показника на 60 мл порівняно із застосуванням сальметеролу в дозі 50 мкг два рази на добу (p<0,001). Застосування препарату в дозі 300 мкг призвело до збільшення показника на 170-180 мл порівняно із застосуванням плацебо (p<0,001) і до збільшення показника на 100 мл порівняно із застосуванням формотеролу в дозі 12 мкг два рази на добу (p<0,001). Застосування обох доз препарату призвело до збільшення на 40-50 мл показника порівняно з незамаскованим застосуванням тіотропію в дозі 18 мкг 1 раз на добу (150 мкг, p=3D0,004; 300 мкг, p=3D0,01).
24-годинний бронхолітичний ефект препарату Онбрез Бризхайлер підтримувався після застосування першої дози протягом однорічного періоду лікування без ознак втрати ефективності (тахіфілаксії).
Симтоматичні переваги
Обидві дози показали статистично значуще полегшення симптомів захворювання порівняно із застосуванням плацебо - задишки і стану здоров'я, які оцінювалися за допомогою динамічного індексу задишки (TDI) та опитування госпіталю Святого Георгія для оцінки дихальної функції (SGRQ) відповідно. Величина відповіді була зазвичай вищою, ніж це було виявлено при застосуванні активних препаратів порівняння (Таблиця). Крім того, пацієнти, які отримували препарат Онбрез Бризхайлер, потребували застосування значно меншої кількості лікарських засобів невідкладної допомоги, мали значно більшу кількість днів, коли не було потреби у застосуванні цих препаратів порівняно з плацебо, а також мали значно більший відсоток днів з відсутністю симптомів захворювання у денний час.
Об'єднаний аналіз даних ефективності лікування протягом 6 місяців показав, що частота випадків загострення ХОЗЛ була статистично значуще нижчою, ніж частота випадків загострення захворювання у групі застосування плацебо. При зіставленні видів лікування порівняно з плацебо при застосуванні препарату в дозах 150 мкг і 300 мкг були визначені співвідношення частот на рівні 0,68 (95 % ДІ [0,47, 0,98]; p-значення 0,036) і 0,74 (95 % ДI [0,56, 0,96]; p-значення 0,026) відповідно. Стосовно осіб африканського походження досвід лікування препаратом обмежений.
Таблиця Полегшення симптомів при проведенні лікування тривалістю 6 місяців
|
Доза препарату (мкг) |
Індакатерол 150 1 раз на добу |
Індакатерол 300 1 раз на добу |
Тіотропій 18 1 раз на добу |
Сальметерол 50 2 рази на добу |
Формотерол 12 2 рази на добу |
Плацебо |
|
Відсоток пацієнтів, які досягли MCID TDI† |
57а 62b |
71b 59c |
57b |
54a |
54c |
45a 47b 41c |
|
Відсоток пацієнтів, які досягли MCID SGRQ† |
53a 58b |
53b 55c |
47b |
49a |
51c |
38a 46b 40c |
|
Зниження кількості впорску-вань/добу лікарського засобу, що застосо-вується для невідкладної допомоги, порівняно з початковим рівнем |
1,3a 1,5b |
1,6b |
1,0b |
1,2a |
н/о |
0,3a 04b |
|
Відсоток днів, коли лікарські засоби для невідкладної допомоги не застосову-валися |
60a 57b |
58b |
46b |
55a |
н/о |
42a 42b |
Дизайн дослідження із застосуванням
а індакатеролу в дозі 150 мкг, сальметеролу і плацебо;
b індакатеролу в дозах 150 і 300 мкг, тіотропію і плацебо;
с індакатеролу в дозі 300 мкг, формотеролу і плацебо.
†MCID - мінімальна клінічно важлива відмінність (зміна в TDI на ≥ 1 пункт, зміна в SGRQ на
≥ 4 пункти).
н/о - не оцінювалося впродовж шести місяців.
Педіатрична популяція
Європейське агентство з лікарських засобів відмовилося від зобов'язання представити результати досліджень препарату Онбрез Бризхайлер в усіх підгрупах педіатричної популяції при хронічному обструктивному захворюванні легень (ХОЗЛ).
Фармакокінетика.
Абсорбція
Середній час досягнення максимальної концентрації індакатеролу| в сироватці крові становив приблизно 15 хвилин|мінути| після|потім| введення|вступу| одноразових|однократних| або повторних інгаляційних доз. Системна дія індакатеролу| збільшувалася при пропорційному підвищенні дози (з 150 мкг до 600 мкг). Абсолютна біодоступність індакатеролу| після|потім| застосування|вживання| інгаляційної дози у середньому становила 43 %. Системна дія зумовлюється| поєднанням абсорбції індакатеролу| в легенях (приблизно 75 %) і кишечнику (приблизно 25 %).
Концентрація індакатеролу| в сироватці крові підвищується при повторному введенні|вступі| індакатеролу| 1 раз на добу. Рівноважний стан|достаток| досягається протягом 12-14 днів. Середнє відношення|ставлення| кумуляції індакатеролу|, тобто AUC| за 24-годинний|годинниковий| інтервал дозування на 14-й день порівняно з 1-м днем знаходилося|перебувало| в діапазоні від 2,9 до 3,5 для інгаляційних доз від 150 мкг до 600 мкг 1 раз на добу.
Розподіл
Після внутрішньовенної інфузії об'єм розподілу індакатеролу протягом фази кінцевого виведення становив 2557 літрів, що свідчить про значний розподіл індакатеролу. Зв'язування індакатеролу in vitro з білками сироватки і плазми крові становило 94,1-95,3 % і 95,1-96,2 % відповідно.
Біотрансформація
Після|потім| перорального застосування|вживання| радіоактивно міченого індакатеролу| під час дослідження ADME| (абсорбції, розподілу, метаболізму і виведення) у людей індакатерол| в незміненому вигляді|виді| був|з'являвся| основним компонентом, що виявлявся в сироватці крові і становив близько третини сумарного показника AUC| за 24 години. Гідроксильований похідний метаболіт був|з'являлося| найбільш значущим |у сироватці крові. Фенольний О-глюкуронід індакатеролу| і гідроксильований індакатерол| також були значущими метаболітами|. Також були визначені такі метаболіти|: діастереомер| гідроксильованого похідного, N-глюкуронід| індакатеролу| та С- і N-деалкільовані| продукти.
Дослідження in vitro показали, що ізоформа UGT1А1 виявляється єдиною ізоформою уридиндифосфатглюкуронозилтрансферази (UGT), що метаболізувала індакатерол до фенольного О-глюкуроніду. Окиснювальні метаболіти були знайдені при інкубації з рекомбінантними CYP1A1, CYP2D6 і CYP3A4. CYP3A4 вважається домінуючим ізоферментом, що бере участь у процесі гідроксилювання індакатеролу. Дослідження in vitro також показали, що індакатерол є низькоафінним субстратом для еффлюксної помпи Р-gp.
Виведення
У клінічних дослідженнях, що включали аналіз сечі, кількість індакатеролу, виведеного в незміненому вигляді з сечею, в цілому була нижча, ніж 2 % від дози. Нирковий кліренс індакатеролу в середньому становив 0,46-1,20 л/год. При порівнянні з сироватковим кліренсом індакатеролу 23,3 л/годину, стає очевидним, що нирковий кліренс відіграє незначну роль (приблизно 2-5 % системного кліренсу) у виведенні системно доступного індакатеролу.
У дослідженні ADME з участю пацієнтів, в якому індакатерол застосовували перорально, шлях виведення індакатеролу з калом переважав над виведенням індакатеролу з сечею. Індакатерол виводився з калом людини в основному у вигляді незміненої вихідної речовини (54 % дози) і меншою мірою - у вигляді гідроксильованих метаболітів індакатеролу (23 % дози). Баланс маси був повним при ≥ 90 % дози, визначеної у виділеннях.
Концентрація індакатеролу| в сироватці крові зменшується в декілька етапів із середнім значенням кінцевого періоду напіввиведення в діапазоні від 45,5 до 126 годин. Ефективний період напіввиведення, визначений на підставі показника кумуляції індакатеролу| після|потім| введення|вступу| повторної дози, варіював у діапазоні від 40 до 52 годин, що узгоджується з часом для досягнення рівноважного стану, який становить близько 12-14 днів.
Особливі групи пацієнтів
Популяційний фармакокінетичний аналіз даних не виявив клінічно значущого впливу віку (дорослі віком до 88 років), статі, маси тіла (32-168 кг) або раси на фармакокінетику індакатеролу. Цей аналіз не виявив жодної різниці між етнічними підгрупами в цій групі населення.
Відповідні зміни в показниках Cmax або AUC індакатеролу у пацієнтів з порушеннями функції печінки легкого або помірного ступеня не спостерігалися, також не спостерігалися відмінності у зв'язуванні індакатеролу з білками крові у пацієнтів з порушеннями функції печінки легкого або помірного ступеня порівняно зі здоровими учасниками дослідження в контрольних групах. Дослідження з участю пацієнтів з порушеннями функції печінки тяжкого ступеня не проводилися.
Через дуже низький відсоток виведення індакатеролу з сечею відносно загального виведення препарату з організму дослідження з участю пацієнтів з порушеннями функції нирок не проводили.
Клінічні характеристики
Показання
Підтримуюча бронходилатаційна терапія обструкції дихальних шляхів у дорослих пацієнтів із хронічним обструктивним захворюванням легенів (ХОЗЛ).
Протипоказання
Гіперчутливість до діючої речовини, лактози або будь-якої з інших допоміжних речовин.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Симпатоміметичні засоби|кошти|
Одночасне застосування|вживання| інших симпатоміметичних засобів|коштів| (як монотерапія або як частина|частка| комбінованої терапії) може посилити|посилювати| небажані ефекти препарату Онбрез Бризхайлер.
Онбрез Бризхайлер не слід застосовувати разом з іншими агоністами бета2-адренорецепторів тривалої дії або лікарськими засобами, що містять агоністи бета2-адренорецепторів тривалої дії.
Гіпокаліємія
Супутнє лікування похідними метилксантину, стероїдами або некалійзберігаючими діуретиками може посилити можливий гіпокаліємічний ефект агоністів бета2-адренорецепторів, тому вимагає обережності.
Блокатори бета-адренорецепторів|
Блокатори бета-адренорецепторів можуть послабити або протидіяти ефекту агоністів бета2-адренорецепторів. Отже, індакатерол не можна застосовувати разом з блокаторам бета-адренорецепторів (включаючи очні краплі), за винятком випадків їх вимушеного обгрунтованого застосування. У разі необхідності слід віддати перевагу кардіоселективним блокаторам бета-адренорецепторів, хоча застосовувати їх слід з обережністю.
Взаємодія з лікарськими засобами, що подовжують інтервал QT
Онбрез Бризхайлер, як і інші агоністи бета2-адренорецепторів, необхідно застосовувати з обережністю пацієнтам, які отримували інгібітори моноамінооксидази, трициклічні антидепре-санти або лікарські засоби, що подовжують інтервал QT, через можливе потенціонування будь-якого впливу на QT інтервал.
Лікарські засоби, які продовжують QT інтервал, можуть збільшувати ризик виникнення шлуночкової аритмії.
Метаболізм і переносники, залучені у лікарські взаємодії
Пригнічення дії основних метаболітів кліренсу індакатеролу|, CYP3A4| і Р-глікопротеїну| (Р-gp) не впливає на безпеку застосування препарату Онбрез Бризхайлер у терапевтичних дозах. Проведено дослідження лікарської взаємодії із застосуванням сильнодіючих та специфічних інгібіторів CYP3A4| і Р-глікопротеїну| (Р-gp) (наприклад, кетоконазол, еритроміцин, верапаміл, ритонавір). Застосування верапамілу в якості прототипу інгібітора Р-глікопротеїну| (Р-gp) призводило до підвищення системної експозиції індакатеролу в 1,4-2 рази та Cmax в 1,5 раз. Сумісне застосування препарату Онбрез Бризхайлер з еритроміцином призводило до підвищення системної експозиції індакатеролу в 1,6 раза та Cmax в 1,2 раза. Застосування кетоконазолу як сильнодіючого подвійного інгібітора Р-глікопротеїну| (Р-gp) та CYP3A4 призводило до підвищення системної експозиції індакатеролу в 2 рази та Cmax в 1,4 раза. Сумісне застосування з ритонавіром, іншим подвійним інгібітором CYP3A4 та Р-глікопротеїну| (Р-gp), призводило до підвищення системної експозиції в 1,6-1,8 раза та не впливало на Cmax.
Узагальнені наведені дані свідчать про те, що зміна активності як Р-глікопротеїну| (Р-gp), так і CYP3A4| впливає на системний кліренс. Двократне підвищення системної експозиції, зумовлене впливом сильнодіючого подвійного інгібітора кетоконазолу, відображає вплив комбінованого інгібування.
Збільшення величини експозиції препарату в результаті лікарських взаємодій не знижує безпеки застосування препарату, про що свідчить досвід лікування препаратом Онбрез Бризхайлер у клінічних дослідженнях до одного року в дозах, які у 2-4 рази перевищують максимальну рекомендовану терапевтичну дозу.
Не було виявлено, що індакатерол призводить до лікарських взаємодій із супутніми лікарськими препаратами. Дослідження in vitro показали, що індакатерол має незначний потенціал спричиняти метаболічні взаємодії з лікарськими препаратами на рівні системної дії, що досягалося у клінічній практиці.
Особливості застосування
Бронхіальна астма
Препарат Онбрез Бризхайлер є агоністом бета2-адренорецепторів тривалої дії, показаний для застосування тільки при ХОЗЛ. Онбрез Бризхайлер не слід застосовувати при бронхіальній астмі через відсутність даних щодо наслідків|за результатами| довгострокового застосування|вживання| Онбрез Бризхайлер при цьому захворюванні. Агоністи бета2-адренорецепторів тривалої дії можуть збільшувати ризик серйозних небажаних явищ, пов'язаних з астмою, включаючи летальні, при використанні для лікування астми.
Гіперчутливість
Повідомлялося про реакції гіперчутливості негайного типу після застосування препарату Онбрез Бризхайлер. Якщо спостерігаються симптоми, що свідчать про алергічні реакції (зокрема утруднення дихання або ковтання, набряк язика, губ та обличчя, кропив'янка, шкірні висипання), застосування препарату Онбрез Бризхайлер слід негайно припинити та розпочати альтернативну терапію.
Парадоксальний бронхоспазм
Як і при застосуванні|вживанні| іншої інгаляційної терапії, застосування|вживання| Онбрез Бризхайлер може призвести до виникнення парадоксального бронхоспазму, що може бути небезпечним для життя. У такому випадку застосування|вживання| Онбрез Бризхайлер слід негайно припинити і розпочати|розпочинати| |вживання|альтернативну терапію.
Збільшення тяжкості захворювання
Онбрез Бризхайлер не показаний на початку лікування гострих епізодів бронхоспазму, тобто як ургентна терапія. У разі|в разі| збільшення тяжкості ХОЗЛ під час застосування|вживання| препарату Онбрез Бризхайлер слід провести повторну оцінку стану|достатку| здоров'я пацієнта і режиму лікування ХОЗЛ. Підвищувати добову дозу препарату Онбрез Бризхайлер більше максимальної дози 300 мкг не рекомендується.
Системні ефекти
Хоча після застосування препарату Онбрез Бризхайлер у рекомендованих дозах клінічно значущого ефекту на серцево-судинну систему зазвичай не спостерігається, як і у разі застосування інших агоністів бета2-адренорецепторів, індакатерол необхідно обережно застосовувати пацієнтам із серцево-судинними захворюваннями, особливо коронарною недостатністю, гострим інфарктом міокарда, серцевою аритмією та артеріальною гіпертензією, пацієнтам із судомними розладами або тиреотоксикозом, а також пацієнтам, які неадекватно реагують на дію агоністів бета2-адренорецепторів.
Серцево-судинні ефекти
Як і інші агоністи бета2-адренорецепторів, індакатерол може спричиняти клінічно значущий ефект на серцево-судинну систему у деяких пацієнтів, що проявляється підвищенням частоти пульсу, підвищенням артеріального тиску та/або іншими симптомами. У такому разі може виникнути необхідність у відміні препарату. Крім того, повідомлялося, що агоністи бета2-адренорецепторів призводять до змін ЕКГ, таких як згладжування зубця Т, подовження інтервалу QT і депресії сегмента ST. Клінічна значущість цих даних невідома. Тому агоністи бета2-адренорецепторів тривалої дії, такі як Онбрез Бризхайлер, слід з обережністю застосовувати пацієнтам зі встановленим або підозрюваним подовженням інтервалу QT або які отримують лікарські засоби, що впливають на інтервал QT.
Клінічно значущі ефекти на подовження інтервалу QT не спостерігалися у клінічних дослідженнях препарату Онбрез Бризхайлер при застосуванні рекомендованих терапевтичних доз.
Гіпокаліємія
У деяких пацієнтів агоністи бета2-адренорецепторів можуть спричинити виникнення вираженої гіпокаліємії, що може призвести до розвитку небажаних ефектів з боку серцево-судинної системи. Зменшення вмісту калію у сироватці крові зазвичай тимчасове та не вимагає поповнення. У пацієнтів з ХОЗЛ тяжкого ступеня гіпокаліємія може бути посилена гіпоксією і супутнім лікуванням, що може підвищити схильність до серцевої аритмії.
Гіперглікемія
Інгаляція високих доз агоністів бета2-адренергічних рецепторів може спричинити підвищення рівня глюкози у плазмі крові. Після початку лікування препарату Онбрез Бризхайлер слід більш ретельно контролювати рівні глюкози у плазмі крові у пацієнтів, хворих на цукровий діабет.
Протягом клінічних досліджень клінічно значущі зміни рівня глюкози у плазмі крові були частішими (на 1-2 %) у пацієнтів, які застосовували Онбрез Бризхайлер у рекомендованих дозах, ніж у тих, хто приймав плацебо. Вплив препарату Онбрез Бризхайлер не досліджували у пацієнтів з погано контрольованим цукровим діабетом.
Допоміжні речовини
Капсули містять лактозу. Пацієнтам з рідкісними спадковими формами непереносимості галактози, дефіциту лактази Лаппа або глюкозо-галактозної мальабсорбції не слід приймати цей лікарський засіб.
Застосування у період вагітності або годування груддю.
Вагітність
Дані щодо дії препарату Онбрез Бризхайлер у період вагітності відсутні. Дослідження на тваринах не свідчать про прямий або опосередкований негативний вплив на репродуктивну функцію. Як і інші агоністи бета2-адренорецепторів, індакатерол може пригнічувати пологову діяльність через розслабляючу дію на гладкі м'язи матки. Індакатерол| у період вагітності слід застосовувати тільки|лише| у випадках, коли очікувана|сподівана| користь для матері| перевищує потенційний ризик для плода.
Період годування груддю
Невідомо, чи потрапляє індакатерол/метаболіти у грудне молоко людини. Наявні фармакокінетичні/токсикологічні дані демонструють екскрецію індакатеролу/метаболітів у молоко тварин. Ризик для дитини на грудному вигодовуванні не можна виключити. Рішення щодо відмови від годування груддю або відміни терапії препаратом Онбрез Бризхайлер слід приймати з урахуванням користі грудного годування для дитини та переваг терапії для жінки.
Фертильність
У щурів спостерігалося зниження відсотка вагітностей. Однак вважається малоймовірним, що індакатерол буде впливати на репродуктивну функцію та фертильність після інгаляції максимально рекомендованої дози.
Здатність впливати на швидкість реакції при керуванні автотранспортом або з іншими механізмами.
Онбрез Бризхайлер зазвичай не впливає або впливає незначним чином на здатність керувати автотранспортом та працювати з іншими механізмами, але слід враховувати можливість розвитку побічних реакцій з боку нервової системи (див. розділ «Побічні реакції»).
Спосіб застосування та дози
Застосовувати дорослим.
Рекомендована доза - інгаляція вмісту 1 капсули Онбрез Бризхайлер 150 мкг за допомогою інгалятора Онбрез Бризхайлер 1 раз на добу. Дозу можна збільшувати тільки|лише| за рекомендацією лікаря|лікарки|.
Інгаляція вмісту 1 капсули Онбрез Бризхайлер 300 мкг 1 раз на добу за допомогою інгалятора Онбрез Бризхайлер продемонструвала додаткову клінічну перевагу в послабленні (усуненні) задишки у пацієнтів із тяжкою формою ХОЗЛ. Максимальна доза - 300 мкг 1 раз на добу.
Онбрез Бризхайлер слід застосовувати в один і той самий час кожного дня.
При пропуску дози наступну|таку| дозу потрібно приймати у той же|звичний| самий час наступного дня.
Пацієнти літнього віку
Максимальна плазмова концентрація та загальна системна експозиція зростають з віком, але корекція дози пацієнтам літнього віку не потрібна.
Порушення функції печінки або нирок
Для пацієнтів з|із| порушеннями функції печінки легкого або помірного ступеня|міри||тягаря| корекція дози не потрібна. Даних щодо застосування препарату пацієнтам з|із| порушеннями функції печінки тяжкого|тяжкого| ступеня|міри| немає. Для пацієнтів з|із| порушеннями функції нирок корекція дози не потрібна.
Спосіб застосування|вживання|
Онбрез Бризхайлер, капсули, слід застосовувати тільки|лише| перорально інгаляційно і лише за допомогою інгалятора Онбрез Бризхайлер.
Капсули Онбрез Бризхайлер ковтати не можна.
Інструкція щодо використання інгалятора.
При кожному призначенні препарату слід застосовувати новий інгалятор Онбрез Бризхайлер. Слід утилізувати інгалятор через 30 днів використання.
|
|
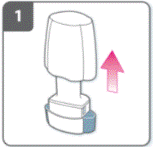
Зняти ковпачок |
|
|
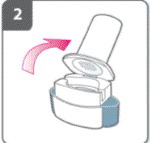
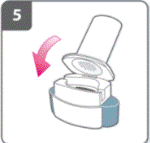
Відкрити інгаляторУтримувати основу інгалятора міцно та нахилити мундштук. Це відкриває інгалятор. |
|
|
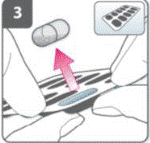
Підготовка капсулиБезпосередньо перед використанням сухими руками вийняти 1 капсулу з блістера. |
|
|
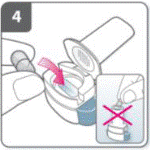
Помістити капсулу: Вставити капсулу у капсульний відсік. Ніколи не розміщувати капсулу безпосередньо у мундштук. |
|
|
Закрити інгалятор: Закривати інгалятор до клацання. |
|
|
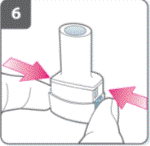
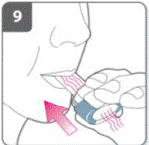
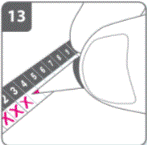
Проколоти капсулу- Тримати інгалятор у вертикальному положенні так, щоб мундштук був спрямований догори. - Проколоти капсулу шляхом одночасного сильного натискання на обидві бічні кнопки. Робіть це тільки 1 раз- У той момент, як капсула проколюється, можна почути клацання. |
|
|
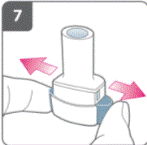
Повністю відпустити бічні кнопки |
|
|
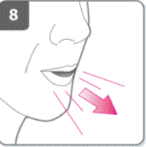
ВидихнутиПерш ніж помістити мундштук у рот, зробити повний видих. Не дути у мундштук |
|
|
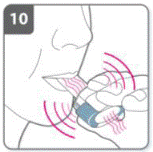
Вдихнути лікарський засібДля того, щоб лікарський засіб потрапив глибоко до дихальних шляхів, необхідно: - Тримати інгалятор, як це показано на малюнку. Бічні кнопки мають бути розташовані перед пацієнтом ліворуч та праворуч. Не стискати бічні кнопки. - Помістити мундштук у рот та щільно стиснути його губами. - Зробити швидкий, але рівномірний вдих так глибоко, як тільки можна. |
|
|
ПриміткаПід час вдиху через інгалятор капсула обертається у камері, і можна чути дзижчання. Пацієнт відчує солодкий аромат, як тільки ліки почнуть потрапляти до легень. Додаткова інформаціяІноді дуже маленькі частки капсули можуть пройти через захисну сітку та потрапити до рота. Якщо це трапиться, можна відчути ці частки на язику. Це не шкідливо, якщо ці частки ковтати або вдихати. Імовірність подрібнення капсули збільшуватиметься, якщо її випадково проколоти більше одного разу (пункт 6). Якщо пацієнт не чує дзижчанняКапсулу може заклинити у камері. Якщо це трапиться: · Відкрити інгалятор і обережно вивільнити капсулу, постукуючи по основі інгалятора. Не натискати на бокові кнопки. · Знову вдихнути ліки, повторивши пункти 8 та 9. |
|
|
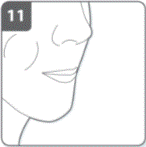
Затримка диханняПісля того, як пацієнт вдихнув ліки: · Затримати дихання, принаймні на 5-10 секунд або на скільки можна, не відчуваючи незручності, одночасно виймаючи інгалятор з рота. · Потім зробити видих. · Відкрити інгалятор та перевірити капсулу на залишки порошку. Якщо в капсулі залишився порошок· Закрити інгалятор. · Повторити пункти 8, 9, 10 та 11. Більшість людей може спорожнити капсулу одним або двома вдихами. Додаткова інформаціяДеякі люди можуть іноді нетривалий час кашляти одразу після вдихання лікарського засобу. Якщо таке трапилося, не слід хвилюватися. Якщо капсула порожня, пацієнт отримав достатню кількість лікарського засобу. |
|
|
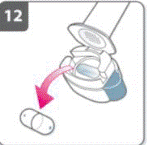
Після завершення прийому лікарського засобу: · Знову відкрити мундштук та видалити порожню капсулу, нахиляючи камеру, щоб капсула випала. Порожню капсулу викинути у побутові відходи. · Закрити інгалятор та вставити на місце ковпачок. Не зберігати капсули в інгаляторі «Onbrez Breezhaler». |
|
|
Робити помітки у щоденному календарі контролю введення лікарського засобу: З внутрішнього боку упаковки є щоденний календар введення препарату. Поставити відмітку в квадратику, що відповідає сьогоднішньому дню, якщо це допоможе нагадати, коли слід прийняти наступну дозу препарату. |
Діти.
Немає даних щодо відповідного застосування препарату Онбрез Бризхайлер дітям (до 18 років).
Передозування
У пацієнтів із|із| ХОЗЛ одноразові|однократні| дози, що перевищують максимальну рекомендовану терапевтичну дозу в 10 разів, були пов'язані з помірним підвищенням частоти пульсу, підвищенням систолічного тиску|тиснення| крові та інтервалу QTc|.
Передозування індакатеролу може призвести до посилення ефектів, характерних для стимуляторів бета2-адренорецепторів, тобто тахікардії, тремору, прискореного серцебиття, головного болю, нудоти, блювання, сонливості, шлуночкової аритмії, метаболічного ацидозу, гіпокаліємії та гіперглікемії.
При передозуванні індакатеролом| показано підтримуюче і симптоматичне лікування. У тяжких випадках пацієнта необхідно госпіталізувати. Можливе|розглядувати| застосування|вживання| кардіоселективних| бета-блокаторів|, але тільки|лише| під наглядом лікаря|лікарки| і з|із| надзвичайною обережністю, оскільки їх застосування|вживання| може спровокувати бронхоспазм.
Побічні реакції
Профіль безпеки
Найчастішими побічними реакціями при застосуванні|вживанні| рекомендованих доз препарату були назофарингіт (14,3 %), інфекції верхніх дихальних шляхів|колій| (14,2 %), кашель (8,2 %), головний біль (3,7 %) і м'язові спазми (3,5 %). В основному ступінь|міра| вираженості|виказувати| цих побічних реакцій був легким або помірним, частота зменшувалася при продовженні лікування.
У рекомендованих дозах профіль небажаних реакцій препарату Онбрез Бризхайлер у пацієнтів з ХОЗЛ показує клінічно незначні системні ефекти стимуляції бета2-адренорецепторів. Зміни середньої частоти серцевих скорочень становили менше 1 удару на хвилину, тахікардія розвивалася рідко і з такою ж частотою, що і в групі прийому плацебо. Відповідне подовження інтервалу QTсF не було виявлено порівняно з групою прийому плацебо. Частота виникнення значущих інтервалів QTсF [тобто >450 мс (у чоловіків) і >470 мс (у жінок)] і гіпокаліємії були такими ж, як і в групі прийому плацебо. Середнє значення максимальних змін вмісту глюкози в крові було аналогічним у групамах прийому препарату Онбрез Бризхайлер і плацебо.
Перелік побічних реакцій у таблиці
У програмі клінічних досліджень фази III препарату Онбрез Бризхайлер брали участь пацієнти із клінічним діагнозом ХОЗЛ помірного або тяжкого ступеня. 4764 пацієнти застосовували індакатерол впродовж одного року у дозах, що до двох разів перевищували максимальну рекомендовану дозу. Із цих пацієнтів 2611 застосовували препарат у дозі 150 мкг 1 раз на добу і 1157 - 300 мкг 1 раз на добу. Приблизно 41 % пацієнтів мали ХОЗЛ тяжкого ступеня. Середній вік пацієнтів становив 64 роки, причому 48 % пацієнтів були віком понад 65 років. Більшість пацієнтів (80 %) належали до європеоїдної раси.
Побічні реакції наведено за класами систем органів згідно з MedDRA та впорядковано за частотою виникнення в порядку спадання: дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000,
< 1/100); рідко (≥ 1/10000, < 1/1000); дуже рідко (< 1/10000); невідомо (не можна оцінити за наявними даними).
Таблиця 1 Побічні реакції
|
Побічні реакції |
Категорія частоти для дози 150 мкг |
Категорія частоти для дози 300 мкг |
|
Інфекції та інвазії Інфекції верхніх дихальних шляхів Назофарингіт Синусит |
Часто Часто Часто |
Дуже часто Дуже часто Часто |
|
З боку імунної системи Підвищена чутливість1 |
Нечасто |
Нечасто |
|
З боку обміну речовин та харчування Цукровий діабет і гіперглікемія |
Нечасто |
Часто |
|
З боку нервової системи Головний біль Запаморочення Парестезія |
Часто Часто Нечасто |
Часто Часто Нечасто |
|
Кардіологічні порушення Ішемічна хвороба серця Фібриляція передсердь Відчуття серцебиття Тахікардія |
Нечасто Нечасто Нечасто Нечасто |
Часто Нечасто Часто Нечасто |
|
З боку дихальної системи, органів грудної клітки та середостіння Кашель Орофарингеальний біль, включаючи подразнення у горлі Ринорея Парадоксальний бронхоспазм |
Часто Часто Часто Нечасто |
Часто Часто Часто Нечасто |
|
З боку шкіри та підшкірної клітковини Свербіж/висипання |
Нечасто |
Часто |
|
З боку кістково-м'язової системи та сполучної тканини М'язовий спазм Міалгія Кістково-м'язовий біль |
Часто Нечасто Нечасто |
Часто Нечасто Часто |
|
Системні порушення та ускладнення у місці введення препарату Біль у грудній клітці Периферичні набряки |
Часто Часто |
Часто Часто |
1Повідомлення про випадки підвищеної чутливості стосувалися досвіду застосування препарату Онбрез Бризхайлер у післяреєстраційний період. Ці повідомлення були отримані на добровільній основі від популяції невизначеного розміру, таким чином, не завжди можливо достовірно оцінити частоту або встановити причинно-наслідковий зв'язок з експозицією лікарського засобу. Тому частота була розрахована, виходячи з досвіду застосування препарату під час проведення клінічних досліджень.
При застосуванні дози 600 мкг 1 раз на добу профіль безпеки препарату Онбрез Бризхайлер в цілому|загалом| був аналогічним|із| такому при застосуванні рекомендованих доз. До додаткових побічних реакцій належить тремор (часто).
Окремі побічні реакції на препарат
Під час клінічних досліджень фази III спостерігалося, що у середньому у 17-20 % пацієнтів виникав спорадичний кашель, який розпочинався протягом 15 секунд після|потім| інгаляції і зазвичай|звично| тривав 5 секунд (приблизно 10 секунд у курців). Кашель спостерігався частіше у жінок, ніж у чоловіков, та у курців. Цей кашель зазвичай|звично| переносився добре і не призводив|призводив| до припинення участі пацієнта в дослідженнях при застосуванні рекомендованих доз (кашель є симптомом ХОЗЛ, і тільки 8,2 % пацієнтів повідомляли про кашель як побічну реакцію). Даних про те, що постінгаляційний кашель пов'язаний з бронхоспазмом, ускладненнями, збільшенням тяжкості захворювання або зниженням ефективності лікування, немає.
Термін придатності. 2 роки.
Умови зберігання. Зберігати при температурі не вище 30 °С в оригінальній упаковці для захисту від вологи. Зберігати в недоступному для дітей місці.
Упаковка. По 10 капсул у блістері; по 1 або 3 блістери разом з інгалятором у картонній коробці.
Категорія відпуску. За рецептом.
Виробник.
Новартіс Фарма Штейн АГ, Швейцарія/Novartis Pharma Stein AG, Switzerland.
Новартіс Фармасьютика С.А., Іспанія/Novartis Farmaceutica S.A., Spain.
Місцезнаходження виробника та його адреса місця провадження діяльності
Шаффхаусерштрассе, 4332 Штейн, Швейцарія/Schaffhauserstrasse, 4332 Stein, Switzerland.
Ронда де Санта Марія 158, 08210 Барбера дель Валлес, Барселона, Іспанія/Ronda de Santa Maria 158, 08210 Barbera del Valles, Barcelona, Spain.
Інші медикаменти цього ж виробника
Форма: капсули м'які по 50 мг in bulk: по 5 капсул у блістері; по 10 блістерів у картонній коробці; по 60 коробок у картонній коробці
Форма: розчин для інфузій, 5 мг/100 мл по 100 мл у флаконі; по 1 флакону в коробці з картону
Форма: мазь очна, по 3,5 г у тубі; по 1 тубі у коробці з картону
Форма: капсули м'які по 25 мг по 5 капсул у блістері; по 10 блістерів у картонній коробці
Форма: таблетки, вкриті плівковою оболонкою, по 50 мг № 14 (7х2) у блістерах