Менопур
Реєстраційний номер: UA/6705/01/02
Імпортер: Феррінг Інтернешнл Сентер СА
Країна: ШвейцаріяАдреса імпортера: Чемін де ла Вергогнаусаз 50, 1162, Сан-Пре, Швейцарія
Форма
порошок ліофілізований для розчину для ін'єкцій по 600 МО ФСГ та 600 МО ЛГ у флаконах № 1 у комплекті з розчинником по 1 мл у попередньо заповнених шприцах № 1
Склад
1 флакон з порошком містить менотропін високоочищений (людський менопаузний гонадотропін високоочищений, лМГ) у кількості, що відповідає 600 МО ФСГ (фолікулостимулюючий гормон) та 600 МО ЛГ (лютеїнізуючий гормон)
Виробники препарату «Менопур»
Країна: Німеччина
Адреса: Вітланд 11, 24109 Кіль, Німеччина
Країна: Швейцарія
Адреса: Чемін де ла Вергогнаусаз 50, 1162, Сан-Пре, Швейцарія
Інструкція по застосуванню
для медичного застосування лікарського засобу
МЕНОПУР
(MENOPUR®)
Склад
Менопур 600 МО:
діюча речовина: менотропін високоочищений;
1 флакон з порошком містить менотропін високоочищений (людський менопаузний гонадотропін високоочищений, лМГ) у кількості, що відповідає 600 МО ФСГ (фолікулостимулюючий гормон) та 600 МО ЛГ (лютеїнізуючий гормон).
Менопур 1200 МО:
діюча речовина: менотропін високоочищений;
1 флакон з порошком містить менотропін високоочищений (людський менопаузний гонадотропін високоочищений, лМГ) у кількості, що відповідає 1200 МО ФСГ (фолікулостимулюючий гормон) та 1200 МО ЛГ (лютеїнізуючий гормон);
допоміжні речовини: лактоза, моногідрат; натрію гідрофосфат, гептагідрат; полісорбат 20;
1 М розчин кислоти фосфорної; 0,5 М розчин натрію гідрофосфату гептагідрату;
1 шприц з розчинником містить: м-крезол, вода для ін'єкцій.
Лікарська форма. Порошок ліофілізований для розчину для ін'єкцій.
Основні фізико-хімічні властивості:
порошок: білий або майже білий ліофілізат у вигляді коржа;
розчинник: прозорий, безбарвний розчин.
Фармакотерапевтична група. Гонадотропіни та інші стимулятори овуляції. Людський менопаузний гонадотропін. Код АТХ G03G A02.
Фармакологічні властивості.
Фармакодинаміка.
У препараті Менопур присутній людський хоріонічний гонадотропін (лХГ) - природний гормон, що міститься у сечі постменопаузних жінок, який переважно забезпечує активність ЛГ.
Менотропін, що має активність ФСГ та ЛГ, індукує фолікулярний ріст і розвиток, а також гонадну секрецію стероїдів у жінок, які не страждають на первинну недостатність яєчників. Спочатку ФСГ запускає відновлення фолікулярного росту на стадії раннього фолікулогенезу, тоді як ЛГ є важливим для оваріального стероїдогенезу та бере участь у фізіологічних процесах, що призводять до розвитку відповідного передовуляторного фолікула. Фолікулярний ріст можна стимулювати ФСГ при повній відсутності ЛГ, але отримані фолікули розвиваються аномально. Крім того, така стимуляція супроводжується низькими рівнями естрадіолу, що призводить до недостатньої лютеїнізації.
Узгоджуючись із дією ЛГ, спрямованою на підвищення стероїдогенезу, в циклах IVF/ICSI з десенсибілізацією, рівні естрадіолу при лікуванні Менопуром є вищими, ніж при застосуванні рекомбінантних препаратів ФСГ. Це слід враховувати, якщо контроль реакції пацієнток проводять шляхом визначення рівнів естрадіолу. Відмінностей у досягнутих рівнях естрадіолу не було встановлено при використанні низькодозових протоколів індукції овуляції у пацієнток з ановуляцією.
Фармакокінетика.
Був досліджений фармакокінетичний профіль ФСГ препарату Менопур. Після 7-денного введення 150 МО Менопуру здоровим жінкам-добровольцям із десенсибілізованим гіпофізом максимальні плазмові концентрації ФСГ (відкориговані відповідно до базових) (середнє ± СО) для підшкірного та внутрішньом'язового введення становили 8,9 ± 3,5 МО/л і 8,9 ± 3,5 МО/л відповідно. Максимальні концентрації ФСГ досягаються протягом 7 годин для обох шляхів введення. Після повторного введення період напіввиведення ФСГ становить 30 ± 11 годин і 27 ± 9 годин для підшкірного та внутрішньом'язового введення відповідно (середнє ± СО). Хоча індивідуальні концентрації ЛГ залежно від часу зростають після введення Менопуру, наявних даних недостатньо для проведення фармакокінетичного аналізу.
Менотропін виводиться, перш за все, нирками.
Фармакокінетика Менопуру у пацієнток з порушенням ниркової або печінкової функції не вивчалася.
Клінічні характеристики
Показання
Лікування безпліддя за наявності таких клінічних показань:
· ановуляція, включаючи синдром полікістозних яєчників (СПКЯ), у жінок, які виявилися нечутливими до лікування кломіфену цитратом;
· контрольована оваріальна гіперстимуляція з метою індукції розвитку множинних фолікулів у рамках проведення допоміжних репродуктивних технологій (ДРТ) (наприклад запліднення in vitro/перенесення ембріона (IVF/ET), трансфер гамети у фаллопієву трубу (GIFT) та внутрішньоцитоплазматичне введення сперми (ICSI);
· стимуляція фолікулярного росту у жінок з гіпогонадотропним гіпогонадизмом.
Протипоказання. Менопур протипоказаний жінкам:
- з гіперчутливістю до діючої речовини або до будь-якої з допоміжних речовин препарату;
- з пухлинами гіпофіза або гіпоталамуса;
- з карциномою яєчників, матки або молочних залоз;
- з гінекологічними кровотечами невстановленої етіології;
- з передчасною менопаузою;
- з кістами яєчників або зі збільшеними яєчниками, що не пов'язано із синдромом полікістозних яєчників (СПКЯ);
- у період вагітності або годування груддю.
Менопур не слід призначати у випадках, коли малоймовірно, що результат лікування буде сприятливим:
- при первинній недостатності яєчників;
- при вроджених вадах розвитку статевих органів, несумісних з вагітністю;
- при фіброїдних пухлинах матки, несумісних з вагітністю.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Медикаментозна взаємодія Менопуру у людини не вивчалася. Навіть за відсутності клінічного досвіду очікується, що одночасне застосування Менопуру та кломіфену цитрату може посилити фолікулярну реакцію. При застосуванні агоністів ГнРГ для десенсибілізації гіпофіза для досягнення належної фолікулярної реакції можуть бути потрібні вищі дози Менопуру.
Особливості застосування. Оскільки Менопур має сильну гонадотропну активність, яка може спричинити побічні ефекти від легкого до середнього ступеня тяжкості, препарат слід застосовувати під контролем лікарів, які спеціалізуються на лікуванні безпліддя та мають досвід такого лікування.
Лікування гонадотропінами потребує ретельного медичного нагляду, а також регулярного моніторингу реакції яєчників, а саме: ультразвукових обстежень, можливо, у поєднанні з визначенням сироваткових рівнів естрадіолу. Реакція на введення менотропіну у пацієнток суттєво відрізняється, причому деякі з них дуже слабко реагують на лікування. Слід застосовувати найнижчу ефективну дозу препарату, що відповідає меті лікування.
Першу ін'єкцію Менопуру слід проводити під безпосереднім наглядом лікаря.
До початку лікування слід підтвердити у подружжя діагноз безпліддя та встановити можливі протипоказання щодо вагітності. Зокрема, пацієнток слід обстежити на наявність гіпотиреозу, недостатності кори надниркових залоз, гіперпролактинемії та пухлин гіпофіза або гіпоталамуса, після чого у разі потреби призначити їм відповідне лікування.
У пацієнток, яким у рамках лікування ановулярного безпліддя або проведення ДРТ проводять стимуляцію фолікулярного росту, можливе збільшення яєчників або їхня гіперстимуляція. Такі випадки можна мінімізувати, суворо дотримуючись рекомендованого дозування та режиму введення препарату, а також здійснюючи ретельний моніторинг терапії.
Точну оцінку фолікулярного розвитку і дозрівання повинен проводити лікар, який має досвід інтерпретації відповідних тестів.
Синдром гіперстимуляції яєчників (СГСЯ).
СГСЯ являє собою клінічне явище, яке відрізняється від неускладненого збільшення яєчників. СГСЯ - це синдром, що проявляється зі зростанням ступеня тяжкості. Ознаки СГСЯ включають збільшення яєчників, високі сироваткові рівні статевих гормонів і збільшення проникності судин, яке може призводити до накопичення рідини у перитонеальній, плевральній та у поодиноких випадках - у перикардіальній порожнинах.
Тяжкі випадки СГСЯ можуть супроводжуватися такими симптомами: абдомінальний біль, абдомінальне розтягнення, надмірне збільшення яєчників, збільшення маси тіла, задишка, олігурія та шлунково-кишкові симптоми, такі як нудота, блювання та діарея. При клінічному обстеженні можуть бути виявлені гіповолемія, згущення крові, порушення балансу електролітів, асцит, гемоперитонеум, плевральний випіт, гідроторакс, гостра дихальна недостатність і тромбоемболія.
Надмірна оваріальна реакція на лікування гонадотропінами рідко призводить до розвитку СГСЯ доти, доки з метою ініціювання овуляції не вводять лХГ. Отже, у разі оваріальної гіперстимуляції не слід вводити лХГ; потрібно порадити пацієнтці утриматися від статевих контактів або використовувати бар'єрні методи контрацепції протягом щонайменше 4 днів. СГСЯ може дуже швидко прогресувати (від 24 годин до декількох днів) та набувати серйозної симптоматики, тому пацієнтка повинна перебувати під медичним контролем протягом щонайменше 2 тижнів після введення лХГ.
Мінімізувати ризик розвитку оваріальної гіперстимуляції та багатоплідної вагітності можна, якщо дотримуватись рекомендованого дозування та режиму введення препарату Менопур, а також ретельно контролювати курс лікування. При проведенні ДРТ ризик розвитку гіперстимуляції можна знизити шляхом аспірації усіх фолікулів перед овуляцією.
СГСЯ може ставати тяжчим і тривалішим у разі настання вагітності. Найчастіше СГСЯ розвивається після завершення гормональної терапії і досягає максимальної частоти приблизно через 7-10 днів після закінчення лікування. Зазвичай СГСЯ минає спонтанно з початком менструації.
У разі тяжкого СГСЯ лікування гонадотропінами слід припинити. Якщо воно все ще триває, пацієнтку необхідно госпіталізувати й розпочати специфічне лікування СГСЯ.
Даний синдром частіше спостерігається у жінок із синдромом полікістозних яєчників.
Багатоплідні вагітності.
У разі багатоплідної вагітності, особливо найвищого порядку, підвищується ризик ускладнень для матері й дитини.
У пацієнток, яким проводять індукцію овуляції із застосуванням гонадотропінів, частота багатоплідних вагітностей вища, ніж у разі природного запліднення. Більшість випадків багатоплідних вагітностей представлена двійнями. Для зменшення ризику багатоплідної вагітності рекомендується проводити ретельний моніторинг оваріальної реакції.
У пацієнток, яким проводять процедури ДРТ, ризик багатоплідних вагітностей головним чином залежить від кількості пересаджених ембріонів, їхньої якості та віку пацієнтки.
До початку лікування пацієнтку слід інформувати про потенційний ризик багатоплідної вагітності.
Переривання вагітності.
Частота випадків переривання вагітності - передчасних пологів і спонтанних абортів - вища у пацієнток, яким стимулюють фолікулярний ріст у рамках проведення процедур ДРТ, ніж у звичайній групі пацієнтів.
Позаматкова вагітність.
У жінок із захворюваннями маткових труб в анамнезі існує ризик позаматкової вагітності незалежно від того, настала вагітність внаслідок спонтанного запліднення чи лікування безпліддя. Повідомлялося, що після проведення IVF частота випадків позаматкової вагітності становить 2 - 5 % порівняно з 1 - 1,5 % випадків для загальної групи пацієнтів.
Новоутворення органів репродуктивної системи.
Повідомлялося про випадки розвитку доброякісних і злоякісних новоутворень яєчників та інших органів репродуктивної системи у жінок, яким для лікування безпліддя застосовували декілька лікарських препаратів. Дотепер не встановлено, чи підвищує лікування із застосуванням гонадотропінів базовий ризик розвитку таких пухлин у безплідних жінок.
Вроджені вади розвитку.
Поширеність вроджених вад розвитку після проведення ДРТ може бути трохи вищою, ніж при спонтанному заплідненні. Вважають, що це є результатом відмінностей характеристик батьків (наприклад вік матері, характеристики сперми) і багатоплідних вагітностей.
Тромбоемболічні ускладнення.
Жінкам із загальновизнаними факторами ризику розвитку тромбоемболічних ускладнень, такими як тромбоемболічна патологія в анамнезі або сімейні випадки цієї патології, тяжкий ступінь ожиріння (індекс маси тіла > 30 кг/м2) або тромбофілія, притаманний підвищений ризик венозної або артеріальної тромбоемболії під час або після завершення лікування із застосуванням гонадотропінів. У таких жінок слід зіставити користь застосування гонадотропінів із можливим ризиком. Проте слід зазначити, що сама вагітність теж є фактором ризику тромбоемболічних ускладнень.
Застосування в період вагітності або годування груддю.
Менопур протипоказаний вагітним жінкам.
Даних щодо застосування менотропіну вагітним жінкам немає або вони обмежені. Дослідження на тваринах щодо дії Менопуру під час вагітності не проводились.
Менопур протипоказаний жінкам, які годують груддю.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Відповідні дослідження не проводилися. Однак малоймовірно, що Менопур може впливати на здатність пацієнток керувати автомобілем або виконувати роботу, що потребує підвищеної уваги та швидкої реакції.
Спосіб застосування та дози.
Лікування із застосуванням Менопуру слід починати під наглядом лікаря, який має досвід лікування безпліддя.
Менопур 600 МО і Менопур 1200 МО призначений для підшкірної ін'єкції після відновлення розчинником, оскільки шприц, що міститься в упаковці, призначений лише для підшкірного введення.
Порошок необхідно розчинити перед застосуванням. Приготовлений розчин призначений для багаторазового застосування і може зберігатися протягом 28 днів.
При розчиненні слід уникати інтенсивного струшування. Розчин не можна використовувати, якщо він непрозорий або містить частинки.
Режими дозування, описані нижче, аналогічні як при підшкірному, так і при внутрішньом'язовому введеннях. Менопур 600 МО і Менопур 1200 МО можна вводити лише підшкірно, оскільки шприц, що міститься в упаковці, призначений лише для підшкірного введення.
Реакція яєчників на введення екзогенних гонадотропінів є індивідуальною. Це призводить до того, що неможливо встановити одну універсальну схему дозування. Отже, дозування препарату слід підбирати індивідуально, згідно з оваріальною відповіддю. Менопур можна застосовувати у вигляді монотерапії або у складі комбінованої терапії сумісно з агоністом або антагоністом гонадотропін-рилізинг-гормону (Гн-РГ). Рекомендовані дози та тривалість лікування залежать від застосовуваного протоколу лікування.
Жінки з ановуляцією (включаючи СПКЯ).
Метою терапії із застосуванням Менопуру є розвиток одного граафова фолікула, з якого після введення людського хоріонічного гонадотропіну (лХГ) вивільняється ооцит.
Терапію із застосуванням Менопуру слід починати протягом перших 7 днів менструального циклу. Рекомендована щоденна початкова доза Менопуру становить від 75 до 150 МО, яку слід підтримувати щонайменше протягом 7 днів. Подальший режим лікування слід підбирати індивідуально, відповідно до реакції яєчників та на підставі результатів клінічного контролю (який включає ультразвукові дослідження, можливо, у поєднанні з визначенням рівнів естрадіолу).
Дозу препарату не слід змінювати частіше ніж через 7 днів. Рекомендоване покрокове збільшення дози становить 37,5 МО, при цьому воно не повинно перевищувати 75 МО. Максимальна добова доза препарату не повинна перевищувати 225 МО. У разі неналежної реакції пацієнтки після 4 тижнів лікування терапевтичний цикл слід припинити і розпочати новий цикл з вищої дози препарату, порівняно з тією, яка застосовувалась у попередньому циклі.
При досягненні оптимальної реакції через 1 день після останньої ін'єкції Менопуру слід зробити разову ін'єкцію лХГ у дозі від 5000 до 10000 МО.
Пацієнтці рекомендується мати статевий контакт у день введення лХГ і наступного дня.
Альтернативно може бути проведене внутрішньоматкове запліднення (IUI). Якщо спостерігається надмірна реакція на застосування Менопуру, курс лікування слід припинити та відмінити введення лХГ (див. розділ «Особливості застосування»). Пацієнтка повинна використовувати бар'єрний метод контрацепції або відмовитися від статевих контактів до початку наступної менструальної кровотечі.
Жінки, у яких проводять контрольовану оваріальну гіперстимуляцію з метою індукції розвитку множинних фолікулів у рамках проведення допоміжних репродуктивних технологій (ДРТ).
Згідно з результатами клінічних випробувань застосування Менопуру, що передбачає десенсибілізацію із застосуванням агоніста ГнРГ, терапію Менопуром слід починати приблизно через 2 тижні після початку лікування агоністом. Протягом щонайменше 5 перших днів лікування рекомендується вводити Менопур у добовій дозі від 150 до 225 МО.
Відповідно до результатів клінічного контролю (що включає ультразвукові дослідження, можливо, у поєднанні з визначенням рівнів естрадіолу), в подальшому дозу слід підбирати індивідуально, відповідно до реакції пацієнтки, при цьому крок збільшення дози не повинен перевищувати 150 МО. Максимальна добова доза препарату не повинна перевищувати 450 МО. У більшості випадків не рекомендується продовжувати лікування більше 20 днів.
При використанні протоколів, які не передбачають десенсибілізації із застосуванням агоністів ГнРГ, терапію із застосуванням Менопуру слід починати на 2-й або 3-й день менструального циклу. Рекомендується використати такі ж дозування і схему введення, що й для протоколів, які передбачають десенсибілізацію із застосуванням агоністів ГнРГ.
При утворенні достатньої кількості фолікулів відповідного розміру для індукції кінцевого дозрівання фолікулів слід зробити разову ін'єкцію лХГ у дозі до 10000 МО.
Пацієнтка повинна перебувати під ретельним медичним спостереженням протягом не менше 2 тижнів після введення лХГ. Якщо спостерігається надмірна реакція на застосування Менопуру, курс лікування слід припинити та відмінити введення лХГ (див. розділ «Особливості застосування»). Пацієнтка повинна використовувати бар'єрний метод контрацепції або відмовитися від статевих контактів до початку наступної менструальної кровотечі.
Приготування розчину Менопур 600 МО та 1200 МО.
Якщо Ваша клініка попросила Вас робити ін'єкції Менопуру самостійно, Вам слід дотримуватися всіх наданих нею інструкцій
Перша ін'єкція Менопуру має бути зроблена під наглядом лікаря або медсестри.
Менопур 600 МО:
Менопур випускається у вигляді порошку у флаконі, перед ін'єкцією його слід розчинити за допомогою одного шприца, наповненого розчинником. Розчинник, який Вам слід застосовувати для розчинення Менопуру, міститься у попередньо наповненому шприці в упаковці.
Менопур 600 МО перед застосуванням слід розчинити за допомогою одного попередньо заповненого шприца з розчинником
Після розчинення порошку за допомогою розчинника цей флакон містить лікарський засіб у кількості, достатній для кількох днів терапії, тож Вам слід переконатися, що Ви набираєте лікарський засіб у кількості, що не перевищує призначену Вашим лікарем.
Ваш лікар призначив Вам дозу Менопуру у МО (одиницях). Для отримання необхідної дози Вам слід використовувати один із 9 наданих шприців для введення, градуйованих у МО (одиницях) ФСГ/ЛГ.
|
|
Для цього слід:
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
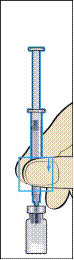
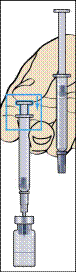
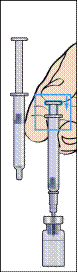
1. Зняти захисний ковпачок з флакона з порошком та гумовий ковпачок із попередньо заповненого шприца з розчинником (рисунок 1).
2. Міцно приєднати голку (голку для відновлення) до попередньо заповненого шприца з розчинником і зняти захисний ковпачок з голки (рисунок 2).
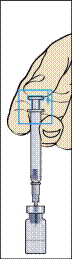
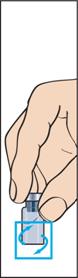
3. Вставити голку вертикально через центр гумової насадки на флаконі з порошком і повільно ввести весь розчинник, уникаючи утворення бульбашок (рисунок 3).
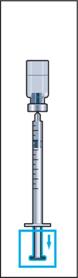
4. Після додавання розчинника у флаконі утворюється незначний надлишковий тиск. Тому слід відпустити поршень шприца, даючи змогу йому піднятися самостійно протягом приблизно 10 секунд. Це допоможе усунути надлишковий тиск у флаконі (рисунок 4).
Вийняти шприц і голку для відновлення.
|
|
|
|
|
|
|
5 |
6 |
7 |
8 |
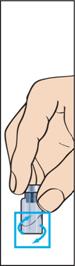
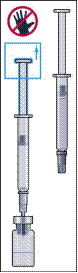
5. Порошок має швидко розчинитися (протягом 2 хвилин), утворивши прозорий розчин. Хоча це зазвичай трапляється при доданні лише кількох крапель розчинника, слід додати розчинник у повному об'ємі. Щоб порошок краще розчинився, слід перемішати розчин, повертаючи флакон (рисунок 5). Не слід збовтувати, оскільки це спричинить утворення повітряних бульбашок.
Флакон із порошком, розчиненим за допомогою одного попередньо заповненого шприца з розчинником, готовий до застосування.
Якщо розчин непрозорий або містить частинки, його не слід використовувати.
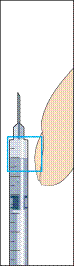
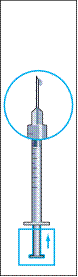
6. Взяти шприц для введення із попередньо приєднаною голкою та вставити голку вертикально в центр флакона. Шприц для введення вже містить незначну кількість повітря, що має бути введене у флакон над рідиною. Перевернути флакон догори дном та набрати призначену дозу Менопуру у шприц для введення ін'єкції (рисунок 6).
ПАМ'ЯТАЙТЕ оскільки цей флакон містить лікарський засіб у кількості, достатній для кількох днів терапії, Вам слід переконатися, що Ви набираєте лікарський засіб у кількості, що не перевищує призначену Вашим лікарем
Якщо Вам призначили Бравель одночасно з Менопуром, Ви можете змішати ці два лікарські засоби, відновивши Менопур і ввівши призначену дозу Менопуру у відновлений розчин препарату Бравель. Наберіть змішаний розчин: Ви можете ввести обидва лікарські засоби разом, замість того, щоб вводити кожен окремо.
7. Вийняти шприц із флакона та набрати невелику кількість повітря у шприц (рисунок 7).
8. Обережно постукати по шприцу для введення, щоб усі повітряні бульбашки зібралися в канюлі (рисунок 8). Обережно виштовхнути все повітря та натискати, поки з голки не вийде перша крапля рідини.
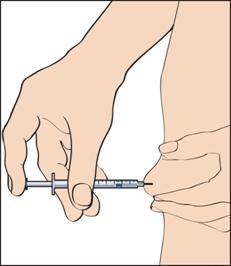
Ваш лікар або медсестра скаже Вам, куди слід робити ін'єкцію (наприклад, передня поверхня стегна, живіт тощо).
Перш ніж робити ін'єкцію, слід продезінфікувати місце ін'єкції за допомогою спиртових серветок, що входять у комплект.
|
|
|
9 |
9. Щоб зробити ін'єкцію, слід защипнути шкіру так, щоб утворилася складка, та ввести голку одним швидким рухом під кутом 90 градусів до тіла. Обережно натиснути на поршень, щоб увести розчин (рисунок 9), після чого вийняти шприц для введення.
Вийнявши шприц для введення, натиснути на місце ін'єкції, щоб зупинити кровотечу. Обережний масаж місця ін'єкції сприятиме розповсюдженню розчину під шкірою.
Не слід викидати використані предмети у побутові відходи; їх слід належним чином утилізувати.
10. Щоб зробити наступну ін'єкцію вже розведеного розчину Менопур, слід повторити кроки 6-9.
Менопур 1200 МО
Менопур випускається у вигляді порошку у флаконі, перед ін'єкцією його слід розчинити за допомогою двох попередньо заповнених шприців з розчинником. Розчинники, які слід застосовувати для розчинення Менопуру, містяться у попередньо заповнених шприцах в упаковці.
Менопур 1200 МО перед застосуванням слід розчинити за допомогою двох попередньо заповнених шприців з розчинником
Після розчинення порошку за допомогою розчинника цей флакон містить лікарський засіб у кількості, достатній для кількох днів терапії, тому Вам слід переконатися, що Ви набираєте лікарський засіб у кількості, що не перевищує призначену Вашим лікарем.
Ваш лікар призначив Вам дозу Менопуру у МО (одиницях). Для отримання необхідної дози Вам слід використовувати один із наданих 18 шприців для введення, градуйованих у МО (одиницях ) ФСГ/ЛГ.
|
|
Для цього слід:
|
|
|
|
|
1 |
2 |
1. Зняти захисний ковпачок з флакона з порошком та гумовий ковпачок з одного із попередньо заповнених шприців з розчинником (рисунок 1).
2. Міцно приєднати голку (голку для відновлення) до попередньо заповненого шприца з розчинником і зняти захисний ковпачок з голки (рисунок 2).
|
|
|
|
|
|
|
|
|
3 |
4 |
5 |
6 |
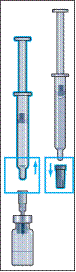
3. Вставити голку вертикально через центр гумової насадки на флаконі з порошком і повільно ввести весь розчинник, уникаючи утворення бульбашок (рисунок 3).
4. Після додання розчинника у флаконі утворюється незначний надлишковий тиск. Тому слід відпустити поршень шприца, даючи змогу йому піднятися самостійно протягом приблизно 10 секунд. Це допоможе усунути надлишковий тиск у флаконі (рисунок 4).
5. Обережно від'єднати шприц від голки, провернувши його, та залишити голку у флаконі.
Зняти захисний ковпачок з другого попередньо заповненого шприца з розчинником і міцно приєднати шприц до голки, зафіксованої у флаконі. Повільно ввести увесь розчинник, уникаючи утворення бульбашок (рисунок 5).
6. Після додавання розчинника у флаконі утворюється незначний надлишковий тиск. Тому слід відпустити поршень шприца, даючи змогу йому піднятися самостійно протягом приблизно 10 секунд. Це допоможе усунути надлишковий тиск у флаконі (рисунок 6).
Вийняти шприц і голку для відновлення.
|
|
|
|
|
|
|
7 |
8 |
9 |
10 |
7. Порошок має швидко розчинитися (протягом 2 хвилин), утворивши прозорий розчин. Хоча це зазвичай трапляється при доданні лише кількох крапель розчинника, слід додати розчинник у повному об'ємі. Щоб порошок краще розчинився, слід перемішати розчин, повертаючи флакон (рисунок 7). Не слід збовтувати, оскільки це спричинить утворення повітряних бульбашок.
Флакон із порошком, розчиненим за допомогою двох попередньо заповнених шприців з розчинником, готовий до застосування.
Якщо розчин непрозорий або містить частинки, його не слід використовувати.
8. Взяти шприц для введення із попередньо приєднаною голкою та вставити голку вертикально в центр флакона. Шприц для введення вже містить незначну кількість повітря, що має бути введене у флакон над рідиною. Перевернути флакон догори дном та набрати призначену дозу препарату Менопур у шприц для введення ін'єкції (рисунок 8).
ПАМ'ЯТАЙТЕ оскільки цей флакон містить лікарський засіб у кількості, достатній для кількох днів терапії, Вам слід переконатися, що Ви набираєте лікарський засіб у кількості, що не перевищує призначену Вашим лікарем
Якщо Вам призначили Бравель одночасно з Менопуром, Ви можете змішати ці два лікарські засоби, відновивши Менопур і ввівши призначену дозу Менопуру у відновлений розчин Бравелю. Наберіть змішаний розчин: Ви можете ввести обидва лікарські засоби разом, замість того, щоб вводити кожен окремо.
9. Вийняти шприц із флакона та набрати невелику кількість повітря у шприц (рисунок 9).
10. Обережно постукати по шприцу для введення, щоб усі повітряні бульбашки зібралися в канюлі (рисунок 10). Обережно виштовхнути все повітря та натискати, поки з голки не вийде перша крапля рідини.
Ваш лікар або медсестра скаже Вам, куди слід робити ін'єкцію (наприклад, передня поверхня стегна, живіт тощо).
Перш ніж робити ін'єкцію, слід продезінфікувати місце ін'єкції за допомогою спиртових серветок, що входять у комплект.
|
|
|
11 |
11. Щоб зробити ін'єкцію, слід защипнути шкіру так, щоб утворилася складка, та ввести голку одним швидким рухом під кутом 90 градусів до тіла. Обережно натиснути на поршень, щоб увести розчин (рисунок 11), після чого вийняти шприц для введення.
Вийнявши шприц для введення, натиснути на місце ін'єкції, щоб зупинити кровотечу. Обережний масаж місця ін'єкції сприятиме розповсюдженню розчину під шкірою.
Не слід викидати використані предмети у звичайний домашній смітник; їх слід належним чином утилізувати.
12. Щоб зробити наступну ін'єкцію вже розведеного розчину Менопур, слід повторити кроки 8-11.
Якщо Ви прийняли Менопур у кількості, більшій, ніж потрібно,
будь ласка, повідомте про це медсестру або лікаря.
Якщо Ви забули прийняти Менопур,
не приймайте подвійну дозу, щоб компенсувати пропущену. Будь ласка, повідомте медсестру або лікаря.
Загальні вказівки
Приготовлений розчин не слід вводити, якщо він містить частинки або є непрозорим.
Будь-який невикористаний протягом встановленого терміну придатності препарат або його відходи слід утилізувати відповідно до місцевих вимог.
Діти.
Препарат не застосовують дітям.
Передозування
Прояви передозування препарату невідомі, хоча можна очікувати розвиток синдрому гіперстимуляції яєчників.
Побічні реакції
У клінічних випробуваннях Менопуру найчастіше повідомлялося про такі побічні реакції: абдомінальний біль, головний біль, реакції та біль у місці введення препарату, частота яких досягала 5 %.
Нижче перелічені основні побічні реакції у жінок, яким застосовували Менопур у клінічних випробуваннях.
Побічні реакції розподілено за частотою таким чином: дуже часті (≥ 1/10), часті (від ≥ 1/100 до < 1/10), нечасті (від ≥ 1/1000 до < 1/100), поодинокі (від ≥ 1/10000 до < 1/1000), рідкісні (< 1/10000), частота невідома.
Порушення з боку органів зору: частота невідома - порушення зоруa.
Порушення з боку шлунково-кишкового тракту: часті - абдомінальний біль, здуття живота, нудота; нечасті - блювання, абдомінальний дискомфорт, діарея.
Загальні порушення і порушення у місці введення: часті - реакції у місці ін'єкціїb; нечасті - слабкість; частота невідома - пірексія, нездужання.
Порушення з боку імунної системи: частота невідома - реакції гіперчутливостіс.
Дослідження: частота невідома - збільшення маси тіла.
Порушення з боку скелетно-м'язової та сполучної тканини: частота невідома - м'язово-скелетний більd.
Порушення з боку нервової системи: часті - головний біль; нечасті - запаморочення.
Порушення з боку статевих органів та молочних залоз: часті - СГСЯe, біль у ділянці тазаf; нечасті - кіста яєчників, скарги на біль в грудяхg; частота невідома - перекрут яєчникаe.
Порушення з боку шкіри та підшкірних тканин: поодинокі - акне, висип; частота невідома - свербіж, кропив'янка.
Порушення з боку серцево-судинної системи: нечасті - припливи; частота невідома - тромбоемболіяe.
a Окремі випадки тимчасового амаврозу, диплопії, мідріазу, скотоми, фотопсії, плаваючі помутніння склистого тіла, помутніння зору і розлади зору були зареєстровані як порушення зору під час постмаркетингового періоду.
b Найбільш часто повідомлялося про реакції в місці ін'єкції, а саме біль у місці ін'єкції.
c Є повідомлення про поодинокі випадки локалізованих або генералізованих алергічних реакцій, включаючи анафілактичні реакції, поряд з відповідною симптоматикою.
d М'язово-скелетний біль включає артралгію, біль у спині, біль у шиї і біль у кінцівках.
e При застосуванні Менопуру в клінічних випробуваннях повідомлялося про розвиток шлунково-кишкових симптомів, пов'язаних з СГСЯ, таких як здуття живота, відчуття дискомфорту, нудота, блювання та діарея. Випадки тяжкого асциту, пов'язаного з СГСЯ і накопичення рідини у тазу, плевриту, задишки, олігурії, тромбоемболічних явищ і перекручення яєчників були представлені як рідкі ускладнення.
f Тазові проблеми включають біль у яєчниках і опущення матки.
g Скарги щодо грудних залоз включають біль у грудях, болючість молочних залоз, дискомфорт, біль у сосках і набухання грудей.
Термін придатності. 3 роки.
Після приготування розчин можна зберігати протягом щонайбільше 28 днів при температурі не вище 25 °С.
Умови зберігання. Зберігати в недоступному для дітей місці. Зберігати в холодильнику
(2-8 °С) в оригінальній упаковці. Не заморожувати.
Несумісність. Приготовлений розчин препарату Менопур не слід змішувати з іншими лікарськими засобами, за винятком препарату урофолітропіну Бравель (ФСГ) виробництва компанії Феррінг. Дослідження продемонстрували, що сумісне введення препаратів Бравель і Менопур істотно не впливає на очікувану біодоступність кожного з них.
Упаковка.
Менопур 600 МО.
1 флакон з порошком у комплекті з 1 попередньо заповненим шприцом з розчинником по 1 мл, 1 голкою для розведення, 9 шприцами для введення та 9 спиртовими серветками в картонній упаковці.
Менопур 1200 МО.
1 флакон з порошком у комплекті з 2 попередньо заповненими шприцами з розчинником по 1 мл, 1 голкою для розведення, 18 шприцами для введення та 18 спиртовими серветками в картонній упаковці.
Категорія відпуску. За рецептом.
Виробник.
Феррінг ГмбХ, Німеччина/Ferring GmbH, Germany.
Місцезнаходження виробника та його адреса місця провадження діяльності
Вітланд 11, 24109 Кіль, Німеччина/Wittland 11, 24109 Kiel, Germany.
ИНСТРУКЦИЯ
по медицинскому применению лекарственного средства
МЕНОПУР
(MENOPUR®)
Состав
Менопур 600 МЕ:
действующее вещество: менотропин высокоочищенный;
1 флакон с порошком содержит менотропин высокоочищенный (человеческий менопаузный гонадотропин высокоочищенный, чМГ) в количестве, соответствующем 600 МЕ ФСГ (фолликулостимулирующий гормон) и 600 МЕ ЛГ (лютеинизирующий гормон).
Менопур 1200 МЕ:
действующее вещество: менотропин высокоочищенный;
1 флакон с порошком содержит менотропин высокоочищенный (человеческий менопаузный гонадотропин высокоочищенный, чМГ) в количестве, соответствующем 1200 МЕ ФСГ (фолликулостимулирующий гормон) и 1200 МЕ ЛГ (лютеинизирующий гормон).
вспомогательные вещества: лактоза, моногидрат; натрия гидрофосфат, гептагидрат; полисорбат 20; 1 М раствор кислоты фосфорной; 0,5 М раствор натрия гидрофосфата гептагидрата;
1 шприц с растворителем содержит м-крезол, вода для инъекций.
Лекарственная форма. Порошок лиофилизированный для раствора для инъекций.
Основные физико-химические свойства:
порошок: белый или почти белый лиофилизат в виде коржа;
растворитель: прозрачный, бесцветный раствор.
Фармакологическая группа. Гонадотропины и другие стимуляторы овуляции. Человеческий менопаузный гонадотропин. Код АТХ G03G A02.
Фармакологические свойства.
Фармакодинамика.
В препарате Менопур присутствует человеческий хорионический гонадотропин (чХГ) - природный гормон, содержащийся в моче постменопаузных женщин, который преимущественно обеспечивает активность ЛГ.
Менотропин, имеющий активность ФСГ и ЛГ, индуцирует фолликулярный рост и развитие, а также гонадную секрецию стероидов у женщин, не страдающих первичной недостаточностью яичников. Сначала ФСГ запускает восстановление фолликулярного роста на стадии раннего фолликулогенеза, тогда как ЛГ важен для овариального стероидогенеза и участвует в физиологических процессах, приводящих к развитию соответствующего предовуляторного фолликула. Фолликулярный рост можно стимулировать ФСГ при полном отсутствии ЛГ, но полученные фолликулы развиваются аномально. Кроме того, такая стимуляция сопровождается низкими уровнями эстрадиола, что приводит к недостаточной лютеинизации.
В соответствии с действием ЛГ, направленным на повышение стероидогенеза, в циклах IVF/ICSI с десенсибилизацией, уровни эстрадиола при лечении Менопуром выше, чем при применении рекомбинантных препаратов ФСГ. Это следует учитывать, если контроль реакции пациенток проводят путем определения уровней эстрадиола. Различий в достигнутых уровнях эстрадиола не было установлено при использовании низкодозовых протоколов индукции овуляции у пациенток с ановуляцией.
Фармакокинетика.
Был исследован фармакокинетический профиль ФСГ препарата Менопур. После 7-дневного введения 150 МЕ Менопура здоровым женщинам-добровольцам с десенсибилизированным гипофизом максимальные плазменные концентрации ФСГ (откорректированы в соответствии с базовыми) (среднее ± СО) для подкожного и внутримышечного введения составляли 8,9 ± 3,5 МЕ/л и 8,9 ± 3,5 МЕ/л соответственно. Максимальные концентрации ФСГ достигаются в течение 7 часов для обоих путей введения. После повторного введения период полувыведения ФСГ составляет 30 ± 11 часов и 27 ± 9 часов для подкожного и внутримышечного введения соответственно (среднее ± СО). Хотя индивидуальные концентрации ЛГ в зависимости от времени растут после введения Менопура, имеющихся данных недостаточно для проведения фармакокинетического анализа.
Менотропин выводится, прежде всего, почками.
Фармакокинетика Менопура у пациенток с нарушением почечной или печеночной функции не изучалась.
Клинические характеристики
Показания
Лечение бесплодия при следующих клинических показаниях:
• ановуляция, включая синдром поликистозных яичников (СПКЯ), у женщин, которые оказались нечувствительными к лечению кломифена цитратом;
• контролируемая овариальная гиперстимуляция с целью индукции развития множественных фолликулов в рамках проведения вспомогательных репродуктивных технологий (ВРТ) (например оплодотворения in vitro/перенос эмбриона (IVF/ET), трансфер гаметы в фаллопиевую трубу (GIFT) и внутрицитоплазматическое введение спермы (ICSI);
• стимуляция фолликулярного роста у женщин с гипогонадотропным гипогонадизмом.
Противопоказания. Менопур противопоказан женщинам:
- с гиперчувствительностью к действующему веществу или к любому из вспомогательных веществ препарата;
- с опухолями гипофиза или гипоталамуса;
- с карциномой яичников, матки или молочных желез;
- с гинекологическими кровотечениями неустановленной этиологии;
- с преждевременной менопаузой;
- с кистами яичников или с увеличенными яичниками, что не связано с синдромом поликистозных яичников (СПКЯ);
- в период беременности и кормления грудью.
Менопур не следует назначать в случаях, когда маловероятно, что результат лечения будет благоприятным:
- при первичной недостаточности яичников;
- при врожденных пороках развития половых органов, несовместимых с беременностью;
- при фиброидных опухолях матки, несовместимых с беременностью.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий.
Медикаментозное взаимодействие Менопура у человека не изучалось. Даже при отсутствии клинического опыта ожидается, что одновременное применение Менопура и кломифена цитрата может усилить фолликулярную реакцию. При применении агонистов ГнРГ для десенсибилизации гипофиза для достижения надлежащей фолликулярной реакции могут потребоваться более высокие дозы Менопура.
Особенности применения. Поскольку Менопур имеет сильную гонадотропную активность, которая может повлечь побочные эффекты от легкой до средней степени тяжести, препарат следует применять под контролем врачей, специализирующихся на лечении бесплодия и имеющих опыт такого лечения.
Лечение гонадотропинами требует тщательного медицинского наблюдения, а также регулярного мониторинга реакции яичников, а именно: ультразвуковых обследований, возможно, в сочетании с определением сывороточных уровней эстрадиола. Реакция на введение менотропина у пациенток существенно отличается, причем некоторые из них очень слабо реагируют на лечение. Следует применять самую низкую эффективную дозу препарата, которая соответствует цели лечения.
Первую инъекцию Менопура следует проводить под непосредственным наблюдением врача.
До начала лечения следует подтвердить у супругов диагноз бесплодия и установить возможные противопоказания к беременности. В частности, пациенток необходимо обследовать на наличие гипотиреоза, недостаточности коры надпочечников, гиперпролактинемии и опухолей гипофиза или гипоталамуса, после чего в случае необходимости назначить им соответствующее лечение.
У пациенток, которым в рамках лечения ановулярного бесплодия или проведения ВРТ проводят стимуляцию фолликулярного роста, возможно увеличение яичников или их гиперстимуляция. Такие случаи можно минимизировать, если строго придерживаться рекомендуемых доз и режима введения препарата, а также осуществлять тщательный мониторинг терапии.
Точную оценку фолликулярного развития и созревания должен проводить врач, имеющий опыт интерпретации соответствующих тестов.
Синдром гиперстимуляции яичников (СГСЯ).
СГСЯ представляет собой клиническое явление, которое отличается от неосложненного увеличения яичников. СГСЯ - это синдром, который проявляется с увеличением степени тяжести. Признаки СГСЯ включают увеличение яичников, высокие сывороточные уровни половых гормонов и увеличение проницаемости сосудов, что может приводить к накоплению жидкости в перитонеальной, плевральной и в редких случаях - в перикардиальной полостях.
Тяжелые случаи СГСЯ могут сопровождаться следующими симптомами: абдоминальная боль, абдоминальное растяжение, чрезмерное увеличение яичников, увеличение массы тела, одышка, олигурия и желудочно-кишечные симптомы, такие как тошнота, рвота и диарея. При клиническом обследовании могут быть выявлены гиповолемия, сгущение крови, нарушение баланса электролитов, асцит, гемоперитонеум, плевральный выпот, гидроторакс, острая дыхательная недостаточность и тромбоэмболия.
Чрезмерная овариальная реакция на лечение гонадотропинами редко приводит к развитию СГСЯ до тех пор, пока с целью инициирования овуляции не вводят чХГ. Поэтому в случае овариальной гиперстимуляции не следует вводить чХГ; нужно посоветовать пациентке воздержаться от половых контактов или использовать барьерные методы контрацепции в течение не менее 4 дней. СГСЯ может очень быстро прогрессировать (от 24 часов до нескольких дней) и приобретать серьезную симптоматику, поэтому пациентка должна находиться под медицинским контролем на протяжении не менее 2 недель после введения чХГ.
Минимизировать риск развития овариальной гиперстимуляции и многоплодной беременности можно, если придерживаться рекомендованной дозировки и режима введения препарата Менопур, а также тщательно контролировать курс лечения. При проведении ВРТ риск развития гиперстимуляции можно снизить путем аспирации всех фолликулов перед овуляцией.
СГСЯ может становиться более тяжелым и длительным при наступлении беременности. Чаще всего СГСЯ развивается после завершения гормональной терапии и достигает максимальной частоты примерно через 7-10 дней после окончания лечения. Обычно СГСЯ проходит спонтанно с началом менструации.
В случае тяжелого СГСЯ лечение гонадотропинами следует прекратить. Если оно все еще продолжается, пациентку необходимо госпитализировать и начать специфическое лечение СГСЯ.
Данный синдром чаще наблюдается у женщин с синдромом поликистозных яичников.
Многоплодные беременности.
В случае многоплодной беременности, особенно высшего порядка, повышается риск осложнений для матери и ребенка.
У пациенток, которым проводят индукцию овуляции с применением гонадотропинов, частота многоплодных беременностей выше, чем при естественном оплодотворении. Большинство случаев многоплодных беременностей представлено двойнями. Для уменьшения риска многоплодной беременности рекомендуется тщательный мониторинг овариальной реакции.
У пациенток, которым проводят процедуры ВРТ, риск многоплодной беременности главным образом зависит от количества пересаженных эмбрионов, их качества и возраста пациентки.
До начала лечения пациентку следует информировать о потенциальном риске многоплодной беременности.
Прерывание беременности.
Частота случаев прерывания беременности - преждевременных родов и спонтанных абортов - выше у пациенток, которым стимулируют фолликулярный рост в рамках проведения процедур ВРТ, чем в обычной группе пациентов.
Внематочная беременность.
У женщин с заболеваниями маточных труб в анамнезе существует риск внематочной беременности независимо от того, наступила беременность вследствие спонтанного оплодотворения или лечения бесплодия. Сообщалось, что после проведения IVF частота случаев внематочной беременности составляет 2 - 5% по сравнению с 1 - 1,5% случаев для общей группы пациентов.
Новообразования органов репродуктивной системы.
Сообщалось о случаях развития доброкачественных и злокачественных новообразований яичников и других органов репродуктивной системы у женщин, которым для лечения бесплодия применяли несколько лекарственных препаратов. До настоящего времени не установлено, повышает ли лечение с применением гонадотропинов базовый риск развития таких опухолей у бесплодных женщин.
Врожденные пороки развития.
Распространенность врожденных пороков развития после проведения ВРТ может быть немного выше, чем при спонтанном оплодотворении. Считают, что это является результатом различий характеристик родителей (например, возраст матери, характеристики спермы) и многоплодных беременностей.
Тромбоэмболические осложнения.
У женщин с общепризнанными факторами риска развития тромбоэмболических осложнений, такими как тромбоэмболическая патология в анамнезе или семейные случаи этой патологии, тяжелая степень ожирения (индекс массы тела >30 кг/м2) или тромбофилия, повышен риск венозной или артериальной тромбоэмболии во время или после завершения лечения с применением гонадотропинов. У таких женщин следует сопоставить пользу применения гонадотропинов с возможным риском. Однако следует отметить, что сама беременность тоже является фактором риска тромбоэмболических осложнений.
Применение в период беременности или кормления грудью.
Менопур противопоказан беременным женщинам.
Данных о применении менотропина беременным женщинам нет или они ограничены. Исследования на животных относительно действия Менопура во время беременности не проводились.
Менопур противопоказан женщинам, кормящим грудью.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Соответствующие исследования не проводились. Однако маловероятно, что Менопур может влиять на способность пациенток управлять автомобилем или выполнять работу, требующую повышенного внимания и быстрой реакции.
Способ применения и дозы.
Лечение с применением Менопура следует начинать под наблюдением врача, имеющего опыт лечения бесплодия.
Менопур 600 МЕ и Менопур 1200 МЕ предназначены для подкожной инъекции после восстановления растворителем, поскольку шприц, который содержится в упаковке, предназначен только для подкожного введения.
Порошок необходимо растворить перед применением. Приготовленный раствор предназначен для многократного применения и может храниться в течение 28 дней.
При растворении следует избегать интенсивного встряхивания. Раствор нельзя использовать, если он непрозрачный или содержит частицы.
Режимы дозирования, описанные ниже, аналогичны как при подкожном, так и при внутримышечном введении. Менопур 600 МЕ и Менопур 1200 МЕ можно вводить только подкожно, поскольку шприц, который содержится в упаковке, предназначен только для подкожного введения.
Реакция яичников на введение экзогенных гонадотропинов является индивидуальной. Это приводит к тому, что невозможно установить одну универсальную схему дозирования. Поэтому дозировку препарата следует подбирать индивидуально, согласно овариальному ответу. Менопур можно применять в виде монотерапии или в составе комбинированной терапии совместно с агонистом или антагонистом гонадотропин-рилизинг-гормона (Гн-РГ). Рекомендуемые дозы и длительность лечения зависят от применяемого протокола лечения.
Женщины с ановуляцией (включая СПКЯ).
Целью терапии с применением Менопура является развитие одного граафова фолликула, из которого после введения человеческого хорионического гонадотропина (чХГ) высвобождается ооцит.
Терапию с применением Менопура следует начинать в течение первых 7 дней менструального цикла. Рекомендуемая ежедневная начальная доза Менопура составляет от 75 до 150 МЕ, которую следует поддерживать в течение не менее 7 дней. Дальнейший режим лечения следует подбирать индивидуально, в соответствии с реакцией яичников и на основании результатов клинического контроля (который включает ультразвуковые исследования, возможно, в сочетании с определением уровня эстрадиола).
Дозу препарата не следует менять чаще, чем через 7 дней. Рекомендуемое пошаговое увеличение дозы составляет 37,5 МЕ, при этом оно не должно превышать 75 МЕ. Максимальная суточная доза не должна превышать 225 МЕ. В случае ненадлежащей реакции пациентки после 4 недель лечения терапевтический цикл следует прекратить и начать новый цикл с более высокой дозы препарата по сравнению с той, которая применялась в предыдущем цикле.
При достижении оптимальной реакции через 1 день после последней инъекции Менопура следует сделать разовую инъекцию чХГ в дозе от 5000 до 10000 МЕ.
Пациентке рекомендуется иметь половой контакт в день введения чХГ и на следующий день.
Альтернативно может быть проведено внутриматочное оплодотворение (IUI). При чрезмерной реакции на применение Менопура курс лечения следует прекратить и отменить введение чХГ (см. раздел «Особенности применения»). Пациентка должна использовать барьерный метод контрацепции или отказаться от половых контактов до начала следующего менструального кровотечения.
Женщины, у которых проводят контролируемую овариальную гиперстимуляцию с целью индукции развития множественных фолликулов в рамках проведения вспомогательных репродуктивных технологий (ВРТ).
Согласно результатам клинических испытаний применения Менопура, предусматривающих десенсибилизацию с применением агониста ГнРГ, терапию Менопуром следует начинать приблизительно через 2 недели после начала лечения агонистом. На протяжении не менее 5 первых дней лечения рекомендуется вводить Менопур в суточной дозе от 150 до 225 МЕ.
Согласно результатам клинического контроля (который включает ультразвуковые исследования, возможно, в сочетании с определением уровней эстрадиола), в дальнейшем дозу следует подбирать индивидуально, в соответствии с реакцией пациентки, при этом шаг увеличения дозы не должен превышать 150 МЕ. Максимальная суточная доза не должна превышать 450 МЕ. В большинстве случаев не рекомендуется продолжать лечение более 20 дней.
При использовании протоколов, которые не предусматривают десенсибилизации с применением агонистов ГнРГ, терапию с применением Менопура следует начинать на 2-й или 3-й день менструального цикла. Рекомендуется использовать такие же дозы и схему введения, что и для протоколов, предусматривающих десенсибилизацию с применением агонистов ГнРГ.
При образовании достаточного количества фолликулов соответствующего размера для индукции конечного созревания фолликулов следует сделать разовую инъекцию чХГ в дозе до 10000 МЕ.
Пациентка должна находиться под тщательным медицинским наблюдением в течение не менее 2 недель после введения чХГ. При чрезмерной реакции на применение Менопура курс лечения следует прекратить и отменить введение чХГ (см. раздел «Особенности применения»). Пациентка должна использовать барьерный метод контрацепции или отказаться от половых контактов до начала следующего менструального кровотечения.
Приготовление раствора Менопур 600 МЕ и 1200 МЕ.
Если Ваша клиника попросила Вас делать инъекции Менопура самостоятельно, Вам следует соблюдать все предоставленные ею инструкции
Первая инъекция Менопура должна быть сделана под наблюдением врача или медсестры.
Менопур 600 МЕ:
Менопур выпускается в виде порошка во флаконе, перед инъекцией его следует растворить с помощью одного шприца, наполненного растворителем. Растворитель, который Вам следует применять для растворения Менопура, содержится в предварительно заполненном шприце в упаковке.
Менопур 600 МЕ перед применением следует растворить с помощью одного предварительно заполненного шприца с растворителем
После растворения порошка с помощью растворителя этот флакон содержит лекарственное средство в количестве, достаточном для нескольких дней терапии, поэтому Вам следует убедиться, что Вы набираете лекарственное средство в количестве, не превышающем назначенного Вашим врачом.
Ваш врач назначил Вам дозу Менопура в МЕ (единицах). Для получения необходимой дозы Вам следует использовать один из 9 предоставленных шприцев для введения, градуированных в МЕ (единицах) ФСГ/ЛГ.

Для этого следует:
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
1. Снять защитный колпачок с флакона с порошком и резиновый колпачок с предварительно заполненного шприца с растворителем (рисунок 1).
2. Крепко присоединить иглу (иглу для восстановления) к предварительно заполненному шприцу с растворителем и снять защитный колпачок с иглы (рисунок 2).
3. Вставить иглу вертикально через центр резиновой насадки на флаконе с порошком и медленно ввести весь растворитель, избегая образования пузырьков (рисунок 3).
4. После добавления растворителя во флаконе образуется незначительное избыточное давление. Поэтому следует отпустить поршень шприца, позволяя ему подняться самостоятельно в течение примерно 10 секунд. Это поможет устранить избыточное давление во флаконе (рисунок 4).
Вынуть шприц и иглу для восстановления.
|
|
|
|
|
|
|
5 |
6 |
7 |
8 |
5. Порошок должен быстро раствориться (в течение 2 минут), образовав прозрачный раствор. Хотя это обычно случается при добавлении лишь нескольких капель растворителя, следует добавить растворитель в полном объеме. Чтобы порошок лучше растворился, следует перемешать раствор, поворачивая флакон (рисунок 5). Не следует взбалтывать, так как это приведет к образованию воздушных пузырьков.
Флакон с порошком, растворенным с помощью одного предварительно заполненного шприца с растворителем, готов к применению.
Если раствор непрозрачный или содержит частицы, его не следует использовать.
6. Взять шприц для введения с предварительно присоединенной иглой и вставить иглу вертикально в центр флакона. Шприц для введения уже содержит незначительное количество воздуха, которое должно быть введено во флакон над жидкостью. Перевернуть флакон вверх дном и набрать назначенную дозу Менопура в шприц для введения инъекции (рисунок 6).
ПОМНИТЕ поскольку этот флакон содержит лекарственное средство в количестве, достаточном для нескольких дней терапии, Вам следует убедиться, что Вы набираете лекарственное средство в количестве, не превышающем назначенного Вашим врачом
Если Вам назначили Бравель одновременно с Менопуром, Вы можете смешать эти два лекарственных средства, восстановив Менопур и введя назначенную дозу Менопура в восстановленный раствор препарата Бравель. Наберите смешанный раствор: Вы можете ввести оба лекарственных средства вместе, вместо того, чтобы вводить по отдельности.
7. Вынуть шприц из флакона и набрать небольшое количество воздуха в шприц (рисунок 7).
8. Осторожно постучать по шприцу для введения, чтобы все воздушные пузырьки собрались в канюле (рисунок 8). Осторожно вытолкнуть весь воздух и нажимать до тех пор, пока с иглы не выйдет первая капля жидкости.
Ваш врач или медсестра скажет Вам, куда следует делать инъекцию (например, передняя поверхность бедра, живот и т.д.).
Прежде чем делать инъекцию, следует продезинфицировать место инъекции с помощью спиртовых салфеток, входящих в комплект.
|
|
|
9 |
9. Чтобы сделать инъекцию, следует защипнуть кожу так, чтобы образовалась складка, и ввести иглу одним быстрым движением под углом 90 градусов к телу. Осторожно нажать на поршень, чтобы ввести раствор (рисунок 9), после чего вынуть шприц для введения.
Вынув шприц для введения, нажать на место инъекции, чтобы остановить кровотечение. Осторожный массаж места инъекции будет способствовать распространению раствора под кожей.
Не следует выбрасывать использованные предметы в бытовые отходы; их следует должным образом утилизировать.
10. Чтобы сделать следующую инъекцию уже разбавленного раствора Менопур, необходимо повторить шаги 6-9.
Менопур 1200 МЕ
Менопур выпускается в виде порошка во флаконе, перед инъекцией его следует растворить с помощью двух предварительно заполненных шприцев с растворителем. Растворители, которые следует применять для растворения Менопура, содержатся в предварительно заполненных шприцах в упаковке.
Менопур 1200 МЕ перед применением следует растворить с помощью двух предварительно заполненных шприцев с растворителем
После растворения порошка с помощью растворителя этот флакон содержит лекарственное средство в количестве, достаточном для нескольких дней терапии, поэтому Вам следует убедиться, что Вы набираете лекарственное средство в количестве, не превышающем назначенного врачом.
Ваш врач назначил Вам дозу Менопура в МЕ (единицах). Для получения необходимой дозы Вам следует использовать один из предоставленных 18 шприцев для введения, градуированных в МЕ (единицах) ФСГ/ЛГ.
|
|
Для этого следует:
|
|
|
|
|
1 |
2 |
1. Снять защитный колпачок с флакона с порошком и резиновый колпачок с одного из предварительно заполненных шприцев с растворителем (рисунок 1).
2. Крепко присоединить иглу (иглу для восстановления) к предварительно заполненному шприцу с растворителем и снять защитный колпачок с иглы (рисунок 2).
|
|
|
|
|
|
|
|
|
3 |
4 |
5 |
6 |
3. Вставить иглу вертикально через центр резиновой насадки на флаконе с порошком и медленно ввести весь растворитель, избегая образования пузырьков (рисунок 3).
4. После добавления растворителя во флаконе образуется незначительное избыточное давление. Поэтому следует отпустить поршень шприца, позволяя ему подняться самостоятельно в течение примерно 10 секунд. Это поможет устранить избыточное давление во флаконе (рисунок 4).
5. Осторожно отсоединить шприц от иглы, провернув его, и оставить иглу во флаконе.
Снять защитный колпачок с другого предварительно заполненного шприца с растворителем и крепко присоединить шприц к игле, зафиксированной во флаконе. Медленно ввести весь растворитель, избегая образования пузырьков (рисунок 5).
6. После добавления растворителя во флаконе образуется незначительное избыточное давление. Поэтому следует отпустить поршень шприца, позволяя ему подняться самостоятельно в течение примерно 10 секунд. Это поможет устранить избыточное давление во флаконе (рисунок 6).
Вынуть шприц и иглу для восстановления.
|
|
|
|
|
|
|
7 |
8 |
9 |
10 |
7. Порошок должен быстро раствориться (в течение 2 минут), образовав прозрачный раствор. Хотя это обычно случается при добавлении лишь нескольких капель растворителя, следует добавить растворитель в полном объеме. Чтобы порошок лучше растворился, следует перемешать раствор, поворачивая флакон (рисунок 7). Не следует взбалтывать, так как это приведет к образованию воздушных пузырьков.
Флакон с порошком, растворенным с помощью двух предварительно заполненных шприцев с растворителем, готов к применению.
Если раствор непрозрачный или содержит частицы, его не следует использовать.
8. Взять шприц для введения с предварительно присоединенной иглой и вставить иглу вертикально в центр флакона. Шприц для введения уже содержит незначительное количество воздуха, которое должно быть введено во флакон над жидкостью. Перевернуть флакон вверх дном и набрать назначенную дозу препарата Менопур в шприц для введения инъекции (рисунок 8).
ПОМНИТЕ поскольку этот флакон содержит лекарственное средство в количестве, достаточном для нескольких дней терапии, Вам следует убедиться, что Вы набираете лекарственное средство в количестве, не превышающем назначенного врачом
Если Вам назначили Бравель одновременно с Менопуром, Вы можете смешать эти два лекарственных средства, восстановив Менопур и введя назначенную дозу Менопура в восстановленный раствор Бравеля. Наберите смешанный раствор: Вы можете ввести оба лекарственных средства вместе, вместо того, чтобы вводить по отдельности.
9. Вынуть шприц из флакона и набрать небольшое количество воздуха в шприц (рисунок 9).
10. Осторожно постучать по шприцу для введения, чтобы все воздушные пузырьки собрались в канюле (рисунок 10). Осторожно вытолкнуть весь воздух и нажимать до тех пор, пока с иглы не выйдет первая капля жидкости.
Ваш врач или медсестра скажет Вам, куда следует делать инъекцию (например, передняя поверхность бедра, живот и т.д.).
Прежде чем делать инъекцию, следует продезинфицировать место инъекции с помощью спиртовых салфеток, входящих в комплект.
|
|
|
11 |
11. Чтобы сделать инъекцию, следует защипнуть кожу так, чтобы образовалась складка, и ввести иглу одним быстрым движением под углом 90 градусов к телу. Осторожно нажать на поршень, чтобы ввести раствор (рисунок 11), после чего вынуть шприц для введения.
Вынув шприц для введения, нажать на место инъекции, чтобы остановить кровотечение. Осторожный массаж места инъекции будет способствовать распространению раствора под кожей.
Не следует выбрасывать использованные предметы в бытовые отходы; их следует должным образом утилизировать.
12. Чтобы сделать следующую инъекцию уже разбавленного раствора Менопур, необходимо повторить шаги 8-11.
Если Вы приняли Менопур в количестве, большем, чем нужно,
пожалуйста, сообщите об этом медсестре или врачу.
Если Вы забыли принять Менопур,
не принимайте двойную дозу, чтобы компенсировать пропущенную. Пожалуйста, сообщите медсестре или врачу.
Общие указания
Приготовленный раствор не следует вводить, если он содержит частицы или является непрозрачным.
Любой неиспользованный в течение установленного срока годности препарат или его отходы следует утилизировать в соответствии с местными требованиями.
Дети.
Препарат не применяют детям.
Передозировка
Проявления передозировки препарата неизвестны, хотя можно ожидать развития синдрома гиперстимуляции яичников.
Побочные реакции
В клинических испытаниях Менопура чаще всего сообщалось о следующих побочных реакциях: абдоминальная боль, головная боль, реакции и боль в месте введения препарата, частота которых достигала 5%.
Ниже перечислены основные побочные реакции у женщин, которым применяли Менопур в клинических испытаниях.
Побочные реакции распределены по частоте следующим образом: очень частые (≥ 1/10), частые (≥ 1/100 до <1/10), нечастые (от ≥ 1/1000 до <1/100), редкие (от ≥ 1/10000 до <1/1000), очень редкие (<1/10000), частота неизвестна.
Нарушения со стороны органов зрения: частота неизвестна - нарушение зренияa.
Нарушения со стороны желудочно-кишечного тракта: частые - абдоминальная боль, вздутие живота, тошнота; нечастые - рвота, абдоминальный дискомфорт, диарея.
Общие нарушения и нарушения в месте введения: частые - реакции в месте инъекцииb; нечастые - слабость, частота неизвестна - пирексия, недомогание.
Нарушения со стороны иммунной системы: частота неизвестна - реакции гиперчувствительностис.
Исследования: частота неизвестна - увеличение массы тела.
Нарушения со стороны костно-мышечной и соединительной ткани: частота неизвестна -скелетно-мышечная больd.
Нарушения со стороны нервной системы: частые - головная боль; нечастые - головокружение.
Нарушения со стороны половых органов и молочных желез: частые - СГСЯe, боль в области тазаf; нечастые - киста яичников, жалобы на боль в грудиg; частота неизвестна - перекрут яичникаe.
Нарушения со стороны кожи и подкожных тканей: редкие - акне, сыпь; частота неизвестна - зуд, крапивница.
Нарушения со стороны сердечно-сосудистой системы: нечастые - приливы; частота неизвестна - тромбоэмболияe.
aОтдельные случаи временного амавроза, диплопии, мидриаза, скотомы, фотопсии, плавающие помутнения стекловидного тела, помутнения зрения и расстройства зрения были зарегистрированы как нарушения зрения в постмаркетинговый период.
bНаиболее часто сообщалось о реакции в месте инъекции, а именно о боли в месте инъекции.
cИмеются сообщения о единичных случаях локализованных или генерализованных аллергических реакций, включая анафилактические реакции, наряду с соответствующей симптоматикой.
dМышечно-скелетная боль включает артралгию, боль в спине, боль в шее и боль в конечностях.
eПри применении Менопура в клинических испытаниях сообщалось о развитии желудочно-кишечных симптомов, связанных с СГСЯ, таких как вздутие живота, ощущение дискомфорта, тошнота, рвота и диарея. Случаи тяжелого асцита, связанного с СГСЯ, и накопления жидкости в тазу, плеврита, одышки, олигурии, тромбоэмболических явлений и перекрута яичников были представлены как редкие осложнения.
fТазовые проблемы включают боль в яичниках и опущение матки.
gЖалобы относительно грудных желез включают боль в груди, болезненность молочных желез, дискомфорт, боль в сосках и набухание груди.
Срок годности. 3 года.
После приготовления раствор можно хранить в течение максимум 28 дней при температуре не выше 25 °С.
Условия хранения. Хранить в недоступном для детей месте. Хранить в холодильнике
(2-8 °С) в оригинальной упаковке. Не замораживать.
Несовместимость. Приготовленный раствор препарата Менопур не следует смешивать с другими лекарственными средствами, за исключением препарата урофоллитропина Бравель (ФСГ) производства компании Ферринг. Исследования показали, что совместное введение препаратов Бравель и Менопур существенно не влияет на ожидаемую биодоступность каждого из них.
Упаковка.
Менопур 600 МЕ.
1 флакон с порошком в комплекте с 1 предварительно заполненным шприцом с растворителем по 1 мл, 1 иглой для разведения, 9 шприцами для введения и 9 спиртовыми салфетками в картонной упаковке.
Менопур 1200 МЕ.
1 флакон с порошком в комплекте с 2 предварительно заполненными шприцами с растворителем по 1 мл, 1 иглой для разведения, 18 шприцами для введения и 18 спиртовыми салфетками в картонной упаковке.
Категория отпуска. По рецепту.
Производитель.
Ферринг ГмбХ, Германия / Ferring GmbH, Germany.
Местонахождение производителя и его адрес места осуществления деятельности
Витланд 11, 24109 Киль, Германия / Wittland 11, 24109 Kiel, Germany.
Інші медикаменти цього ж виробника
Форма: ліофілізат оральний по 120 мкг, по 10 ліофілізатів у блістері; по 1, або по 3 або по 10 блістерів у картонній коробці
Форма: супозиторії ректальні по 1000 мг № 28 (7х4) у блістерах
Форма: розчин для ін'єкцій, 15 мкг/мл; по 1 мл в ампулі; по 10 ампул у картонній упаковці
Форма: таблетки пролонгованної дії по 500 мг по 10 таблеток у блістері; по 5 або 10 блістерів у картонній коробці
Форма: порошок для розчину для ін'єкцій по 80 мг, 1 флакон з порошком у комплекті з 1 попередньо наповненим шприцом з розчинником (вода для ін'єкцій) по 5 мл (з маркуванням 4,0 мл та об'ємом наповнення 4,2 мл), 1 адаптером для флакона, 1 голкою для введення та 1 стержнем поршня в картонній упаковці; 1 флакон з порошком у комплекті з 1 попередньо наповненим шприцом з розчинником (вода для ін'єкцій) по 5 мл з маркуванням 4,0 мл та об'ємом наповнення 4,2 мл, 1 адаптером для флакона, 1 голкою для введення та 1 стержнем поршня (з маркуванням англійською мовою) в картонній упаковці