Кеппра®
Регистрационный номер: UA/9155/02/01
Импортёр: ЮСБ Фарма С.А.
Страна: БельгияАдреса импортёра: Алле где ля Решерш 60, В- 1070 Брюссель - Бельгия
Форма
раствор оральный, 100 мг/мл по 300 мл в флаконе; по 1 флакону с мерным пластиковым шприцем в пачке из картона
Состав
1 мл раствора содержит леветирацетаму 100 мг
Виробники препарату «Кеппра®»
Страна производителя: Франция
Адрес производителя: 17 Роуте де Меулан, 78520 Лимау, Франция
Данный текст является неофициальным переводом с украинской версии.
Инструкция по применению
для медицинского применения лекарственного средства
КЕППРА®
(Keppra®)
Состав
действующее вещество: levetiracetam;
1 мл раствора содержит леветирацетаму 100 мг;
вспомогательные вещества: кислота лимонная моногидрат, аммонию глициризинат, натрию цитрат, метилпарабен(Е 218), пропилпарабен(Е 216), глицерин 85 % (Е 422), мальтит жидкий(Е 965), калию ацесульфам(Е 950), вкусовая добавка виноградная Firmenich 501040A, вода очищена.
Врачебная форма. Раствор оральный.
Основные физико-химические свойства: прозрачная жидкость.
Фармакотерапевтична группа. Противоэпилептические средства. Леветирацетам.
Код ATX N03A Х14.
Фармакологические свойства.
Фармакодинамика.
Леветирацетам, активное вещество, есть производным пиролидону(S- энантиомер альфа-етил-2-оксо-1-пиролидин-ацетамиду), за химической структурой отличается от известных противоэпилептических лекарственных средств.
Механизм действия леветирацетаму недостаточно изучен, но установлено, что он отличается от механизма действия известных противоэпилептических препаратов. На основании проведенных исследований in vitro и in vivo допускают, что леветирацетам не изменяет основные характеристики нервной клетки и нормальную нейротрансмиссию. Исследование іn vitro показали, что леветирацетам влияет на внутришненейрональни уровни Са2+ путем частичного притеснения тока через Са2+ каналы N- типа и снижения высвобождения Ca2+ из интранейрональних депо. Он также частично нивелирует притеснение ГАМК- и глицин-регулеваного току, предопределенное действием цинка и β-карболинами. Кроме того, в ходе исследований in vitro леветирацетам связывался со специфическими участками в тканях мозга грызунов. Местом связывания является белок синаптичних везикул 2А, что участвует в слиянии везикул и высвобождении нейротрансмиттеров. Родство(в ранговом порядке) леветирацетаму и соответствующих аналогов с белком синаптичних везикул 2А коррелировала с мощностью их противосудорожного действия в моделях аудиогенной эпилепсии у мышей. Эти результаты дают возможность допустить, что взаимодействие между леветирацетамом и белком синаптичних везикул 2А может частично объяснять механизм противоэпилептического действия препарата.
Леветирацетам обеспечивает защиту от судорог в широком спектре моделей парциальных и первично генерализуемых нападений у животных, не вызывая просудомного эффекта. Основной метаболит неактивный.
У человека активность препарата подтверждена как относительно фокальных, так и генерализуемых эпилептических нападений(эпилептиформные проявления/фотопароксизмальная реакция), что свидетельствует о широком спектре фармакологического профиля леветирацетаму.
Фармакокинетика.
Леветирацетам характеризуется высокой растворимостью и проницаемостью. Фармакокинетика носит линейный характер, не зависит от времени и характеризуется низкой миж- и интрасубъектной переменчивостью. После повторного применения препарата клиренс не изменяется. Признаков влияния пола, расы или циркадного ритма на фармакокинетику не отмечалось. Профиль фармакокинетики был подобным у здоровых добровольцев и больных эпилепсией.
Благодаря полному и линейному всасыванию уровни препарата в плазме можно предусмотреть, исходя из пероральной дозы леветирацетаму, выраженной в мг/кг массы тела. Поэтому отслеживать плазменные уровни леветирацетаму нет потребности.
У взрослых и детей отмечалась значительная корреляция между концентрацией препарата в слюне и плазме(соотношение концентраций в слюне/плазме колебалось от 1 до 1,7 после приема таблеток для перорального приложения и через 4 часы после приема орального раствора).
Взрослые и подростки
Всасывание.
Леветирацетам быстро всасывается после перорального приложения. Абсолютная пероральная биодоступность близка до 100 %. Пиковые концентрации в плазме крови(Cmax) достигаются через 1,3 часы после приема препарата. Равновесное состояние достигается через 2 дни применения препарата дважды на сутки. Пиковые концентрации(Cmax) обычно представляют 31 и 43 мкг/мл после разовой дозы 1000 мг и повторной дозы 1000 мг дважды на день соответственно. Степень всасывания не зависит от дозы и не изменяется под действием еды.
Распределение.
Данных относительно распределения препарата в тканях человека нет. Ни леветирацетам, ни его основной метаболит значительным образом не связываются с белками плазмы крови(< 10 %). Объем распределения леветирацетаму представляет от 0,5 до 0,7 л/кг, который приблизительно равняется общему объему воды в организме.
Метаболизм.
Метаболизм леветирацетаму у человека незначителен. Основным путем метаболизма(24 % дозы) является ферментный гидролиз ацетамидной группы. Ізоформи печеночного цитохрома Р450 не берут участия в образовании основного метаболиту - ucb L057. Гидролиз ацетамидной группы наблюдался в большом количестве тканей, включая клетки крови. Метаболіт ucb L057 фармакологически неактивный.
Также были определены два второстепенных метаболити. Один образовывался в результате гидроксилирования пиролидонового кольца(1,6 % от дозы), второй - в результате размыкания пиролидонового кольца(0,9 % от дозы).
Другие неопределенные компоненты представляли лишь 0,6 % от дозы.
Взаимного превращения энантиомеров леветирацетаму или его основного метаболиту в условиях in vivo не наблюдалось.
В ходе исследований іn vitro леветирацетам и его основные метаболит не подавляли активность основных изоформ печеночного цитохрома Р450 человека(CYP3A4, 2A6, 2C9, 2C19, 2D6, 2E1 и 1A2), глюкуронилтрансферази(UGT1A1 и UGT1A6) и епоксидгидроксилази. Также леветирацетам не подавляет глюкуронидацию вальпроевой кислоты in vitro.
В культуре гепатоцитов человека леветирацетам обнаруживал слабое влияние или же вовсе не влиял на CYP1A1/2, SULT1E1 или UGT1A1. В высоких концентрациях(680 мкг/мл) леветирацетам вызывал слабую индукцию CYP2B6 и CYP3A4, однако в концентрациях, подобных к Cmax после повторного приложения 1500 мг дважды на сутки, это влияние не было биологически значимым. Даны in vitro и даны in vivo относительно взаимодействия с пероральными контрацептивами, дигоксином и варфарином указывают на то, что в условиях in vivo значимой индукции ферментов не ожидается. Поэтому взаимодействие леветирацетаму с другими веществами маловероятно.
Выведение.
Период полувыведения препарата из плазмы у взрослых представлял 7±1 год и не зависел от дозы, пути введения или повторного приложения. Средний общий клиренс представлял 0,96 мл/хв/кг.
Основное количество препарата, в среднем 95 % дозы, выводилось почками(приблизительно 93 % дозы выводились в течение 48 часов). С калом выводится лишь 0,3 % дозы.
Кумулятивное выведение с мочой леветирацетаму и его основного метаболиту представляло 66 % и 24 % от дозы соответственно в первые 48 часы. Почечный клиренс леветирацетаму и ucb L057 представляет 0,6 и 4,2 мл/хв/кг соответственно, что свидетельствует о выведении леветирацетаму путем гломерулярной фильтрации с дальнейшей реабсорбцией в канальцях и что основной метаболит также выводится путем активной канальцевой секреции в придачу к гломерулярной фильтрации. Выведение леветирацетаму коррелирует с клиренсом креатинина.
Пациенты пожилого возраста.
У летних пациентов период полувыведения растет приблизительно на 40 % (10-11 часы). Это связано с ухудшением функций почек у данной популяции(см. раздел "Способ применения и дозы").
Нарушение функции почек.
Видимый общий клиренс леветирацетаму и его основного метаболиту коррелирует с клиренсом креатинина. Поэтому пациентам с умеренными и тяжелыми нарушениями функции почек рекомендуется корректировать пидтримуючу суточную дозу леветирацетаму в соответствии с клиренсом креатинина(см. раздел "Способ применения и дозы").
У пациентов с анурией в терминальной стадии болезни почек период полувыведения представлял приблизительно 25 и 3,1 часы соответственно в период между сеансами диализа и во время его проведения. В течение фракционного 4-часового сеанса диализа выводилось 51 % леветирацетаму.
Нарушение функции печенки.
Фармакокинетика леветирацетаму не изменялась у пациентов с легкими и умеренными нарушениями функции печенки(класс А и В за шкалой Чайлда - Пью). У пациентов с тяжелыми нарушениями функции печенки(класс С за шкалой Чайлда - Пью) общий клиренс был на 50 % ниже, чем у пациентов с нормальной функцией печенки, но это было предопределенно преимущественно сопутствующим снижением почечного клиренса(см. раздел "Способ применения и дозы").
Пациентам с легкими и умеренными нарушениями функции печенки коррекция дозы не нужна. У пациентов с тяжелым нарушением печеночных функций клиренс креатинина может не в полной мере отображать тяжесть почечной недостаточности. Тому, если клиренс креатинина представляет < 60 мл/хв/1,73 м2, пидтримуючу суточную дозу рекомендуется уменьшить на 50 % (см. раздел "Способ применения и дозы").
Педиатрическая популяция.
Деть возрастом 4-12 годы.
После применения разовой дозы(20 мг/кг) у детей, больных эпилепсией(от 6 до 12 лет), период полувыведения леветирацетаму представлял 6 часы. Видимый клиренс, откорректированный с учетом массы тела, был приблизительно на 30 % выше, чем у взрослых пациентов с эпилепсией. После повторного перорального приложения(20-60 мг/кг/сутки) у больных эпилепсией детей(4-12 годы) леветирацетам всасывался быстро. Пиковые концентрации в плазме крови достигались через 0,5-1 час после приема дозы. Пиковые концентрации и площадь зоны под кривой зависимости концентрации от времени росли линейно и зависели от дозы. Период полувыведения представлял приблизительно 5 часы; видимый общий клиренс - 1,1 мл/хв/кг.
Младенцы и дети(от 1 месяца до 4 лет).
После разовой дозы(20 мг/кг) орального раствора 100 мг/мл у больных эпилепсией детей(в возрасте от 1 месяца до 4 лет) леветирацетам всасывался быстро, пиковые концентрации в плазме крови наблюдались приблизительно через 1 час после приема дозы препарата. Фармакокінетичні показатели свидетельствовали, что период полувыведения был короче(5,3 часы), чем у взрослых(7,2 часы), а видимый клиренс быстрее(1,5 мл/хв/кг), чем у взрослых(0,96 мл/хв/кг).
Результаты популяционного анализа фармакокинетики, проведенного у пациентов в возрасте от 1 месяца до 16 лет, свидетельствовали о значительной корреляции массы тела с видимым клиренсом(клиренс рос при увеличении массы тела) и видимым объемом распределения. Возраст также влиял на оба параметра. Этот эффект был более выражен у младенцев младшего возраста, при росте уменьшался и был исчезающе малым у детей возрастом около 4 лет.
Данные обоих популяционных фармакокинетичних анализов свидетельствовали о росте видимого клиренса леветирацетаму приблизительно на 20 % при сопутствующем применении фермент-индукуючих противоэпилептических препаратов.
Клинические характеристики
Показание
Монотерапия(препарат первого выбора) при лечении:
- парциальных нападений со вторичным генерализованием или без такой у взрослых и подростков в возрасте от 16 лет, в которых впервые диагностирована эпилепсия.
Как дополнительная терапия при лечении:
- парциальных нападений со вторичным генерализованием или без такой у взрослых и детей в возрасте от 1 месяца, больных эпилепсией;
- миоклоничних судорог у взрослых и подростков от 12 лет, больных ювенильной миоклоничну эпилепсией;
- первичных генерализуемых тоніко-клонічних нападений у взрослых и подростков в возрасте от 12 лет, больных идиопатической генерализуемой эпилепсией.
Противопоказание
Повышенная чувствительность к леветирацетаму или к другим производным пиролидону, а также к любым вспомогательным веществам препарата.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Противоэпилептические препараты.
Предрегистрационные данные, полученные в ходе клинических исследований, проведенных при участии взрослых пациентов, указывают на то, что леветирацетам не оказывает влияния на другие противоэпилептические препараты(фенитоин, карбамазепин, вальпроева кислота, фенобарбитал, ламотриджин, габапентин и примидон), а они, в свою очередь, не влияют на фармакокинетику леветирацетаму.
Отсутствующие даны относительно клинически значимого взаимодействия лекарственного средства у пациентов детского возраста, как и у взрослых, которые получали до 60 мг/кг/время леветирацетаму.
Ретроспективная оценка фармакокинетичной взаимодействия у детей и подростков с эпилепсией(от 4 до 17 лет) подтвердила, что вспомогательная терапия с пероральным применением леветирацетаму не влияла на равновесные сывороточные концентрации одновременно примененных карбамазепину и вальпроату. Однако данные свидетельствуют, что клиренс леветирацетаму на 20 % более высок у детей, которые принимают ферментовмисни противосудорожные средства. Коррекция дозы не нужна.
Пробенецид.
Пробенецид(500 мг 4 разы на сутки) - препарат, который блокирует секрецию почечных канальцив, подавляет почечный клиренс основного метаболиту, но не самого леветирацетаму. Однако концентрации этого метаболиту остаются низкими. Ожидается, что другие препараты, которые выводятся с помощью активной канальциевой секреции, также способны снижать почечный клиренс метаболиту. Влияние леветирацетаму на пробенецид не исследовалось, влияние леветирацетаму на другие препараты, которые активно секретируются, например нестероидные противовоспалительные препараты и сульфонамид, неизвестный.
Метотрексат.
Сообщалось, что одновременное применение леветирацетаму и метотрексату снижает клиренс метотрексату, что приводит к увеличению/удлинения концентрации метотрексату в крови к потенциально токсичным уровням. Уровни метотрексату и леветирацетаму в крови следует тщательным образом контролировать у пациентов, которые получают лечение двумя препаратами одновременно.
Пероральные контрацептивы и фармакокинетични взаимодействия с другими препаратами.
Леветирацетам в суточной дозе 1000 мг не изменяет фармакокинетику пероральных противозачаточных средств(етинилестрадиолу и левоноргестрелу); эндокринные показатели(уровни ЛГ и прогестерону) не изменялись. Леветирацетам в суточной дозе 2000 мг не изменяет фармакокинетику дигоксина и варфарину; значения протромбинового времени оставались неизмененными. Дигоксин, пероральные противозачаточные средства и варфарин, в свою очередь, не влияют на фармакокинетику леветирацетаму при одновременном приложении.
Слабительные средства.
В отдельных случаях сообщали о снижении эффективности леветирацетаму при одновременном применении осмотического слабительного средства макроголу с пероральным леветирацетамом. Поэтому не следует принимать макрогол перорально в течение одного часа до и в течение одного часа после приема леветирацетаму.
Антациды.
Нет данных о влиянии антацидных препаратов на всасывание леветирацетаму.
Еда и алкоголь.
Степень всасывания леветирацетаму не зависит от еды, но скорость всасывания несколько снижена в случае приема вместе с едой. Нет данных о взаимодействии леветирацетаму с алкоголем.
Особенности применения
Прекращение лечения.
В случае необходимости прекращения приема препарата отмену рекомендуется проводить постепенно(например для взрослых и подростков с массой тела 50 кг и больше - уменьшать дозу 500 мг дважды на сутки каждые 2-4 недели; для младенцев в возрасте от 6 месяцев, детей и подростков с массой тела менее 50 кг следует снижать дозу не более чем на 10 мг/кг дважды на сутки каждые 2 недели; для младенцев в возрасте до 6 месяцев дозу следует снижать не более чем на 7 мг/кг дважды на сутки каждые 2 недели).
Почечная недостаточность.
Пациенты с почечной недостаточностью могут нуждаться коррекции дозы леветирацетаму. У пациентов с тяжелыми нарушениями печеночной функции рекомендуется провести оценку функции почек перед тем, как назначать дозу препарата(см. раздел "Способ применения и дозы").
Острое поражение почек.
Применение леветирацетаму очень редко сопровождалось острым поражением почек, время до возникновения которого колебалось от нескольких дней до несколько месяцев.
Общий анализ крови.
Были описаны жидкие случаи снижения количества клеток крови(нейтропения, агранулоцитоз, лейкопения, тромбоцитопения и панцитопения) в связи с применением леветирацетаму - как правило, в начале лечения. Рекомендуется проводить полный анализ крови пациентам, в которых наблюдается значительная слабость, лихорадка, рецидивные инфекции или нарушения свертывания крови(см. раздел "Побочные реакции").
Суицид.
У пациентов, которые получали лечение противоэпилептическими препаратами(в т. ч. леветирацетамом), отмечались случаи суицида, попыток суицида и суицидальних мыслей и поведения. Цель-анализ результатов рандомизированных, плацебо-контролируемых испытаний противоэпилептических лекарственных средств показал некоторое увеличение риску возникновения суицидальних мыслей и поведения. Механизм возникновения такого риска не изучен. В связи с наличием такого риска состояние пациентов следует контролировать относительно признаков депрессии, суицидальних мыслей и поведения и при необходимости корректировать лечение. Пациентов(или их опекунов) следует предупредить о необходимости сообщать о любых симптомах депрессии, суицидальних мыслей и поведения своему врачу.
Деть.
Имеются даны относительно пациентов детского возраста не указывают на наличие влияния на рост, половое дозревание. Но отдаленные последствия относительно возможностей учебы, интеллекта, роста эндокринных функций, полового дозревания, репродуктивного потенциала у детей не изучены.
Не достаточно данных относительно безопасности применения препарата у детей с эпилепсией в возрасте до 1 года: лишь 35 дети в возрасте до 1 года с парциальными судорогами принимали участие в клинических исследованиях и только 13 из них были в возрасте до 6 месяцев.
Вспомогательные вещества.
Препарат содержит метилпарабен(E218) и пропилпарабен(E216), что могут вызывать аллергические проявления(возможно, отсроченные). Он также содержит мальтит жидкий, потому пациентам с редкими наследственными заболеваниями, которые связаны с непереносимостью фруктозы, употребления противопоказано.
Применение в период беременности или кормления груддю.
Беременность.
Результаты исследований на животных свидетельствуют о наличии репродуктивной токсичности. Анализ данных около 1000 женщин из реестров беременных, которым применяли монотерапию леветирацетамом в течение первого триместру беременности, не подтвердил существенное увеличение риска тяжелых аномалий развития, хотя тератогенный риск не может быть полностью исключен. Применение нескольких противоэпилептических средств потенциально увеличивает вероятность возникновения аномалий развития плода, сравнительно с монотерапией. Леветирацетам не следует применять в период беременности, кроме случаев абсолютной необходимости, а также женщинам детородного возраста, которые не применяют контрацепцию. Физиологичные изменения в период беременности могут изменять концентрацию леветирацетаму. Во время беременности наблюдалось снижение плазменной концентрации леветирацетаму. Такое снижение наиболее выражено в третьем триместре(до 60 % от исходной концентрации к беременности). Следует обеспечить надлежащий клинический надзор за беременными женщинами, которые получают леветирацетам. Прекращение применения противоэпилептических средств может привести к обострению болезни, которая может навредить матери и плоду.
Кормление груддю.
Леветирацетам проникает в грудное молоко женщины. Поэтому кормление груддю не рекомендовано. Однако если леветирацетам необходимо применять в период кормления груддю, следует взвесить пользу и риски лечения и важность кормления груддю.
Влияние на детородную функцию.
Не выявлено влиянию на детородную функцию в исследованиях на животных. Потенциальный риск для человека неизвестен, потому что нет доступных клинических данных.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Леветирацетам незначительно или умеренно влияет на способность руководить автотранспортом или работать с другими механизмами. Через возможную индивидуальную чувствительность некоторые пациенты могут отмечать сонливость и другие симптомы, связанные с влиянием на центральную нервную систему, особенно в начале лечения или в процессе увеличения дозы. Поэтому таким пациентам следует быть осторожными при занятии деятельностью, которая нуждается повышенной концентрации внимания, например при управлении автомобилем или работе с механизмами. Пациентам рекомендуется воздерживаться от управления автотранспортными средствами и работы с другими механизмами до тех пор, пока не будет установлено, что их способность заниматься такой деятельностью не нарушена.
Способ применения и дозы
Препарат применять внутренне, независимо от приема еды. Раствор оральный можно принимать после разведения в стакане воды или бутылке для кормления. Суточную дозу распределять на два одинаковых приема.
Монотерапия
Взрослые и подростки в возрасте от 16 лет.
Монотерапию у взрослых и подростков в возрасте от 16 лет рекомендовано начинать с дозы 500 мг/сутки(по 250 мг 2 разы на сутки). Через 2 недели дозу можно увеличить к начальной терапевтической - 1000 мг/сутки(по 500 мг 2 разы на сутки). Дальше дозу можно увеличивать на 250 мг дважды на сутки каждые две недели в зависимости от клинического ответа. Максимальная суточная доза представляет 3000 мг/сутки(по 1500 мг 2 разы на сутки).
Дети и подростки в возрасте до 16 лет.
Безопасность и эффективность применения препарата Кеппра® детям и подросткам до 16 лет как монотерапии не установлены.
Данные отсутствуют.
Дополнительная терапия
Врач должен назначить наиболее соответствующую врачебную форму, способ применения и количество приемов препарата в зависимости от возраста, массы тела и дозы.
Взрослые и подростки(12-17 годы) с массой тела от 50 кг
Начальная терапевтическая доза представляет 1000 мг/сутки(по 500 мг х 2 разы на сутки). Из этой дозы можно начинать в первый день лечения.
В зависимости от клинического ответа и переносимости суточную дозу можно увеличить до 3000 мг/сутки(1500 мг 2 разы на сутки). Дозу можно увеличивать или уменьшать на 1000 мг/сутки(500 мг 2 разы на сутки) каждые 2-4 недели.
Младенцы возрастом 6-23 месяцы, дети(2-11 годы) и подростки(12-17 годы) с массой тела менее 50 кг
Начальная терапевтическая доза представляет 10 мг/кг дважды на сутки.
В зависимости от клинического ответа и переносимости дозу можно увеличивать до 30 мг/кг дважды на сутки. Дозу нельзя увеличивать или уменьшать больше чем на 10 мг/кг дважды на сутки каждые две недели. Следует применять наименьшую эффективную дозу.
Детям с массой тела 50 кг и больше применять те же дозы, что и взрослым.
Рекомендованные дозы для младенцев в возрасте от 6 месяцев, детей и подростков :
|
Масса тела |
Начальная доза - 10 мг/кг дважды на сутки |
Максимальная доза - 30 мг/кг дважды на сутки |
|
6 кг(1) |
60 мг(0,6 мл) дважды на сутки |
180 мг(1,8 мл) дважды на сутки |
|
10 кг(1) |
100 мг(1 мл) дважды на сутки |
300 мг(3 мл) дважды на сутки |
|
15 кг(1) |
150 мг(1,5 мл) дважды на сутки |
450 мг(4,5 мл) дважды на сутки |
|
20 кг(1) |
200 мг(2 мл) дважды на сутки |
600 мг(6 мл) дважды на сутки |
|
25 кг |
250 мг дважды на сутки |
750 мг дважды на сутки |
|
От 50 кг(2) |
500 мг дважды на сутки |
1500 мг дважды на сутки |
( 1) Детям с массой тела 25 кг или меньшее лечение следует начать препаратом Кеппра®, 100 мг/мл, раствор оральный.
( 2) Детям с массой тела 50 кг и больше применять те же дозы, что и взрослым.
Младенцы в возрасте от 1 к <6 месяцы
Начальная терапевтическая доза представляет 7 мг/кг дважды на сутки.
В зависимости от клинического ответа и переносимости дозу можно увеличивать до 21 мг/кг дважды на сутки. Дозу нельзя увеличивать или уменьшать больше чем на 7 мг/кг дважды на сутки каждые две недели. Следует применять наименьшую эффективную дозу.
Младенцам лечения следует начать препаратом Кеппра®, 100 мг/мл, раствор оральный.
Дозы, рекомендованные для младенцев в возрасте от 1 до 6 месяцев, :
|
Масса тела |
Начальная доза - 7 мг/кг дважды на сутки |
Максимальная доза - 21 мг/кг дважды на сутки |
|
4 кг |
28 мг(0,3 мл) дважды на сутки |
84 мг(0,85 мл) дважды на сутки |
|
5 кг |
35 мг(0,35 мл) дважды на сутки |
105 мг(1,05 мл) дважды на сутки |
|
7 кг |
49 мг(0,5 мл) дважды на сутки |
147 мг(1,5 мл) дважды на сутки |
Особенные группы пациентов
Пациенты пожилого возраста
Коррекция дозы у летних пациентов необходима только в случае имеющихся нарушений функции почек(см. раздел "Пациенты с нарушением функции почек").
Пациенты с нарушением функции почек
Суточную дозу леветирацетаму необходимо подбирать индивидуально.
Взрослым пациентам дозу препарата следует корректировать, как показано в таблицах ниже. Для корректировки дозы за таблицей необходимо определить клиренс креатинина пациента(КК) в мл/мин.
У взрослых и подростков с массой тела 50 кг и больше КК в мл/хв можно рассчитать за уровнем креатинина в сыворотке крови(мг/дл) за такой формулой:
[ 140 ─ веки(в годах)] × масса тела(кг)
КК(мл/хв) =3D -------------------------------------------------------------- × 0,85(для женщин).
72 × КК сыворотки крови(мг/дл)
Потом КК откорректировать в соответствии с площадью поверхности тела(ППТ), как показано дальше:
КК(мл/хв)
КК(мл/хв/1,73м2) =3D --------------------------- ×1,73.
ППТ пациента(м2)
Рекомендации относительно коррекции дозы для взрослых пациентов и подростков с массой тела 50 кг и больше с нарушением функции почек.
|
Степень тяжести почечной недостаточности |
Клиренс креатинина(мл/хв/1,73 м2) |
Режим дозирования |
|
Нормальная функция почек |
>80 |
от 500 до 1500 мг 2 разы на сутки |
|
Легкая степень |
50-79 |
от 500 до 1000 мг 2 разы на сутки |
|
Средняя степень |
30-49 |
от 250 до 750 мг 2 разы на сутки |
|
Тяжелая степень |
<30 |
от 250 до 500 мг 2 разы на сутки |
|
Терминальная стадия(пациенты, которые находятся на диализе(1)) |
- |
от 500 до 1000 мг 1 раз в сутки(2) |
( 1) В первый день лечения рекомендуется применить погрузочную дозу леветирацетаму 750 мг.
( 2) После диализа рекомендуется применить дополнительную дозу 250-500 мг.
Для детей с почечной недостаточностью дозу леветирацетаму необходимо корректировать в соответствии с почечной функцией, поскольку клиренс леветирацетаму связан с почечной функцией. Эта рекомендация основывается на исследовании при участии взрослых пациентов с нарушением почечной функции.
Для подростков, детей и младенцев КК в мл/хв/1,73 м2 можно рассчитать, исходя из концентрации креатинина в сыворотке(мг/дл), применяя такую формулу(формула Шварца) :
Рост(см) × ks
КК(мл/хв/1,73 м2) =3D ---------------------------------.
КК сыворотки крови(мг/дл)
У доношенных младенцев в возрасте до 1 года ks =3D 0,45; у детей в возрасте до 13 лет и подростков-девочек ks =3D 0,55; у подростков-ребят ks =3D 0,7.
Рекомендации относительно коррекции дозы для младенцев, детей и подростков с массой тела менее 50 кг с нарушением функции почек.
|
Степень тяжести почечной недостатно-сти |
Клиренс креатини-ну(мл/хв/1,73 м2) |
Доза и частота применения(1) |
|
|
Младенцы в возрасте от 1 к < 6 месяцы |
Младенцы в возрасте от 6 к 23 месяцев, дети и подростки с массой тела менее 50 кг |
||
|
Нормальная функция почек |
> 80 |
7-21 мг/кг ( 0,07-0,21 мл/кг) дважды на сутки |
10-30 мг/кг(0,1-0,3 мл/кг) дважды на сутки |
|
Легкая степень |
50-79 |
7-14 мг/кг ( 0,07-0,14 мл/кг) дважды на сутки |
10-20 мг/кг(0,1-0,2 мл/кг) дважды на сутки |
|
Средняя степень |
30-49 |
3,5-10,5 мг/кг ( 0,035-0,105 мл/кг) дважды на сутки |
5-15 мг/кг(0,05-0,15 мл/кг) дважды на сутки |
|
Тяжелая степень |
< 30 |
3,5-7 мг/кг ( 0,035-0,07 мл/кг) дважды на сутки |
5-10 мг/кг(0,05-0,1 мл/кг) дважды на сутки |
|
Терминальная стадия(пациенты, которые находятся на диализе) |
-- |
7-14 мг/кг ( 0,07-0,14 мл/кг) один раз на сутки(2) (4) |
10-20 мг/кг(0,1-0,2 мл/кг) один раз на сутки(3) (5) |
( 1) Для дозирования до 250 мг, для доз, не кратные 250 мг, когда рекомендованное дозирование невозможно получить приемом нескольких таблеток, а также для пациентов, которые не могут проглотить таблетку, следует применять Кеппра®, раствор оральный.
( 2) В первый день лечения рекомендуется применить погрузочную дозу леветирацетаму 10,5 мг/кг(0,105 мл/кг).
( 3) В первый день лечения рекомендуется применить погрузочную дозу леветирацетаму 15 мг/кг(0,15 мл/кг).
( 4) После диализа рекомендуется применить дополнительную дозу 3,5-7 мг/кг(0,035-0,07 мл/кг).
( 5) После диализа рекомендуется применить дополнительную дозу 5-10 мг/кг(0,05-0,1 мл/кг).
Пациенты с нарушением функции печенки
Коррекция дозы не нужна для пациентов со слабым и умеренным нарушением функции печенки. У пациентов с тяжелыми нарушениями функции печенки клиренс креатинина может не в полной мере отображать степень почечной недостаточности. Поэтому пациентам с клиренсом креатинина < 60 мл/хв/1,73м2 суточную пидтримуючу дозу рекомендовано уменьшить на 50 %.
Деть
Врач должен назначать наиболее соответствующую врачебную форму, дозирование и форму выпуска в зависимости от возраста, массы тела и дозы.
Младенцам и детям в возрасте до 6 лет желательно применять препарат Кеппра® в форме раствора орального. Кроме того, имеющиеся дозирования таблеток не подходят для начального лечения детей с массой тела до 25 кг, для пациентов, которые не могут проглотить таблетку, или для применения доз до 250 мг. В этих случаях следует применять препарат Кеппра® в форме раствора орального.
Метод применения раствора орального
Дозирование осуществлять с помощью мерного шприца|шприц-машины|, что добавляется в упаковке.
Шприцы|шприц-машины| номинальной емкости|вместимости|:
· 10 мл(отвечает 1000 мг леветирацетаму) с подилкой 0,25 мл(отвечает 25 мг) для детей в возрасте от 4 лет, подростков и взрослых;
· 3 мл| (отвечает 300 мг|миллиграммовых эквивалентов|) из|с| подилкой 0,1 мл| (отвечает 10 мг|миллиграммовых эквивалентов|) для младенцев и детей младшего возраста от 6 месяцев до < 4 годов;
· 1 мл(отвечает 100 мг) с подилкой 0,05 мл(отвечает 5 мг) для младенцев в возрасте от 1 к < 6 месяцы.
Отмеряющую дозу разводить в стакане воды(200 мл|) или в бутылке для кормления.
Дозирование раствора с помощью мерного шприца|шприц-машины|:
· открыть|отворять| флакон, нажав|нажимать| на колпачок и повернув|повернуть| его против|против| часовой стрелки(рис. 1);
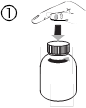
· отделить переходник от шприца(рис. 2); вставить переходник в шейку флакона(рис. 3). Убедиться в том, что он надежно закреплен;

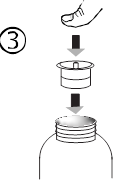
· вставить шприц|шприц-машину| в открытый переходник(рис. 4);перевернуть|переворачивать| флакон дном кверху(рис. 5);
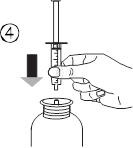

· набрать в шприц|шприц-машину| небольшое количество раствора, потянув поршень вниз(рис. 5А), потом нажать на поршень, чтобы|если бы| удалить|уничтожать| любые пузырьки(рис. 5В);
· наполнить шприц|шприц-машину| раствором, потянув поршень к отметке, которая отвечает необходимому количеству раствора в миллилитрах, назначенному врачом|врачом| (рис. 5С);



· перевернуть|переворачивать| флакон дном книзу(рис. 6А). Вынуть шприц|шприц-машину| из|из| переходника(рис. 6В);

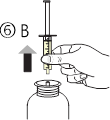
· ввести|вводить| содержимое шприца|шприц-машины| в стакан из|с| водой или бутылку для кормления, прижав|нажимать| поршень к дну шприца(рис. 7);
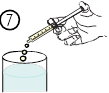
· выпить полностью|полностью| содержимое стакана/ бутылки для кормления;|стаканы|
· закрыть флакон пластиковым колпачком;
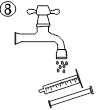
· промыть шприц|шприц-машину| водой(рис. 8).
Деть.
Кеппра®, раствор для орального приложения можно назначать детям от 1 месяца до 6 лет. Врач проводит подбор оптимальной врачебной формы, силы действия в зависимости от возраста, массы тела и дозы. Препарат не рекомендован для применения детям в возрасте до 1 месяца в связи с отсутствием данных относительно безопасности и эффективности препарата. Необходимо иметь в виду, что нельзя применять препарат в форме таблеток для начального лечения детей с массой тела ниже 25 кг в случаях назначения высоких доз; у пациентов, которые не могут глотать таблетку; для применения в дозах, ниже 250 мг; в таких случаях необходимо применять в форме раствора для перорального приложения.
Безопасность и применение препарата в качестве монотерапии для детей и подростков до 16 лет не установлена.
Передозировка
Симптомы.
При передозировке препарата Кеппра® наблюдались сонливость, возбуждение, агрессия, притеснение дыхания, притеснения сознания, запятая.
Лечение.
В случае острой передозировки необходимо промывать желудок или вызывать блюет. Специального антидота нет. При необходимости проводить симптоматическое лечение, в т. ч. с использованием гемодиализа(выводится до 60 % леветирацетаму и 74 % первичного метаболиту).
Побочные реакции
Чаще всего сообщалось о таких побочных реакциях, как назофарингит, сонливость, головная боль, повышенная утомляемость и головокружение. Профиль побочных явлений, который приводится, основывается на обобщающем анализе данных плацебо-контролируемых клинических испытаний, в которых в целом участвовали 3416 пациенты, которые получали леветирацетам. Эти данные дополняются использованием леветирацетаму в соответствующих расширенных открытых исследованиях, а также постмаркетинговым опытом. Профиль безопасности леветирацетаму, как правило, похожий в разных возрастных группах(взрослые и дети) при применении за разными установленными показаниями.
Побочные реакции, о которых сообщалось в клинических исследованиях(касательно взрослых, подростков, детей и младенцев в возрасте от 1 месяца) и в течение постмаркетингового периода, перечислены в следующей таблице по системе Классификации Органов и Систем с определением их частоты. Частота определяется таким образом: очень часто(≥ 1/10); часто(≥ 1/100 к < 1/10); нечасто(≥ 1/1000 к < 1/100); редко(≥ 1/10000 к < 1/1000) и очень редко(< 1/10000).
|
Классы систем органов за MedDRA |
Частота побочных реакций |
|||
|
очень часто (≥ 1/10) |
часто ( ≥ 1/100 к < 1/10) |
нечасто ( ≥ 1/1000 к < 1/100) |
редко ( ≥ 1/10000 к < 1/1000) |
|
|
Инфекции и инвазия |
Назофарингит |
Инфекции |
||
|
Расстройства со стороны кровеносной и лимфатической систем |
Тромбоцитопения лейкопения |
Нейтропения, панцитопения агранулоцитоз |
||
|
Расстройства со стороны иммунной системы |
Реакция на лекарственное средство из еозинофилеею и синдромом гиперчувствительности к лекарственному средству(DRESS- синдром), гиперчувствительность(включая ангионевротический отек и анафилаксию) |
|||
|
Расстройства питания и обмена веществ |
Анорексия |
Увеличение массы тела, уменьшения массы тела |
Гіпонатріємія |
|
|
Психические расстройства |
Депрессия, враждебность/ агрессивность тревожность, бессонница раздражительность |
Попытки самоубийства изменения настроения, возбуждения |
Суицид, расстройства личности, аномальное мышление |
|
|
Расстройства со стороны нервной системы |
Сонливость, головная боль |
Судороги, нарушения равновесия, головокружения летаргия, тремор |
Амнезия, нарушение памяти, атаксия, нарушение координации парестезия, расстройства внимания |
Гиперкинезия, дискинезия, хореоатетоз |
|
Расстройства со стороны органов зрения |
Диплопия, размытость зрения |
|||
|
Расстройства со стороны органов слуха и равновесия |
Вертиго |
|||
|
Расстройства со стороны органов дыхания, грудной клетки и средостения |
Кашель |
|||
|
Желудочно-кишечные расстройства |
Диарея, диспепсия, тошнота, блюет, боль в животе |
Панкретит |
||
|
Гепатобіліарні расстройства |
Отклонение от нормы результатов печеночных проб |
Гепатит, печеночная недостаточность |
||
|
Нарушение со стороны почек и сечевидильной системы |
Острое поражение почек |
|||
|
Расстройства со стороны кожи и подкожной клетчатки |
Высыпание |
Экзема, зуд, аллопеция |
Токсичный эпидермальный некролиз, синдром Стівенса - Джонсона, мультиформна эритема |
|
|
Расстройства со стороны скелетной мускулатуры и соединительной ткани |
Миалгия, мышечная слабость |
Рабдоміоліз и повышение уровня креатинфосфокинази в крови* |
||
|
Общие расстройства и расстройства в месте введения |
Астения/ утомляемость |
|||
|
Травмы, отравления и процедурные осложнения |
Травмы |
* Распространенность значимо более высока у японцев сравнительно с пациентами не японского происхождения.
Редко наблюдались случаи энцефалопатии, которая возникала после применения леветирацетаму. Эти нежелательные эффекты, как правило, возникали в начале лечения(от нескольких дней до несколько месяцев) и были оборотными после прекращения лечения.
Описание отдельных побочных реакций.
Риск анорексии растет при одновременном применении леветирацетаму из топираматом.
При проявлениях аллопеции в некоторых случаях отмечалось возобновление волосяного покрова после прекращения применения леветирацетаму.
При проявлениях панцитопении в некоторых случаях наблюдалось притеснение костного мозга.
Возможны проявления аллергических реакций на леветирацетам или вспомогательные вещества, которые содержатся в препарате.
Деть.
Среди пациентов в возрасте от 1 месяца до 4 лет в целом 190 пациенты получали лечение леветирацетамом в ходе плацебо-контролируемых и открытых дополнительных исследований. 60 из этих пациентов получали лечение леветирацетамом в ходе плацебо-контролируемых исследований. Среди пациентов возрастом 4-16 годы в целом 645 пациенты получали лечение леветирацетамом в ходе плацебо-контролируемых и открытых дополнительных обследований. 233 из этих пациентов получали лечение леветирацетамом в ходе плацебо-контролируемых исследований. В обеих отмеченных возрастных группах эти данные дополнены данными относительно применения леветирацетаму в писляреестрацийний период.
Кроме того, в ходе писляреестрацийного исследования безопасности лечения препаратом получало 101 младенец в возрасте до 12 месяцев. Новых данных из безопасности относительно применения леветирацетаму младенцам с эпилепсией в возрасте до 12 месяцев получено не было.
Профиль побочных реакций леветирацетаму в целом похож в разных возрастных группах и при всех утвержденных показаниях эпилепсии. Результаты относительно безопасности применения препарата детям, полученные в ходе плацебо-контролируемых клинических исследований, отвечали профилю безопасности леветирацетаму у взрослых, кроме побочных реакций со стороны поведения и психики, которые у детей были чаще, чем у взрослых. У детей и подростков в возрасте от 4 до 16 лет блюет(очень часто, 11,2 %), возбужденность(часто, 3,4 %), изменение настроения(часто, 2,1 %), аффективная лабильность(часто, 1,7 %), агрессия(часто, 8,2 %), аномальное поведение(часто, 5,6 %) и летаргия(часто, 3,9 %) наблюдались с большей частотой, чем в других возрастных группах или в общем профиле из безопасности. У младенцев и детей в возрасте от 1 месяца до 4 лет раздражительность(очень часто, 11,7 %) и нарушение координации(часто, 3,3 %) наблюдались с большей частотой, чем в других возрастных группах или в общем профиле из безопасности.
В двойном слепом плацебо-контролируемом исследовании из безопасности для детей, которое проводилось с целью довести не низшую эффективность препарата сравнительно с активным контролем, оценивали влияние леветирацетаму на когнитивные и нейропсихологические показатели у детей в возрасте от 4 до 16 лет с парциальными нападениями. Препарат Кеппра® не отличался(не был менее эффективным) от плацебо относительно изменения от исходного уровня внимания и памяти за шкалой Leiter - R, суммарного показателя проверки памяти в популяции в соответствии с протоколом. Результаты, связанные с поведенческими и эмоциональными функциями, указывали на усиления у пациентов, которых лечили леветирацетамом, агрессивного поведения, которое определялось стандартизировано и систематически, с использованием валидизованих средств(СВСL - Achenbach Child Behavior Checklist - Контрольный список детского поведения Ахенбаха). Однако у пациентов, которые получали леветирацетам в ходе долгосрочного открытого исследования дальнейшего наблюдения, в среднем не наблюдалось ухудшения поведенческих и эмоциональных функций; в частности показатели агрессивного поведения не были хуже исходного уровня.
Отчетность относительно побочных реакций
Отчетность относительно подозреваемых побочных реакций после утверждения лекарственного средства важна. Это позволяет продолжить мониторинг соотношения польза/риск лекарственного средства. Медицинским работникам просят сообщать о любых подозреваемых побочных реакциях через национальную систему отчетности.
Срок пригодности. 3 годы.
Условия хранения.
Хранить в оригинальной упаковке при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Упаковка
По 300 мл в флаконе; по 1 флакону с мерным пластиковым шприцем в пачке из картона с маркировкой украинским языком.
Категория отпуска. За рецептом.
Производитель.
НекстФарма САС, Франция /
NextРharma SAS, France.
Местонахождение производителя и его адрес места осуществления деятельности
17 Роуте де Меулан, 78520 Лімау, Франция /
17 Route de Meulan, 78520 Limay, France.
Заявитель
ЮСБ Фарма С.А., Бельгия /
UCB Рharma S.A., Belgium.
Местонахождение заявителя
Алле где ля Решерш 60, В- 1070 Брюссель, Бельгия /
Allée de la Recherche 60, B-1070 Bruxelles, Belgium.
Другие медикаменты этого же производителя
Форма: таблетки, покрытые пленочной оболочкой, по 800 мг по 15 таблетки в блистере; по 2 блистеры в картонной пачке
Форма: таблетки, покрытые пленочной оболочкой, по 150 мг по 14 таблетки в блистере; по 1 или 4 блистеры в картонной коробке
Форма: таблетки, покрытые пленочной оболочкой, по 50 мг по 14 таблетки в блистере; по 1 или 4 блистеры в картонной коробке
Форма: таблетки, покрытые оболочкой, по 500 мг по 10 таблетки в блистере; по 3 или 6 блистеры в картонной пачке
Форма: таблетки, покрытые пленочной оболочкой, по 100 мг по 14 таблетки в блистере; по 1 или 4 блистеры в картонной коробке